题目内容
【题目】测定空气中氧气体积含量的方法很多,如图所示是小明用红磷在空气中燃烧的测定方法。实验过程如下:
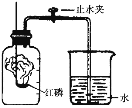
第一步:将集气瓶容积划分为五等份,并做好标记。
第二步:点燃燃烧匙内的红磷,立即伸入集气瓶中并把塞子塞紧。
第三步:待红磷熄灭并冷却后,打开止水夹,观察现象。
(1)第二步中可以观察到的实验现象是:_______________。
(2)第二步中发生的反应文字表达式为:_________________。
(3)实验完毕,若进入集气瓶中水的体积小于总容积的1/5,你认为导致这一结果的原因可能是:_______________。(填一点)
(4)燃烧后,集气瓶内剩余的气体主要是氮气。 请结合本实验推测氮气的化学性质有:______________。(填一点)
(5)已知镁在空气中燃烧不仅会与氧气反应,还会与氮气反应:镁+氮气![]() 氮化镁。根据上述反应,能否用镁代替红磷测定空气成分,理由是:______________。
氮化镁。根据上述反应,能否用镁代替红磷测定空气成分,理由是:______________。
(6)小红同学又提出了新的测定空气中氧气体积含量的方案,如图所示,取一团用食盐水浸泡过的,光亮无锈的铁丝绒,放入一支洁净的试管的底部,将试管倒放在一个盛有水的烧杯中。与上面装置相比,你认为此装置的优点是:_____________。

【答案】红磷燃烧,产生大量白烟,放出热量 磷+氧气![]() 五氧化二磷 红磷量不足(或装置漏气等合理即可) 不可燃(或不助燃) 不能,镁不仅能和氧气反应还能和氮气反应,这样会导致水面上升超过的
五氧化二磷 红磷量不足(或装置漏气等合理即可) 不可燃(或不助燃) 不能,镁不仅能和氧气反应还能和氮气反应,这样会导致水面上升超过的![]() ,不能确定氧气的含量 操作简便、无污染(合理即可)
,不能确定氧气的含量 操作简便、无污染(合理即可)
【解析】
(1)红磷燃烧时的现象是:产生大量白烟,放出热量;
(2)红磷燃烧生成了五氧化二磷,反应的文字表达式为:磷+氧气![]() 五氧化二磷;
五氧化二磷;
(3)实验完毕,若进入集气瓶中水的体积小于总容积的![]() ,导致这一结果的原因可能是:红磷的量不足、装置漏气等.
,导致这一结果的原因可能是:红磷的量不足、装置漏气等.
(4)燃烧后,集气瓶内剩余的气体主要是氮气.由红磷的熄灭,可推测氮气的化学性质是不可燃、不助燃.
(5)已知镁在空气中燃烧不仅会与氧气反应,还会与氮气反应:镁+氮气![]() 氮化镁.根据上述反应,不能用镁代替红磷测定空气成分,理由是镁不仅能和氧气反应还能和氮气反应,这样会导致水面上升超过的
氮化镁.根据上述反应,不能用镁代替红磷测定空气成分,理由是镁不仅能和氧气反应还能和氮气反应,这样会导致水面上升超过的![]() ,不能确定氧气的含量.
,不能确定氧气的含量.
(6)小红同学又提出了新的测定空气中氧气体积含量的方案,如图乙所示,取一团用食盐水浸泡过的,光亮无锈的铁丝绒,放入一支洁净的试管的底部,将试管倒放在一个盛有水的烧杯中.与上面装置相比,该实验操作简便,误差小、不产生污染物等.

 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
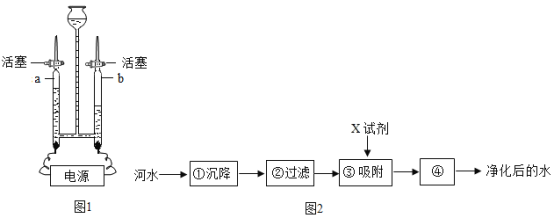
暑假接力赛新疆青少年出版社系列答案【题目】钙是人体中的常量元素,因缺钙而导致骨质疏松、佝偻病等的患者应在医生的指导下服用钙片。某补钙药剂说明书的部分信息如图1所示。现将100g盐酸分成五等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与关系图如图2.请根据有关信息回答问题。
实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
加入盐酸的质量(g) | 20 | 20 | 20 | 20 |
剩余固体的质量(g) | 35 | 30 | a | 20 |
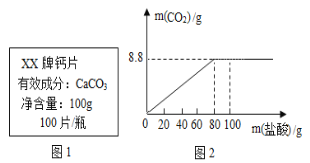
(1)a的数值为_____。
(2)该品牌补钙药剂中CaCO3的质量分数是_____?该盐酸中溶质的质量分数是多少?_____(写出计算过程,计算结果精确至0.1%)
【题目】教材中“分解过氧化氢制氧气的反应中二氧化的化作用”,以及“寻找新的催化剂”研究性实验,引起了化学研究小组同学们的兴趣。
(提出疑问)氧化铁能否作过氧化氢溶液分解的能化剂?如果能,其效果加何?
实验步骤 | 实验现象 |
①分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星的木条,观察现象 | A试管中产生气泡,带火星的木条复燃;B试管中无明显现象 |
②待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次实验,观察现象 | 试管中均产生气泡,带火星的木条均复燃 |
③将实验②中的剩余物小心过滤,并将所得虑渣进行洗涤、干燥、称量,所得固体质量仍为ag | |
④分别量取_____过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象 |
(实验结论)(1)A中产生的气体是_____。
(2)实验2、3证明:氧化铁的质量和_____在反应前后均没有发生变化,可以作过氧化氢分解的催化剂。
(3)实验4的步骤中应填写_____。
(4)写出氧化铁催化过氧化氢分解的化学反应文字表达式_____。
(实验评价)(5)设计实验4的目的是_____。
(6)若实验4观察到D试管中产生气泡的速率更快,由此可以得到的结论是_____。
(表达与交流)(7)小组同学在常温下,将a、b、c三个试管中分别加入等量5%过氧化氢的溶液,在其他条件相同时,各滴2滴5%、10%、20%的硫酸铜溶液。绘制了产生的氧气体积和时间变化的曲线如图,请你回答:
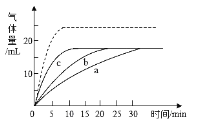
①写出两条规律性结论:_____、_____。
②若实验中所得的曲线如图中虚线所示,请推测其中可能的原因_____。