题目内容
【题目】某实验学校初三兴趣小组利用如下装置(部分固定装置已略去)。制备氮化钙,并探究其化学式
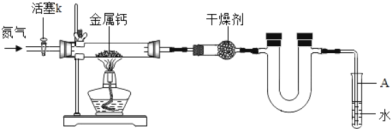
(1)反应过程中末端导管必须插入试管A的水中,目的是_____。
(2)制备氮化钙的操作步骤是:①打开活塞k并通入N2;②点燃酒精灯,进行反应;③反应结束后,_____;④拆除装置,取出产物。
(3)数据记录如下:
空硬玻璃管质量m0/g | 硬玻璃管与钙的质量m1/g | 硬玻璃管与产物的质量m2/g |
114.8 | 120.8 | 122.2 |
①计算得到化学式(实验式)CaxN2,其中x=_____。
②若通入的N2中混有少量O2,如上计算得到的x的值_____ (填写“偏大”、“偏小”、“不变”),判断依据是_____。
【答案】防止空气中的氧气通过末端导管进入实验装置与钙反应 停止加热,继续通氮气至装置冷却 3 偏小 因为钙的总量不变,含有氧化钙的氮化钙总质量增大,钙与氮(不纯)元素的质量比减小,其个数比也变小,所以x值会减小
【解析】
(1)导管插入水中,可以防止防止空气中的氧气通过末端导管进入实验装置与钙反应;
(2)为防止试管内的水倒流,反应结束后,需要继续通入氮气,将末端导管从试管A中撤出水面,再熄灭酒精灯;
(3)①参加反应钙的质量=120.8g﹣114.8g=6g,反应生成氮化钙的质量=122.2g﹣114.8g=7.4g;
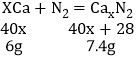
![]() 解得:X=3
解得:X=3
②因为钙的总量不变,含有氧化钙的氮化钙总质量增大,钙与氮(不纯)元素的质量比减小,其个数比也变小,所以x值会减小。若通入的N2中混有少量O2,如上计算得到的x<3。

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目