题目内容
【题目】下列图象不能正确反映其时应变化关系的是( )
A. 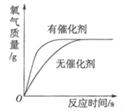 用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气
用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气
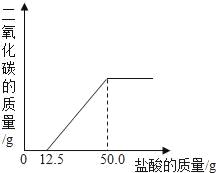
B. 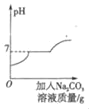 向盐酸和氯化钙的混合溶液中不断滴加碳酸钠溶液
向盐酸和氯化钙的混合溶液中不断滴加碳酸钠溶液
C. 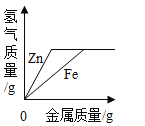 向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉
向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉
D.  向一定质量的氯化铜和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液
向一定质量的氯化铜和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液
【答案】C
【解析】
A、用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气时,利用催化剂时反应速率快一些,但是最终产生氧气的质量相等,图像与事实相符,故A正确;
B、向盐酸和氯化钙的混合溶液中不断滴加碳酸钠溶液时,碳酸钠先和稀盐酸反应,随着稀盐酸的不断反应,溶液pH升高,恰好完全反应时溶液pH=7,继续加入碳酸钠溶液时,再和氯化钙反应生成碳酸钙沉淀和氯化钠,反应过程中溶液pH不变,完全反应后继续加入碳酸钠溶液时,溶液pH升高,图像与事实相符,故B正确;
C、金属与酸反应时氢气来源于酸中的氢元素,因为酸的量相同,金属过量,故生成的氢气应该相等;锌的相对原子质量大于铁,至完全反应,消耗的锌的质量大于铁的质量,图像与事实不相符,故C错误;
D、向一定质量的氯化铜和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液时,氢氧化钠先和稀盐酸反应生成氯化钠和水,后和氯化铜反应生成氢氧化铜沉淀和氯化钠,图像与事实相符,故D正确。故选C。

 轻松暑假总复习系列答案
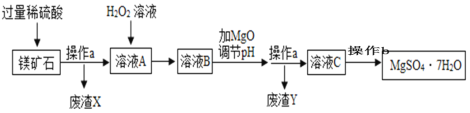
轻松暑假总复习系列答案【题目】图一、图二是某兴趣小组探究金属、酸的化学性质时所做的两组实验。实验结束后,将两组实验试管中的物质分别全部倒入甲、乙两个洁净的烧杯中,据图回答:
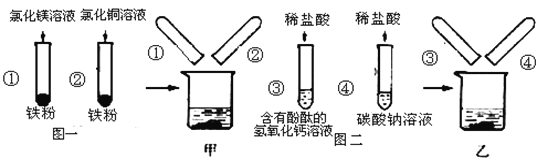
(1)在图一所示的实验中,试管②中发生反应的化学方程式是___________。
(2)将①②两只试管反应后的液体倒入甲烧杯中,发现红色固体物质明显增多。完全反应后,甲烧杯中的溶液中一定含有的阳离子是:_____________。
(3)当观察到③试管中的液体____________时,证明盐酸和氢氧化钙溶液能发生反应。
(4)将③④两只试管反应后的液体倒入乙烧杯中,观察到先有气泡产生,后有白色沉淀出现,溶液呈无色。则试管④反应后的溶液中的溶质共有哪些___________________(写化学式)。
(5)将乙烧杯内的物质进行过滤,对所得无色滤液中溶质成分进行了如下探究:
甲同学认为无色滤液中一定含有NaCl和 HCl,你认为甲同学的观点是否正确_________,其原因是:_________。
乙同学认为无色滤液中一定含有NaCl,一定不含有Na2CO3;
丙同学认为无色滤液中一定含有NaCl,还可能含有另外一种物质,于是做了如下实验:
实验操作 | 实验现象 | 实验结论 |
步骤1:取少量滤液于试管中,向其中滴加足量的__________溶液 | 有白色沉淀生成 | 滤液中的溶质有NaCl 和________ (写化学式) |
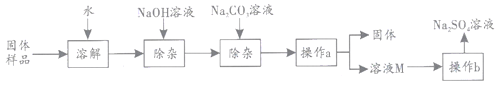
【题目】火锅是我国独创的美食,历史悠久。火锅常用的一种燃料是固体酒精。某化学兴趣小组的同学对“固体酒精”产生了好奇,并对其成分进行了如下探究。请回答下列问题:
(查阅资料)
a.固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成的。
b.氯化钙溶液、氯化钠溶液均呈中性。
(提出问题)
①酒精中是否含有碳元素?
②固体酒精中的氢氧化钠是否变质?
(实验探究)
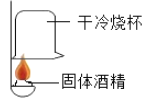
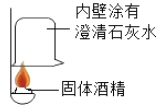
(1)探究乙醇燃烧的生成物:
实验方案 |
|
|
实验现象 | 烧杯内壁出现水雾 | 烧杯内壁_____ |
实验结论 | 说明酒精燃烧生成_____ | 说明酒精燃烧生成二氧化碳 |
从上述实验可得出酒精中一定含有_____元素。
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,请用化学方程式表示该沉淀的形成:_____,由此说明氢氧化钠已变质。
(3)为进一步确定氢氧化钠的变质程度,同学们分组进行探究。
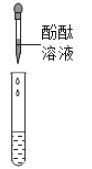
①甲组同学取适量的烧杯上层清液于两支试管中,按如图所示进行实验。
实验方案 |
|
|
实验现象 | 溶液变红 | 产生白色沉淀 |
实验结论 | 清液中有氢氧化钠 | 清液中有_____ |
②乙组同学认为甲组同学的实验不能证明清液中一定有氢氧化钠,理由是_____。于是他们另取烧杯中的上层清液,加足量的氯化钡溶液,充分反应后静置,再取反应后的上层清液,滴加酚酞溶液,酚酞溶液变红。
(反思交流)
(4)乙组同学的实验中加足量的氯化钡溶液的目的是_____。
(实验结论)小组同学经过讨论,一致认为该固体酒精中的氢氧化钠部分变质。
(拓展交流)小组同学经过讨论发现,通过下列方法也可以判断固体酒精中的氢氧化钠是否变质。
(5)取该样品少量于试管中,加入适量的水,振荡,样品全部溶于水,再向其中加入足量的_____,观察到_____,说明样品真的变质了。该实验中相关反应的化学方程式为_____。