题目内容
【题目】CO2是一种廉价的碳资源,其综合利用具有重要意义。
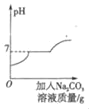
(1)CO2可以被氢氧化钠溶液捕获,反应的化学方程式为______。
(2)工业上以CO2为原料生产尿素[CO(NH2)2]的反应的微观示意图如下:
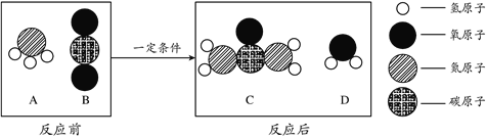
尿素中含有______种元素, 其中氮元素的质量分数的计算式为_____。
【答案】2NaOH+CO2=Na2CO3+H2O 4 ![]()
【解析】
由微观反应示意图可知,氨气和二氧化碳在一定条件下能反应生成尿素和水,方程式为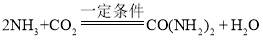 。
。
(1)CO2可以被氢氧化钠溶液捕获,是由于二氧化碳和氢氧化钠反应生成碳酸钠和水,反应的化学方程式为2NaOH+CO2=Na2CO3+H2O;
(2)由尿素[CO(NH2)2]的化学式可知尿素中含有碳、氧、氮、氢四种元素;某元素的质量分数就是该元素质量与组成物质的元素总质量之比,尿素中氮原子的质量分数=![]() =
=![]() 。
。

 一线名师提优试卷系列答案
一线名师提优试卷系列答案【题目】食品包装中常有一小包干燥剂(或双吸剂),课外小组的同学对他们产生了浓厚的兴趣,对生活中的干燥剂进行探究。
查阅资料: (1)包装中常用的干燥剂
种类 | 生石灰 | 硅胶 | 氯化钙 | 蒙脱石 |
特点 | 无毒、无味 | |||
白色块状或粉末,有腐蚀性 | 透明多孔颗粒 | 白色多孔块状、粒状或蜂窝状固体 | 纯天然原料膨润土制作成的小颗粒 | |
(2)实验室常用氢氧化钠和浓硫酸做干燥剂。生活中很少浓硫酸做干燥剂的原因是_____(至少写出一点)。
(进行实验)同学们进行了下列两组探究活动:
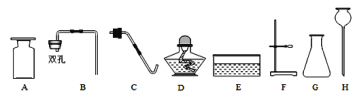
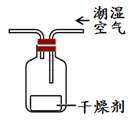
探究I:探究几种干燥剂的干燥效率:分别取下列干燥剂各15g平铺在培养皿底部,按下图所示进行实验,实验结果如下表:
| 序号 | ① | ② | ③ |
干燥剂种类 | 硅胶 | 氯化钙 | 蒙脱石 | |
干燥时间/秒 | 3602 | 1238 | 2810 |
探究II:比较几种干燥剂的干燥能力。按下图所示进行实验,实验结果如下表:
| 序号 | ① | ② | ③ |
干燥剂种类 | 浓硫酸 | 生石灰 | CaCl2 | |
干燥剂质量/g | 10 | 10 | 10 | |
最大增重量/g | 10.3 | 17 | 12 |
(解释与结论)
(1)探究I中,还必须控制的变量是_____。该探究得出的结论是_____。
(2)探究II中,比较几种干燥剂干燥能力强弱的依据是____。
(3)10克氯化钙最大吸水量是12 克,吸水后,形成氯化钙溶液,该溶液中溶质的质量分数为_____。
(反思与评价)探究II的设计存在的问题是_____。