题目内容
【题目】将一小块银白色的金属钠放置在空气中会发生下列变化:
![]()
(提出问题)常温下钠与氧气反应,产物有哪些?
(查阅资料)钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:Na2O+H2O=2NaOH;2Na2O2+2H2O=4NaOH+O2↑
(作出猜想)常温下钠与氧气反应的产物。
猜想1:Na2O; 猜想2:Na2O2; 猜想3:_______。
(实验探究一)
实验操作 | 实验现象 | 实验结论 |
取少量钠的氧化物加入足量蒸馏水 | (_____) | 猜想1正确 |
(继续探究)钠在空气中放置一段时间得到白色固体的成分
(作出猜想)猜想一:Na2CO3猜想二:Na2CO3和NaOH
(实验探究二)
实验操作 | 实验现象 | 实验结论 |
1.取少量白色固体加入足量_____。 | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
2.过滤、取少量滤液加入酚酞。 | (______) |
(实验反思)
(1)类比氧化铁与盐酸的反应,写出氧化钠与盐酸反应的化学方程式_______;
(2)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl=4NaCl+2H2O+X,X的化学式为______;
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2___碱性氧化物(填“是”或“不是”)。
【答案】Na2O和Na2O2 没有气泡生成 氯化钙溶液 酚酞试液变红 Na2O+2HCl=2NaCl+H2O O2 不是
【解析】
[作出猜想]
猜想一是Na2O,猜想二是Na2O2,所以猜想三是氧化钠和过氧化钠的混合物,故填Na2O和Na2O2;
[实验探究]
由于氧化钠与水反应只生成了氢氧化钠,取少量钠的氧化物加入足量蒸馏水,没有气泡生成即可证明猜想一正确,故填没有气泡生成;
[实验探究二] 碳酸钠能与足量的氯化钙反应生成碳酸钙沉淀和氯化钠,且氯化钙、氯化钠溶液都呈中性,氢氧化钠溶液呈碱性,能使酚酞试液变红色,实验操作1故填氯化钙溶液; 操作2实验现象故填酚酞试液变红;
[实验反思]
(1)氧化铁和稀盐酸反应生成氯化铁和水,推测氧化钠和稀盐酸反应生成氯化钠和水,故填Na2O+2HCl=2NaCl+H2O;
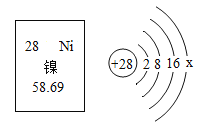
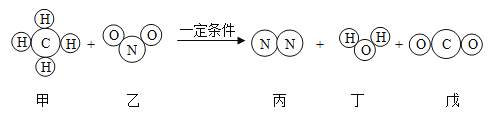
(2)反应反应前原子种类和数目分别是4个钠原子、4个氧原子、4个氢原子、4个氯原子,反应后原子种类和数目分别是4个钠原子、2个氧原子、4个氢原子、4个氯原子和1个X,根据质量守恒定律可知前后差2个氧原子应该有1个X提供,所以X是氧气,故填O2;
(3)由题知能与酸反应只生成盐和水的氧化物称为碱性氧化物,而过氧化钠和盐酸反应除了生成盐类物质氯化钠和水,还生成了氧气,所以过氧化钠不是碱性氧化物,故填不是。

【题目】根据下列实验方案进行实验,不能达到相应实验目的是( )
编 号 | A | B | C | D |
实验装置 |
|
|
|
|
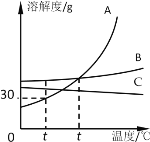
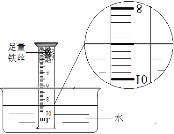
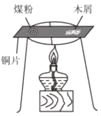
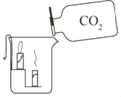
实 验目的 | 探究燃烧条件之一:需要可燃物 | 探究CO2的密度比空气大 | 探究铁钉生锈时O2是否参与反应 | 探究影响物质溶解性的因素之一:溶剂的种类 |
A. A B. B C. C D. D
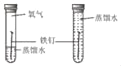
【题目】某研究性小组在一定温度下,用下图所示的实验装置进行一氧化碳还原纯净的氧化铁的实验。
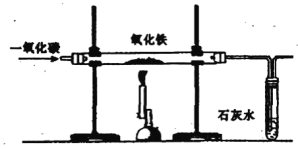
(1)在上述实验装置(已检查气密性)中加好药品、连接好仪器后进行的第一步操作是____________。
(2)实验开始后,右侧试管中发生反应的化学方程式为_______________________。
(3)从环保角度看,实验装置该如何改进?________________________________。
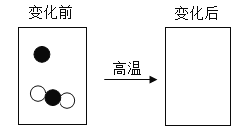
(4)实验中观察到玻璃管内固体由红棕色全部变为黑色。现对产物黑色粉末A的成分进行如下探究:
(查阅资料)①一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁粉,三种物质均为黑色;②铁的氧化物均不和硫酸铜发生反应。
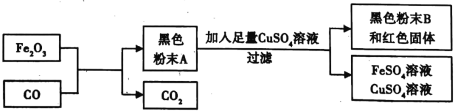
(提出向题)黑色粉末A可能是什么呢?
(进行猜想)(1)小明认为黑色粉末A全部是铁粉。但小华认为小明的猜想是错误的,理由是______。
(2)小华提出了猜想①和猜想②,请结合所学知识补充余下的一个猜想。
猜想①:黑色粉末A由铁粉和四氧化三铁(Fe3O4)组成;
猜想②:黑色粉末A由铁粉和氧化亚铁(FeO)组成:
猜想③:_______
(查阅资料)①铁的氧化物都能与稀盐酸或稀硫酸反应②四氧化三铁、铁粉能被磁铁吸引;
(实验探究)
方案 | 实验操作 | 可能的现象 | 结论 |
① | 取适量黑色粉末A用磁铁吸引 | 黑色粉末全部被吸引 | 猜想①正确 |
② | 取适量黑色粉末A用磁铁吸引 | 黑色粉末部分被吸引 | 猜想②正确 |
③ | ________ | ______ | 猜想③正确 |
(反思评价)(1)小娟认为在方案①②中,方案________的结论正确。(填数字符号)
(2)请你在表格中填写好证明你的猜想③的实验操作和现象。
(得出结论)在高温下,一氧化碳和氧化铁反应可生成铁,氧化亚铁,四氧化三铁。