题目内容
【题目】根据下列实验方案进行实验,不能达到相应实验目的是( )
编 号 | A | B | C | D |
实验装置 |
|
|
|
|
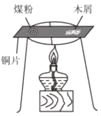
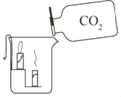
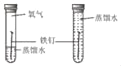
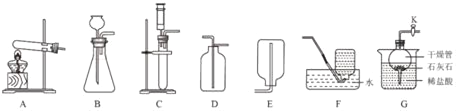
实 验目的 | 探究燃烧条件之一:需要可燃物 | 探究CO2的密度比空气大 | 探究铁钉生锈时O2是否参与反应 | 探究影响物质溶解性的因素之一:溶剂的种类 |
A. A B. B C. C D. D
【答案】A
【解析】
A、煤粉、木屑都是可燃物,不能探究燃烧条件:需要可燃物,故A错误;
B、下层的蜡烛先熄灭,上层的蜡烛后熄灭,说明了CO2的密度比空气大,故B正确;
C、左边试管中的铁钉能与氧气、水充分接触,右边试管中的铁钉只能与水接触,一段时间后,左边试管中的铁钉生锈,右边试管中的铁钉不生锈,能探究铁钉生锈时O2是否参与反应,故C正确;
D、图中实验,溶质相同,溶剂的种类不同,能探究影响物质溶解性的因素,故D正确。故选A。

 阅读快车系列答案
阅读快车系列答案【题目】将一小块银白色的金属钠放置在空气中会发生下列变化:
![]()
(提出问题)常温下钠与氧气反应,产物有哪些?
(查阅资料)钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:Na2O+H2O=2NaOH;2Na2O2+2H2O=4NaOH+O2↑
(作出猜想)常温下钠与氧气反应的产物。
猜想1:Na2O; 猜想2:Na2O2; 猜想3:_______。
(实验探究一)
实验操作 | 实验现象 | 实验结论 |
取少量钠的氧化物加入足量蒸馏水 | (_____) | 猜想1正确 |
(继续探究)钠在空气中放置一段时间得到白色固体的成分
(作出猜想)猜想一:Na2CO3猜想二:Na2CO3和NaOH
(实验探究二)
实验操作 | 实验现象 | 实验结论 |
1.取少量白色固体加入足量_____。 | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
2.过滤、取少量滤液加入酚酞。 | (______) |
(实验反思)
(1)类比氧化铁与盐酸的反应,写出氧化钠与盐酸反应的化学方程式_______;
(2)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl=4NaCl+2H2O+X,X的化学式为______;
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2___碱性氧化物(填“是”或“不是”)。
【题目】第三组同学进行“影响可燃物燃烧剧烈程度的因素”的探究
按下表进行燃烧实验,记录反应的现象。
实验编号 | 可燃物 | 集气瓶中气体 | 反应现象 |
① | 细铁丝 | 氧气 | 剧烈燃烧、大量放热________ |
② | 细铁丝 | 空气 | 不燃烧 |
③ | 铁粉 | 空气 | 剧烈燃烧、迸发出大量火星 |
(1)实验①的现象还有__________________;该反应的化学方程式为____________。
(2)欲证明可燃物燃烧剧烈程度与氧气的浓度有关,须进行的对比实验为__________(填序号);通过实验②和③对比,可得出的结论是___________。
(3)相同条件下,氧气浓度还会影响可燃物是否完全燃烧,举例说明_________。
【题目】以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究并帮忙填写空格(包括表中的空格)。
(提出问题)化学反应前后各物质的质量总和是否相等?
(猜想与假设)猜想1:不相等;猜想2:相等。
(实验探究)甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲组 | 乙组 | |
实验方案(反应后略) |
|
|
实验现象 | 有气泡产生,天平指针向右偏转 | 铁钉表面有红色物质析出,溶液颜色发生改变,天平指针没有偏转 |
结论 | 猜想1正确反应的化学方程式:_____ | 猜想2正确 |
(反思评价)究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体溢出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在_____中进行。
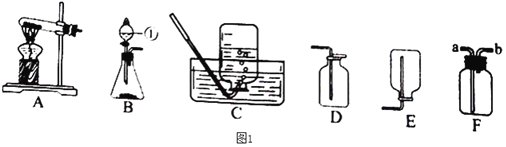
(优化装置)同学们对甲组左盘中的反应装置进行了如下三种改进,你认为最佳装置是_____ (填序号),从另外两种装置中任选一种指出其不足_____。
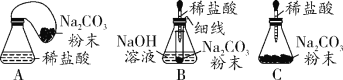
(得出结论)同学们利用改进后的最佳装置进行再次探究,均得出猜想2正确。进一步分析发现,反应体系中器材参加化学反应和未参加反应的物质的质量在反应前后保持不变,最终得出结论:_______的各物质的质量总和等于反应后生成的各物质的质量总和。
(解释应用)解释:化学反应前后,原子的种类、数目、质量均不变,所以质量守恒。
应用:某固体物质受热会发生分解反应,生成氧化铜、水和二氧化碳三种物质,则该固体物质一定由_____种元素组成。