题目内容
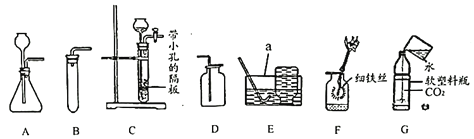
【题目】某化学兴趣小组在实验室用氯酸钾和二氧化锰混合加热制取氧气时,发现制得的气体有刺激性气味,于是在老师的指导下对该气体成分进行探究。
(提出问题)氯酸钾和二氧化锰混合加热后产生的气体成分是什么?
(查阅资料)![]() 氯酸钾和二氧化锰混合加热产生的气体只以单质形式存在;
氯酸钾和二氧化锰混合加热产生的气体只以单质形式存在;
![]() 氯气
氯气![]() 是有刺激性气味的气体,能溶于水,能使湿润的淀粉碘化钾试纸变蓝。
是有刺激性气味的气体,能溶于水,能使湿润的淀粉碘化钾试纸变蓝。
(猜想与假设)猜想一:该气体是![]() ;猜想二:该气体是
;猜想二:该气体是![]() ;猜想三:该气体是______
;猜想三:该气体是______
(实验探究)
序号 | 实验操作 | 实验现象 | 结论 |
| 小丽用排水法收集A、B两瓶气体,将带火星木条伸入A中;湿润的淀粉碘化钾试纸伸入B中。 | A中带火星木条复燃,B中淀粉碘化钾试纸不变色。 | 猜想 ______ 成立 |
| 小岚用向上排空气法收集C、D两瓶气体,将带火星木条伸入C中,湿润的淀粉碘化钾试纸伸入D中。 | C中带火星木条复燃,D中淀粉碘化钾试纸 ______ | 猜想三成立 |
(反思与评价)小涛认为小丽的结论不正确,原因是______
(拓展应用)![]() 氯酸钾和二氧化锰混合加热,当不再产生气体时的剩余固体是______、______
氯酸钾和二氧化锰混合加热,当不再产生气体时的剩余固体是______、______![]() 填化学式
填化学式![]() 。
。
![]() 二氧化锰不仅能作催化剂还可以做反应物。请完成该反应的化学方程式:
二氧化锰不仅能作催化剂还可以做反应物。请完成该反应的化学方程式:![]()
![]()
![]() ______
______![]() 。
。
【答案】O2和Cl2 一 变蓝 用排水法收集时,氯气溶于水了,不能判断反应产物中是否有氯气 KCl ![]() 2H2O
2H2O
【解析】
猜想与假设:氯酸钾与二氧化锰混合加热后产生的气体成分可能为O2、Cl2或O2和Cl2的混合物;
实验探究:1、用排水集气法收集A、B两瓶气体,将带火星木条伸入A中,木条复燃,说明用氧气产生;将湿润的淀粉碘化钾试纸伸入B中,B中淀粉碘化钾试纸不变色,说明无氯气,故猜想一成立;2、用向上排空气法收集C、D两瓶气体,将带火星木条伸入C中,木条复燃,说明用氧气产生;将湿润的淀粉碘化钾试纸伸入D中, D中淀粉碘化钾试纸变蓝,说明有氯气产生,故猜想三成立。
反思与评价:氯气(Cl2)是有剌激性气味的气体,能溶于水,小涛认为小丽的结论不正确,原因是:用排水法收集时,氯气溶于水了,不能判断反应产物中是否有氯气;
拓展应用:
1、化学反应前后元素的种类不变,氯酸钾和二氧化锰混合加热产生少量固体,为氯化钾,二氧化锰为催化剂,反应前后质量不变,故当不再产生气体时的剩余固体是混合物,含有氯化钾和二氧化锰,化学式为:KCl、![]() ;
;
2、反应物中锰、氧、氢、氯原子个数分别为1、2、4、4,反应后的生成物中锰、氧、氢、氯原子个数分别为1、0、0、4,根据质量守恒定律,反应前后原子种类、数目不变,则方框中含有4个氢原子和2个氧原子,则每个分子由2个氢原子和1个氧原子构成,则物质的化学式为H2O,横线处应填2H2O。

【题目】珍珠粉是一种补钙剂,某兴趣小组对珍珠粉的主要成分及其含量展开了一系列探究。
(实验探究一)(1)珍珠粉的主要成分是什么?
实验 | 实验操作 | 实验现象 |
步骤一 | 取少量样品于试管中,加入足量_____ | 产生无色气泡 |
步骤二 | 将步骤一产生的气体通入澄清石灰水 | 产生白色沉淀 |
②写出步骤二中发生反应的化学方程式_____。
(实验结论)珍珠粉的主要成分为碳酸钙。
(实验探究二)测定珍珠粉中碳酸钙的质量分数。(杂质不与稀盐酸反应)
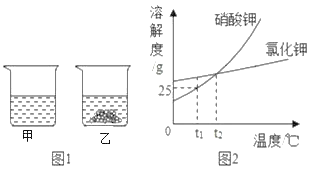
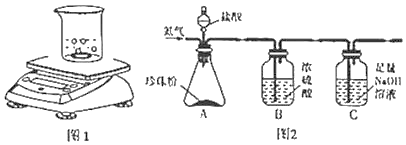
(方案一)(2)该兴趣小组的同学利用如图1所示装置进行实验探究,称得烧杯的质量为40.03g。称得珍珠粉样品的质量为12g。加入足量的稀盐酸质量为200g,完全反应后,电子天平的示数为247.63g。请你计算珍珠粉中碳酸钙的质量分数______。(写出计算步骤:计算结果保留到0.1%)
(方案二)(3)该兴趣小组的同学认为图2所示装置也可测定珍珠粉中碳酸钙的质量分数,需要测定的数据有样品的质量和_____的质量。如果没有装置B,会使测得的碳酸钙的质量分数_____。(填“偏大”、“偏小”或者“不变“)
【题目】某课外活动小组的同学为测定假黄金(铜锌合金)的组成,称取25克假黄金样品置于烧杯中,用稀硫酸80克分4次加入,实验数据记录如下.求:
实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
稀硫酸的质量/克 | 20 | 20 | 20 | 20 |
残留金属的质量/克 | 21.75 | 18.5 | 15.25 | 15.25 |
(1)假黄金与稀硫酸恰好完全反应是___________次;
(2)25克假黄金样品中锌的质量为______________克;
(3)四次实验产生气体的总质量是多少_________?(写出详细计算过程)