题目内容
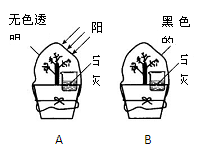
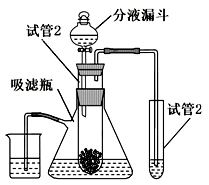
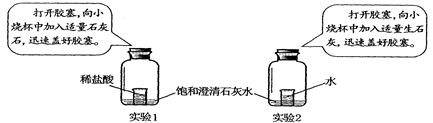
九(1)班的几位同学根据下列各实验装置图,设计和讨论了许多问题,请你也参与他们的探究过程:
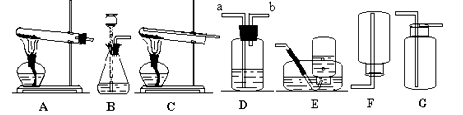
⑴万星同学说:“选择‘A与E’或 组合成装置可制取氧气。”请你写出其中一种实验室制氧气的化学方程式 。
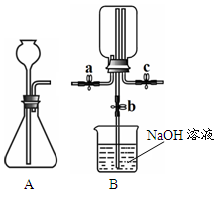
⑵古力同学说:“用锌和盐酸制取的氢气中常含有少量HCl气体,用D装置可除去HCl气体,D中应盛放 溶液”。
文涛同学说:“D装置还可以收集和储备氧气,若要用水将装置中已收集的氧气排出,水应从(填“a”或“b”) 端通入。”
⑶闵杰同学说:“上次用C装置做氢气还原氧化铜实验,实验结束时发现红色的铜又变成黑色,我现在才明白其中的原因是 。”
⑷周琦同学说:“选B作制取气体的发生装置,应满足的条件是 ,
。”
⑸在实验中我们要遵守实验规则。如使用A装置时应注意的事项有(只写一条)
。
⑹李亮的家庭化学实验室只有如下物品:a.试管;b.导管与橡皮塞;c.煤气和煤气炉;
d.托盘天平;e.筷子;f.铁钉;g.铜丝;h.食盐; i.食醋;j.石灰水;k.硫酸铜;m.水。
请你与李亮一起完成如下实验:
①若要探究牙膏中是否含有碳酸钙,需要用到其中的物品是(填序号) ;
②若要利用上述物品证明铁的活动性比铜强,则设计的实验方案中的实验现象是
,反应的化学方程式为______ ______;
③请利用上述李亮家庭化学实验室的物品设计实验,探究加速食盐溶于水的某一方法的有效性。选择的方法是 ;实验方案是 。

⑴万星同学说:“选择‘A与E’或 组合成装置可制取氧气。”请你写出其中一种实验室制氧气的化学方程式 。
⑵古力同学说:“用锌和盐酸制取的氢气中常含有少量HCl气体,用D装置可除去HCl气体,D中应盛放 溶液”。
文涛同学说:“D装置还可以收集和储备氧气,若要用水将装置中已收集的氧气排出,水应从(填“a”或“b”) 端通入。”
⑶闵杰同学说:“上次用C装置做氢气还原氧化铜实验,实验结束时发现红色的铜又变成黑色,我现在才明白其中的原因是 。”
⑷周琦同学说:“选B作制取气体的发生装置,应满足的条件是 ,
。”
⑸在实验中我们要遵守实验规则。如使用A装置时应注意的事项有(只写一条)
。
⑹李亮的家庭化学实验室只有如下物品:a.试管;b.导管与橡皮塞;c.煤气和煤气炉;
d.托盘天平;e.筷子;f.铁钉;g.铜丝;h.食盐; i.食醋;j.石灰水;k.硫酸铜;m.水。
请你与李亮一起完成如下实验:
①若要探究牙膏中是否含有碳酸钙,需要用到其中的物品是(填序号) ;
②若要利用上述物品证明铁的活动性比铜强,则设计的实验方案中的实验现象是
,反应的化学方程式为______ ______;
③请利用上述李亮家庭化学实验室的物品设计实验,探究加速食盐溶于水的某一方法的有效性。选择的方法是 ;实验方案是 。
(1) A与G(或“B与G”) 2H2O2
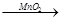 2H2O+O2↑
2H2O+O2↑(2) NaOH(或氢氧化钠)(其它可溶性碱也可给分); a
(3) 未继续通入氢气至铜冷却 (4) 固体和液体(或液体与液体)反应,且反应不需要加热
(5) 试管口应略向下倾斜(或试管内药品应平辅或应用酒精灯外焰加热或对试管加热时应先预热)
(其它合理答案也可给分)
(6)、①a b i j ②铁钉表面有红色物质析出;Fe+CuSO4→Cu+FeSO4
③加热、搅拌、振荡等,但设计的实验必须在此条件下能完成。举例答案:方法:加热(1分)
方案:取适量相同质量的食盐,分别同时放入有相同水量的试管中,将其中一个加热,比较观察食盐溶解情况。(一定要强调控制的变量,强调食盐与水的量各1分)
本题考查的是常用气体的发生装置和收集装置与选取方法,书写化学方程式。
(1)根据氧气的实验室制法及其发生装置和收集装置的选择条件判断,双氧水在二氧化锰的催化作用下生成氧气和水,发生装置属于固体和液体不加热反应生成气体,氧气密度比空气大,可以采用向上排空气法收集。
(2)氢气属于中性气体,氯化氢属于酸性气体,故可用碱液来除,如氢氧化钠,可与之反应生成氯化钠和水;因为水的密度大于氧气,故若要用水将装置D中已收集的氧气排出,水应从a端通入。
(3)实验结束后,要继续通入氢气一段时间,等冷却下来再撤导管;否则,空气中的氧气就会进入试管和灼热的铜重新氧化生成氧化铜。
(4)根据发生装置的选择条件可知,B装置为固体和液体(或液体与液体)反应,且反应不需要加热。
(5)这是对试管加热的注意事项的一个考查,可根据加热装置的注意事项解答,如试管口要略向下倾斜等。
(6)①碳酸钙能和醋酸反应生成二氧化碳,检验二氧化碳的方法是通入澄清石灰水,石灰水变浑浊,故选a b i j。
②排在前面的金属能把后面的金属从它的盐溶液中置换出来,故可用铁和硫酸铜反应来证明铁的活动性比铜强,故可见铁钉表面有红色物质析出,即Fe+CuSO4═Cu+FeSO4。
③加速溶解的方法很多,在日常生活中常见的方法有加热、搅拌等;如取适量相同质量的食盐,分别同时放入有相同水量的试管中,将其中一个加热,比较观察食盐溶解情况。
(1)根据氧气的实验室制法及其发生装置和收集装置的选择条件判断,双氧水在二氧化锰的催化作用下生成氧气和水,发生装置属于固体和液体不加热反应生成气体,氧气密度比空气大,可以采用向上排空气法收集。
(2)氢气属于中性气体,氯化氢属于酸性气体,故可用碱液来除,如氢氧化钠,可与之反应生成氯化钠和水;因为水的密度大于氧气,故若要用水将装置D中已收集的氧气排出,水应从a端通入。
(3)实验结束后,要继续通入氢气一段时间,等冷却下来再撤导管;否则,空气中的氧气就会进入试管和灼热的铜重新氧化生成氧化铜。
(4)根据发生装置的选择条件可知,B装置为固体和液体(或液体与液体)反应,且反应不需要加热。
(5)这是对试管加热的注意事项的一个考查,可根据加热装置的注意事项解答,如试管口要略向下倾斜等。
(6)①碳酸钙能和醋酸反应生成二氧化碳,检验二氧化碳的方法是通入澄清石灰水,石灰水变浑浊,故选a b i j。
②排在前面的金属能把后面的金属从它的盐溶液中置换出来,故可用铁和硫酸铜反应来证明铁的活动性比铜强,故可见铁钉表面有红色物质析出,即Fe+CuSO4═Cu+FeSO4。
③加速溶解的方法很多,在日常生活中常见的方法有加热、搅拌等;如取适量相同质量的食盐,分别同时放入有相同水量的试管中,将其中一个加热,比较观察食盐溶解情况。

练习册系列答案
相关题目