��Ŀ����
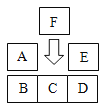
����Ŀ��άC����Ƭ��һ�ֳ����IJ���ά����C�ı���Ʒ��ijƷ��άC����Ƭ�����³ơ���Ʒ��������Ҫ�ɷ���ͼ1��ʾ��

��1�����й���ά����C��˵����ȷ����_____������ĸ����
a��ά����C��C��H��O����Ԫ�����
b��ά����C����Է�������Ϊ176g
c��ά����C��6��̼ԭ�ӡ�8����ԭ�Ӻ�6����ԭ�ӹ���
d��ά����C��C��H��OԪ�ص�������Ϊ9��1��12
��2���Ķ���Ʒ��Ӫ���ɷֱ���ÿ100gάC����Ƭ����5750mg��1mg��10��3g������֪��Ʒ�����ɷֲ�����Ԫ�أ���Ʒ��̼�����Ƶ���������Ϊ_____��
��3��άC����Ƭˮ��Һ����ԵIJⶨ������ƷһƬͶ������ˮ�У������ݲ�������Ӧԭ��Ϊ��H3C6H5O2+3NaHCO3��Na3C6H5O2+3CO2��+3_____���ѧʽ���������ٲ�����������Һ�����ԡ�
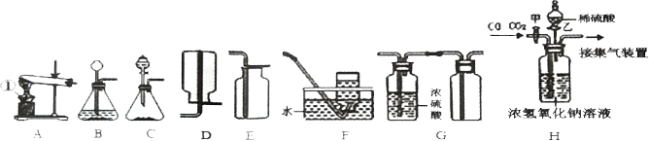
��4��άC����Ƭ��̼���������������IJⶨ���������ʵ����Ʒ����������ƷһƬͶ������ˮ�У������ٲ������������ƿ��ƿ���������ʵ���������װ����ͼ2��ʾ��
������������
��Ʒ | ��Ӧǰ | ��Ӧ�� | ||
��ƿ | ����ˮ | άC����Ƭ | ��ƿ��ƿ���������� | |
����/g | 71.75 | 50.00 | 4.00 | 125.53 |
�ٸ����������ݼ��㱾Ʒ��̼�����Ƶ���������____________��д��������̣������ȷ��0.1%����
��ʵ��ⶨ������⣨2�����������������ƫ������ԭ����_____��
���𰸡�ad 21% H2O 10.5% װ�����в���Ķ�����̼
��������
![]()
��1��a��ά����C��C��H��O����Ԫ����ɡ���a��ȷ��
b��ά����C����Է�������Ϊ176����λ��1����g����b����ȷ��
c��ά����C��ά����C���ӹ��ɣ�������ԭ��ֱ�ӹ��ɡ���C����ȷ��
d��ά����C��C��H��OԪ�ص�������Ϊ![]() ����d��ȷ����ѡad��
����d��ȷ����ѡad��
��2��ÿ100gάC����Ƭ����5750mg��1mg��10��3g����5.75g����֪��Ʒ�����ɷֲ�����Ԫ�أ���Ʒ��̼�����Ƶ���������Ϊ![]()
��3�����������غ㶨�ɿ�֪����Ӧǰ��̼ԭ��9������ԭ��11������ԭ��11������ԭ��3������Ӧ��������ԭ��3����̼ԭ��9������ԭ��5������ԭ��8����ȱ����ԭ��6������ԭ��3�����ֲ���3�������У����Զ�Ӧ����![]() ��
��
��4���ٸ��������غ㶨�ɿɵã����ɵĶ�����̼������Ϊ
![]()
�豾Ʒ��̼�����Ƶ���������Ϊx
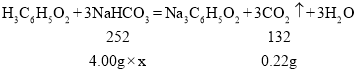
![]()
![]()
��ʵ��ⶨ������⣨2�����������������ƫ������ԭ����װ�����в���Ķ�����̼��

 ͬ����ϰǿ����չϵ�д�
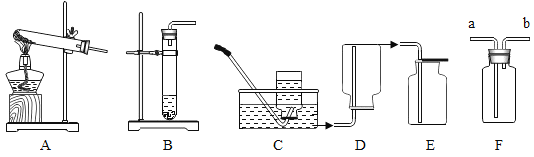
ͬ����ϰǿ����չϵ�д�����Ŀ���ڻ�ѧʵ���ҿ����գ���ʦ�ó���ƿ�ޱ�ǩ���Լ����ֱ��ǹ����Һ�壬��ȡ�����Լ����Թ��л�ϣ���������һ����ɫ���塣ͬѧ�ǶԴ�����չ����һϵ��̽����
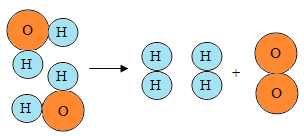
��1������Ʋ�������Ƕ�����̼����֤����ʵ�鷽�����£�
���� | ʵ�鲽�� | ��������� |
�����������CO2 | __________ | __________ |
����������Ļ�ѧ����ʽ������__________��
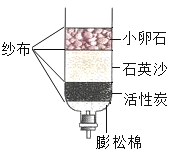
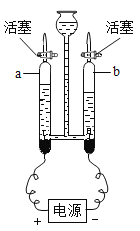
��2��������ȡ�����壬���õķ���װ�ÿ�ѡȡ��ͼ�е�____������ţ���������ͼ��Fװ���ռ������壬����Ӧ��____ ��ѡ�a����b�����˵��롣
����Ŀ��Ϊ��֤�������ƵĻ�ѧ����ij��ȤС��ͬѧ������ͼ��ʾʵ�顣�����ʵ��ش�����
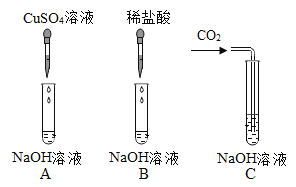
��1��A�Թ��й۲쵽��ʵ��������_____��
��2����ͬѧ�۲쵽B�Թ�������������Ȼ����B�Թ��м����μ�1��2����ɫ��̪��Һ������Һ��Ϊ��ɫ��������_____����������������������֤������������Һ��ϡ���ᷢ���˷�Ӧ��
��3��Ϊ����֤C�Թ�����̼�������ɣ���ͬѧ��Ƶ�ʵ�鷽�������ʾ�����������д������
���������ϣ�̼������Һ�Լ���
���� | ʵ�鲽�� | ʵ������ | ��Ӧ�Ļ�ѧ����ʽ |
һ | ��ȡ������Ӧ����Һ����һ֧�Թ��� �ڼ��������ϡ���� | _____ | _____ |
�� | ��_____ ��_____ | _____ | _____ |