题目内容
【题目】根据下列装置,结合所学化学知识回答问题:
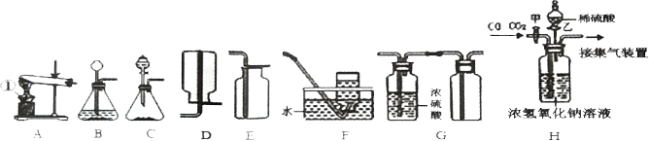
(1)写出标号①仪器的名称:_____。
(2)用装置A制取氧气的化学方程式为_____,为了获得较纯净的氧气应选择的收集装置是_____(在A一F中选)。
(3)实验室用过氧化氢溶液和二氧化锰粉末混合制取氧气,可选用B或C做气体发生装置,与B相比较,C装置的优点是_____。
(4)若用G装置收集一瓶干燥的某气体,则该气体不可能是_____(填字母代号)。
A O2 B H2 C NH3 D HCl
(5)工业上常需分离CO、CO2的混合气体。某同学采用装置H也能达到分离该混合气体的目的,操作步骤如下:
①关闭活塞乙,打开活塞甲,通入混合气体,可收集到_____气体;
②然后,_____(填操作),又可收集到另一种气体。
【答案】酒精灯 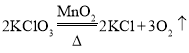 F 能够控制反应速率 BC CO 关闭活塞甲,打开活塞乙
F 能够控制反应速率 BC CO 关闭活塞甲,打开活塞乙
【解析】
(1)根据图中信息可知,仪器①是酒精灯;
(2)装置A是固体加热发生装置,但试管口处没有棉花团,所以是利用加热氯酸钾和二氧化锰制取氧气,化学方程式为: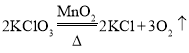 ,氧气不溶于水且密度比空气大,所以可以采用排水法或者向上排空气法收集氧气,为了获得较纯净的氧气,应采用排水法,选F;
,氧气不溶于水且密度比空气大,所以可以采用排水法或者向上排空气法收集氧气,为了获得较纯净的氧气,应采用排水法,选F;
(3)C装置加入液体时使用的是分液漏斗,分液漏斗可以控制加入液体的速率,从而控制整个反应的速率,而长颈漏斗不能,故C装置的优点是能够控制反应速率;
(4)若用G装置收集一瓶干燥的某气体,则该气体不能和浓硫酸反应,且密度应比空气密度大
A、氧气不能和浓硫酸反应,密度比空气大,不符合题意;
B、氢气密度比空气小,符合题意;
C、氨气能和浓硫酸反应,符合题意;
D、氯化氢不能和浓硫酸反应,密度比空气大,不符合题意。故选BC。
(5)①关闭活塞乙,打开活塞甲,通入混合气体,二氧化碳和氢氧化钠反应生成碳酸钠和水,一氧化碳不反应,所以可收集到一氧化碳;
②然后关闭活塞甲,打开活塞乙,加入稀硫酸,稀硫酸和碳酸钠反应生成二氧化碳、硫酸钠和水,又可收集到CO2。

【题目】维C泡腾片是一种常见的补充维生素C的保健品。某品牌维C泡腾片(以下称“本品”)的主要成分如图1所示。

(1)下列关于维生素C的说法正确的是_____(填字母)。
a.维生素C由C、H、O三种元素组成
b.维生素C的相对分子质量为176g
c.维生素C由6个碳原子、8个氢原子和6个氧原子构成
d.维生素C中C、H、O元素的质量比为9:1:12
(2)阅读本品的营养成分表:每100g维C泡腾片含钠5750mg(1mg=10﹣3g)。已知本品其他成分不含钠元素,则本品中碳酸氢钠的质量分数为_____。
(3)维C泡腾片水溶液酸碱性的测定:将本品一片投入蒸馏水中,有气泡产生,反应原理为:H3C6H5O2+3NaHCO3=Na3C6H5O2+3CO2↑+3_____(填化学式)。待不再产生气体后,测得溶液呈酸性。
(4)维C泡腾片中碳酸氢钠质量分数的测定:称量相关实验用品质量,将本品一片投入蒸馏水中,待不再产生气体后,称量锥形瓶及瓶内所有物质的总质量。装置如图2所示。
相关数据如表:
物品 | 反应前 | 反应后 | ||
锥形瓶 | 蒸馏水 | 维C泡腾片 | 锥形瓶及瓶内所有物质 | |
质量/g | 71.75 | 50.00 | 4.00 | 125.53 |
①根据以上数据计算本品中碳酸氢钠的质量分数____________(写出计算过程,结果精确到0.1%)。
②实验测定结果与题(2)计算结果相比有明显偏差,其可能原因是_____。