题目内容
【题目】化学兴趣小组探究某双吸剂(成分是铁粉)是否变质,进行了如下实验,取27.2g样品加入稀硫酸溶液,实验测得相关数据如所示:某双吸剂样品27.2g+稀硫酸277 g![]()
![]() 得到溶液的质量为304 g
得到溶液的质量为304 g
请回答下列问题(双吸剂不含其他杂质):
(1)分析实验数据,完全反应生成氢气的质量为多少g。
(2)通过计算分析该双吸剂是否变质(写出计算步骤)。
(3)缺铁会贫血。假设反应后溶质只有一种,经测定反应后的溶液的溶质质量分数为20%,则反应后的溶液经过处理用于补铁(假设铁没有散失) ,可以补充铁质量为多少g。
【答案】(1)0.2(2)该双吸剂已经变质(3)22.4 g
【解析】
(1)根据质量守恒定律,反应前后总质量相等,生成的氢气质量:![]() ;
;
(2)根据化学方程式![]() ,利用铁完全反应时产生氢气的质量可求出样品中铁的质量,如果铁的质量比样品质量小,说明样品已经变质,如果铁的质量与样品质量一样,则样品没有变质。
,利用铁完全反应时产生氢气的质量可求出样品中铁的质量,如果铁的质量比样品质量小,说明样品已经变质,如果铁的质量与样品质量一样,则样品没有变质。
解:设生成0.2 g氢气需要参加反应的铁的质量为x
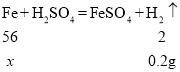
![]()
x=5.6g
样品质量27.2 g大于5.6 g。该双吸剂已经变质。
答:该双吸剂已经变质;
(3)完全反应后的溶液的溶质只有FeSO4,溶质FeSO4质量: ![]() ,60.8g FeSO4中铁元素质量:
,60.8g FeSO4中铁元素质量:![]() ;
;
故答案为:0.2;该双吸剂已经变质;22.4 g。

 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案【题目】下列实验方案不能达到相应实验目的的是( )
|
|
|
|
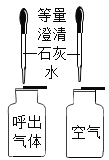
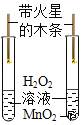
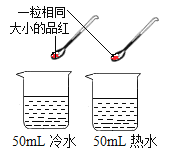
A证明蜡烛中含有氢元素 | B证明呼出气体比呼入空气中的CO2含量多 | C证明二氧化锰是过氧化氢分解的催化剂 | D证明温度越高,分子运动速率越快 |
A.AB.BC.CD.D
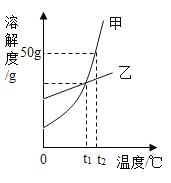
【题目】维C泡腾片是一种常见的补充维生素C的保健品。某品牌维C泡腾片(以下称“本品”)的主要成分如图1所示。

(1)下列关于维生素C的说法正确的是_____(填字母)。
a.维生素C由C、H、O三种元素组成
b.维生素C的相对分子质量为176g
c.维生素C由6个碳原子、8个氢原子和6个氧原子构成
d.维生素C中C、H、O元素的质量比为9:1:12
(2)阅读本品的营养成分表:每100g维C泡腾片含钠5750mg(1mg=10﹣3g)。已知本品其他成分不含钠元素,则本品中碳酸氢钠的质量分数为_____。
(3)维C泡腾片水溶液酸碱性的测定:将本品一片投入蒸馏水中,有气泡产生,反应原理为:H3C6H5O2+3NaHCO3=Na3C6H5O2+3CO2↑+3_____(填化学式)。待不再产生气体后,测得溶液呈酸性。
(4)维C泡腾片中碳酸氢钠质量分数的测定:称量相关实验用品质量,将本品一片投入蒸馏水中,待不再产生气体后,称量锥形瓶及瓶内所有物质的总质量。装置如图2所示。
相关数据如表:
物品 | 反应前 | 反应后 | ||
锥形瓶 | 蒸馏水 | 维C泡腾片 | 锥形瓶及瓶内所有物质 | |
质量/g | 71.75 | 50.00 | 4.00 | 125.53 |
①根据以上数据计算本品中碳酸氢钠的质量分数____________(写出计算过程,结果精确到0.1%)。
②实验测定结果与题(2)计算结果相比有明显偏差,其可能原因是_____。