题目内容
【题目】某工厂产生的废渣(主要含![]() 、
、![]() ,还有一定量的
,还有一定量的![]() )可用于制备硫酸亚铁晶体,其工艺流程如下:(查阅资料:
)可用于制备硫酸亚铁晶体,其工艺流程如下:(查阅资料:![]() 不溶于水和酸。)
不溶于水和酸。)
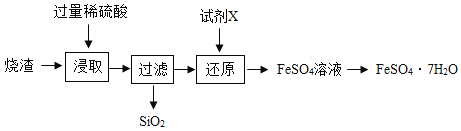
(1)“浸取”步骤中![]() 与硫酸反应生成硫酸亚铁和水,写出反应的化学方程式为_______;
与硫酸反应生成硫酸亚铁和水,写出反应的化学方程式为_______;
(2)“浸取”步骤中常常将废渣粉碎、搅拌或提高硫酸浓度,目的都是____________;
(3)“还原”步骤的目的是将![]() 转化为
转化为![]() ,“试剂”可选用下列两种物质:
,“试剂”可选用下列两种物质:
①若试剂X是![]() 转化原理:
转化原理:![]() ,则Y的化学式为________;
,则Y的化学式为________;
②若试剂X是![]() 转化原理:
转化原理:![]() ,测得还原后的溶液pH增大,其原因是:
,测得还原后的溶液pH增大,其原因是:
A ![]() 和过量的硫酸反应 B ________________________
和过量的硫酸反应 B ________________________
【答案】![]() 加快反应速率
加快反应速率 ![]()
![]() 的酸性没有
的酸性没有![]() 强(合理给分)
强(合理给分)
【解析】
(1)氧化亚铁和硫酸反应生成硫酸亚铁和水,化学方程式为:FeO+H2SO4=FeSO4+H2O;
(2)“浸取”步聚中常常将废渣粉碎、搅拌或提高硫酸浓度,目的都是:加快反应速率;
(3)由反应的化学方程式可知,反应前后硫原子都是4个,铁原子都是2个,反应后的氧原子是16个,反应前应该是16个,其中2个包含在2Y中,反应后氢原子是4个,反应前应该是4个,都包含在2Y中,所以Y是H2O;
若试剂X是Fe转化原理; Fe+Fe2 (SO4)3=3FeSO4,测得还原后的溶液pH增大,其原因是:
A Fe 和过量的硫酸反应
B 硫酸亚铁的酸性没有硫酸铁强。
故答案为:(1)FeO+H2SO4=FeSO4+H2O;
(2)加快反应速率;
(3)H2O;硫酸亚铁的酸性没有硫酸铁强。

 每课必练系列答案
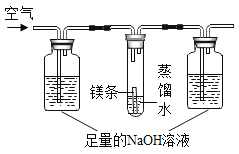
每课必练系列答案【题目】某研究小组发现,原本银白色有金属光泽的镁,漏置在空气中一段时间后,表面覆盖一层灰黑色物质。该小组同学进行了如下探究。
探究一:灰黑色物质成分
(猜想与假设)
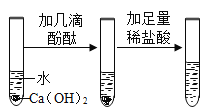
小明说:灰黑色可能含有MgO、Mg(OH)2、Mg2(OH)2CO3。小芳说:不可能是MgO,原因是______________________________。
(进行试验)
实验编号 | 实验操作 | 实验现象 |
① | 取灰黑色粉末于试管中,滴加稀盐酸 | 有气泡产生 |
② | 将产生的气体通入澄清的石灰水中 | 石灰水变混浊 |
(得出结论)
得出结论灰黑色物质中一定含有________________;写出实验②中发生的化学方程式________________。
探究二:产生灰黑色物质的原因
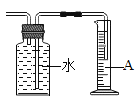
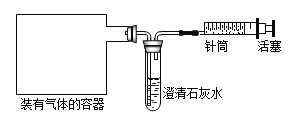
在猜想产生灰黑色物质的原因时,小华认为,镁条变黑与N2无关,其理由是____________。为进一步探究产生灰黑色物质的原因,设计如图实验,其中NaOH溶液的作用是_________________,经过一段时间,试管中镁条基本无变化。
(得出结论)镁表面的黑色物质是美与空气中O2、CO2、H2O共同作用的结果。
(实验拓展)①用镁条实验前一般要进行的操作是_______________。 ②保存镁条的方法是_______________。