题目内容
【题目】在托盘天平的两盘上各放一只质量相同的烧杯,在两只烧杯里分别加入100g溶质质量分数为73%的稀盐酸,天平呈平衡状态。然后向左、右两盘的烧杯中分别加入下列各物质,充分反应后,天平指针不会发生偏转的是(不考虑稀盐酸的挥发)( )
A.10g碳酸钙和10g碳酸钠B.8.4g碳酸氢钠和8.4g碳酸镁
C.1.8g铝粉和1.8g锌粉D.4.6g氧化铁粉末和4.8g镁条
【答案】BD
【解析】
加入的盐酸质量相等,需要判断两端加入一定量物质后增加质量是否相等,增加质量相等时天平能仍然保持平衡,不相等时天平发生偏转。
A、100g溶质质量分数为73%的稀盐酸中氯化氢的质量为![]() ,
,
设与碳酸钙反应的稀盐酸的质量为x1
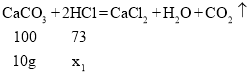
![]()
![]()
设与碳酸钠反应的稀盐酸的质量为y1
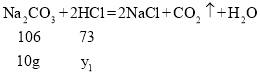
![]()
![]()
加入的碳酸钙恰好完全反应,生成4.4g二氧化碳;加入的碳酸钠不足,没有将稀盐酸完全反应,所以根据参与反应的碳酸钠的质量可求出生成了4.15g二氧化碳,碳酸钙与稀盐酸反应生成的二氧化碳更多,天平不能保持平衡,故A不正确;
B、设与碳酸氢钠反应的稀盐酸的质量为x2
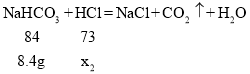
![]()
![]()
设与碳酸氢钠反应的稀盐酸的质量为y2
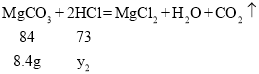
![]()
![]()
加入的碳酸氢钠不足,没有把稀盐酸完全反应,参与反应的碳酸氢钠的质量,可求出生成的二氧化碳的质量为4.4g;加入的碳酸镁恰好与稀盐酸完全反应,可求出生成的二氧化碳的质量为4.4g。所以天平能保持平衡,故B正确;
C、设与铝粉反应的稀盐酸的质量为x3
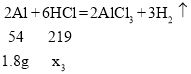
![]()
![]()
设与锌粉反应的稀盐酸的质量为y3
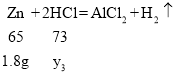
![]()
![]()
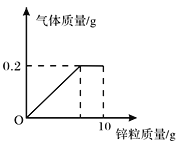
加入的铝粉恰好与稀盐酸完全反应,可求得生成的氢气得到质量为0.2g;加入的锌粉不足,没有把稀盐酸完全反应,所以依据参与反应的锌粉的质量,可求出生成的氢气的质量为0.055g。所以天平不能保持平衡,故C不正确;
D、氧化铁粉末与稀盐酸反应生成氯化铁和水,没有气体生成,根据质量守恒定律可知,反应完之后,氧化铁反应的那边的天平增加重量4.6g;
设与镁条反应的稀盐酸的质量为y4
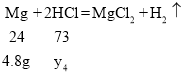
![]()
![]()
加入的镁条过量,依据参与反应的稀盐酸的质量,可求出生成的氢气的质量为0.2g。烧杯质量增加了4.8g-0.2g=4.6g,所以天平平衡,故D正确。故选BD。

【题目】为测定镁和硫酸镁固体混合物中镁元素的质量分数,先称取混合物10g,放入一干净的烧杯中,然后取一定溶质质量分数的稀硫酸100g,平均分五次加入其中,充分振荡,实验所得数据如下表:
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 | 20 |
生成气体的总质量/g | 0.12 | x | 0.36 | 0.4 | y |
(1)上表中x=_______、y=_______.
(2)固体混合物中镁元素的质量分数为__________.
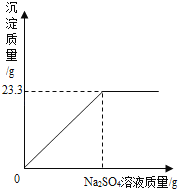
【题目】石灰石样品的主要成分是碳酸钙(已知其它杂质不与盐酸反应)。某兴趣小组的同学将50g盐酸分5次加入到10g该石灰石样品中,得到如下部分数据和图象:
次数 | 第一次 | 第二次 | 第三次 |
加入盐酸的质量/g | 10 | 10 | 10 |
剩余固体的质量/g | 8 | 6 | 4 |
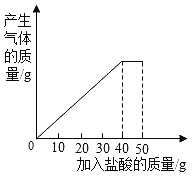
请计算:
(1)10g石灰石样品中所含杂质的质量为_______g.
(2)求所加盐酸的溶质质量分数._______
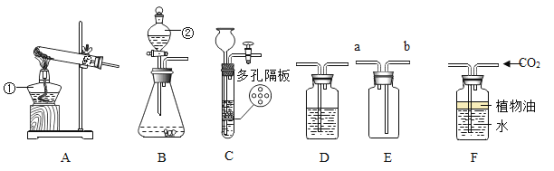
【题目】(实验一)下图是实验室制取气体的一些装置,据图回答问题。
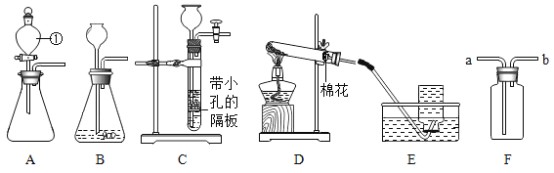
(1)写出制定仪器的名称①____
(2)实验室用C装置制取氢气,反应的化学方程式:_____,装置的优点:____.如果用装置F收集氢气,气体从____(填“a”或“b”)端管口通入。
(实验二)某化学兴趣小组对“酸和碱中和反应”进行探究,进行如下实验:取5ml氢氧化钠溶液于烧杯中,滴加酚酞试剂,溶液变红,接着滴加稀盐酸,用玻璃棒搅拌,溶液褪为无色,有关的化学方程式:_____
(1)(提出猜想)小明同学认为最终的溶液的溶质有二种可能:_____,②是氯化钠
(2)(设计实验)同学们设计了如下方案并进行实验:
实验操作 | 实验现象 | 实验结论 |
取少量溶液于试管中,向其中滴加_____ | ______ | 猜想①正确 |