题目内容
【题目】常用仪器的使用、常见气体的制取是初中化学实验的基础内容,请根据下列实验装置回答问题。
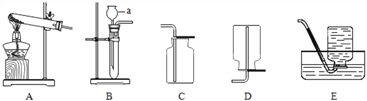
(1)写出仪器名称:a_________________。
(2)实验室用A装置制取氧气的化学方程式:____________________________。
(3)实验室收集二氧化碳的装置是__________,用化学方程式表示检验二氧化碳的原理__________________。
(4)二氧化氯(ClO2)可用作消毒剂。常温下,ClO2是一种橙黄色、有刺激性气味的气体,11℃以下为红色液体,易溶于水,见光易分解,可用固体氯酸钠(NaClO3)与浓盐酸反应制取,反应的化学方程式为:2NaClO3 + 4HCl═2ClO2↑+ Cl2↑+ 2X + 2NaCl。
①制取气体的发生装置是____________(填装置序号)。
②上述反应中X的化学式为_________。
【答案】 长颈漏斗 2KClO3 ![]() 2KCl + 3O2↑ C CO2 + Ca(OH)2 = CaCO3↓+ H2O B H2O
2KCl + 3O2↑ C CO2 + Ca(OH)2 = CaCO3↓+ H2O B H2O
【解析】(1)根据常见仪器解答;(2)根据氯酸钾在二氧化锰的催化并加热的条件下分解生成氯化钾和氧气解答;(3)根据二氧化碳能溶于水且密度比空气大解答;根据二氧化碳与氢氧化钙溶液反应生成碳酸钙沉淀和水解答;(4)①根据反应物的状态和反应条件分析解答;②根据质量守恒定律分析解答。(1)仪器a的名称为长颈漏斗;(2)氯酸钾在二氧化锰的催化并加热的条件下分解生成氯化钾和氧气,反应的化学方程式为2KClO3 ![]() 2KCl+3O2↑;(3)二氧化碳能溶于水且密度比空气大,用向上排空气法收集,收集装置为C;检验二氧化碳的原理是二氧化碳与氢氧化钙溶液反应生成碳酸钙沉淀和水,反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O;(4)①固体氯酸钠(NaClO3)与浓盐酸在常温下反应即可制取ClO2,故应选择固液混合常温型发生装置B;②反应前后Na、Cl、O、H原子个数比为2、6、6、4,2、6、4、0。反应前后氧原子相差2个,氢原子相差4个,又X前的计量数为2,故X中含2个氢原子和1个氧原子,因此X的化学式为H2O。
2KCl+3O2↑;(3)二氧化碳能溶于水且密度比空气大,用向上排空气法收集,收集装置为C;检验二氧化碳的原理是二氧化碳与氢氧化钙溶液反应生成碳酸钙沉淀和水,反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O;(4)①固体氯酸钠(NaClO3)与浓盐酸在常温下反应即可制取ClO2,故应选择固液混合常温型发生装置B;②反应前后Na、Cl、O、H原子个数比为2、6、6、4,2、6、4、0。反应前后氧原子相差2个,氢原子相差4个,又X前的计量数为2,故X中含2个氢原子和1个氧原子,因此X的化学式为H2O。

 新思维寒假作业系列答案
新思维寒假作业系列答案【题目】实验室进行粗盐的提纯
(1)涉及的操作有:①过滤②溶解③蒸发结晶。正确的顺序是_________。(填序号)
(2)用托盘天平称量所需粗盐的质量,托盘天平调节平衡后,接下来的操作顺序
是_________(填序号)①在右盘中添加砝码,需要用游码时移动到相应刻度、②在托盘上分别放质量相等的纸、③在左盘中添加粗盐
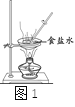
(3)下图1中玻璃棒的作用是搅拌,_________。当_________时停止加热。
(4)配制溶液①用质量分数为5%的氯化钠溶液配制70g质量分数为3%的氯化钠溶液,需要水的质量是_____g。量取水的体积(水的密度为1g/mL),请在图2标出所需水的体积示数_________。②从表中找出稀释的过程需要用到的数据(20℃)是_______g/cm3。

20℃氯化钠溶液的密度
浓度% | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
密度g/cm3 | 1.005 | 1.013 | 1.02 | 1.027 | 1.034 | 1.041 | 1.043 |
【题目】科学方法对化学学习起着事半功倍的作用。
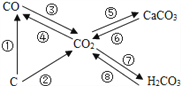
(1)分类归纳是研究化学物质的重要方法。如图是某同学整理的碳及其化合物的知识网络图,转化③常用于冶炼工业,工业上用赤铁矿炼铁时,反应的化学方程式为_____________,二氧化碳使紫色石蕊试液变红涉及的反应是如图所示转化中_______(填序号)。
(2)微观粒子模型化是研究化学变化的重要方法。
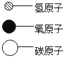
①下图是钠与氯气反应生成氯化钠的示意图。该图说明在化学反应过程中一定发生变化的是__________(填字母)。
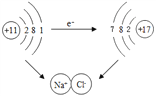
A.原子核 B.原子核最外层电子数 C.原子的电子层数
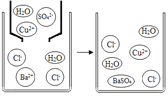
②下图是硫酸铜溶液与氯化钡溶液反应示意图。从粒子角度分析该化学反应能发生的原因是___________________________。
③A、B、C、D表示4种物质,下图是部分物质的微观示意图。A和B在一定条件下反应生成C和D。
物质 | B | C | D |
|
微观示意图 |
|
|
|
若一定质量的A和4.8g B恰好完全反应,可生成4.4gC和2.7gD,则A的化学式是____。
④我国科学家创造性地构建了“单中心铁催化剂”,在甲烷高效转化研究中获得重大突破。甲烷转化反应的微观示意图如下:
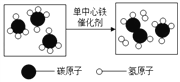
图示所表示的反应的化学方程式为___________________。
(3)控制变量、设计对比实验是实验探究的重要方法。
下图实验是大小形状相同的Mg、Zn、Fe、Cu四种金属同时投入到盐酸中发生的现象,金属周围的黑点表示生成的气体。下列结论不正确的是__(填字母)。
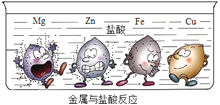
A.铜不能发生置换反应
B.四种金属中金属活动性最强的是Mg
C.等质量的锌和铁分别与足量的盐酸反应生成气体质量:Zn比Fe多
【题目】某同学把干燥、纯净的氯酸钾和二氧化锰的混合物31.5g装入大试管中,加热制取氧气,并在不同时刻测定试管内剩余固体物质的质量(如下表):
反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
剩余固体质量/g | 28.9 | 26.3 | 23.7 | 21.9 | 21.9 |
分析表中数据,完成下列问题:
(1)完全反应后,生成氧气的质量为___________g;
(2)把剩余固体加入足量的水溶解过滤得到滤液55g(二氧化锰难溶于水),计算滤液中溶质的质量分数是多少?(精确到0.1%) ___________