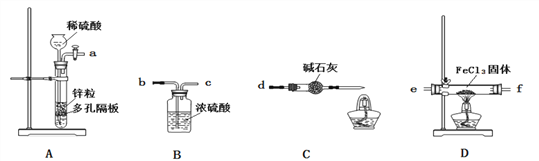
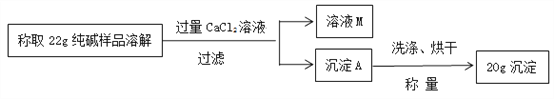
题目内容
【题目】科学方法对化学学习起着事半功倍的作用。
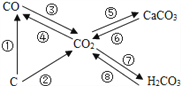
(1)分类归纳是研究化学物质的重要方法。如图是某同学整理的碳及其化合物的知识网络图,转化③常用于冶炼工业,工业上用赤铁矿炼铁时,反应的化学方程式为_____________,二氧化碳使紫色石蕊试液变红涉及的反应是如图所示转化中_______(填序号)。
(2)微观粒子模型化是研究化学变化的重要方法。
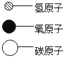
①下图是钠与氯气反应生成氯化钠的示意图。该图说明在化学反应过程中一定发生变化的是__________(填字母)。
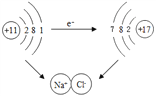
A.原子核 B.原子核最外层电子数 C.原子的电子层数
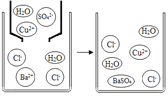
②下图是硫酸铜溶液与氯化钡溶液反应示意图。从粒子角度分析该化学反应能发生的原因是___________________________。
③A、B、C、D表示4种物质,下图是部分物质的微观示意图。A和B在一定条件下反应生成C和D。
物质 | B | C | D |
|
微观示意图 |
|
|
|
若一定质量的A和4.8g B恰好完全反应,可生成4.4gC和2.7gD,则A的化学式是____。
④我国科学家创造性地构建了“单中心铁催化剂”,在甲烷高效转化研究中获得重大突破。甲烷转化反应的微观示意图如下:
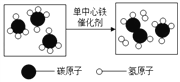
图示所表示的反应的化学方程式为___________________。
(3)控制变量、设计对比实验是实验探究的重要方法。
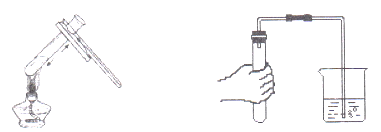
下图实验是大小形状相同的Mg、Zn、Fe、Cu四种金属同时投入到盐酸中发生的现象,金属周围的黑点表示生成的气体。下列结论不正确的是__(填字母)。
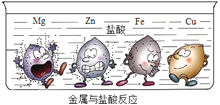
A.铜不能发生置换反应
B.四种金属中金属活动性最强的是Mg
C.等质量的锌和铁分别与足量的盐酸反应生成气体质量:Zn比Fe多
【答案】 Fe2O3+3CO![]() 2Fe+3CO2 ⑦ B 钡离子和硫酸根离子结合生成难溶于水的硫酸钡沉淀 C2H6O(或C2H5OH) 2CH4
2Fe+3CO2 ⑦ B 钡离子和硫酸根离子结合生成难溶于水的硫酸钡沉淀 C2H6O(或C2H5OH) 2CH4 ![]() C2H4+2H2 AC
C2H4+2H2 AC
【解析】(1)根据氧化铁与一氧化碳在高温的条件下反应生成铁和二氧化碳解答;根据二氧化碳与水反应生成碳酸,碳酸显酸性使紫色石蕊溶液变红解答;(2)①根据物质的化学性质与原子的最外层电子数有关进行分析;②根据硫酸铜和氯化钡反应生成硫酸钡沉淀和氯化铜进行分析;③根据反应的微观示意图结合相关数据计算解答;④根据反应的微观示意图分析解答;(3)根据在金属活动性顺序中,只有排在氢前的金属才可以和稀酸溶液反应生成氢气,而且越靠前的金属活动性就越强,和稀酸溶液反应时现象就越剧烈进行分析。(1)氧化铁与一氧化碳在高温的条件下反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO高温2Fe+3CO2;二氧化碳与水反应生成碳酸,碳酸显酸性使紫色石蕊溶液变红,故选⑦;(2)①图甲是钠与氯气反应生成氯化钠的示意图,该图说明在化学反应过程中,原子核不变,电子层数可能变化,原子在发生化学变化时,通过得失电子形成化合物,所以一定发生变化的是B;②硫酸铜和氯化钡反应生成硫酸钡沉淀和氯化铜,所以从粒子角度分析该化学反应能发生的原因是:钡离子和硫酸根离子结合生成难溶于水硫酸钡沉淀;③由图可知,B、C、D分别为氧气、二氧化碳、水。二氧化碳中氧元素的质量=4.4g×![]() =3.2g,二氧化碳中碳元素的质量=4.4g-3.2g=1.2g;水中氧元素的质量=2.7g×
=3.2g,二氧化碳中碳元素的质量=4.4g-3.2g=1.2g;水中氧元素的质量=2.7g×![]() =2.4g,水中氢元素的质量=2.7g-2.4g=0.3g;故A中碳元素的质量为1.2g,氧元素的质量=3.2g+2.4g-4.8g=0.8g,氢元素的质量为0.3g。A中C、H、O的原子个数比为
=2.4g,水中氢元素的质量=2.7g-2.4g=0.3g;故A中碳元素的质量为1.2g,氧元素的质量=3.2g+2.4g-4.8g=0.8g,氢元素的质量为0.3g。A中C、H、O的原子个数比为![]() =2:6:1,那么A的化学式为C2H6O(或C2H5OH);④由图可知,该反应的化学方程式为2CH4
=2:6:1,那么A的化学式为C2H6O(或C2H5OH);④由图可知,该反应的化学方程式为2CH4 ![]() C2H4+2H2;(3)在金属活动性顺序中,只有排在氢前的金属才可以和稀酸溶液反应生成氢气,而且越靠前的金属活动性就越强,和稀酸溶液反应时现象就越剧烈,所以A、铜不能与酸发生反应,铜可以将硝酸银中的银置换出来,所以不能说铜不会发生置换反应,错误;B、镁表面的气泡产生最剧烈,所以四种金属中金属活动性最强的是Mg,正确;C、每65份质量的锌会生成2份质量的氢气,每56份质量的铁会生成2份质量的氢气,所以等质量的锌和铁分别与足量的盐酸反应生成气体质量:Zn比Fe少,错误。故选AC。
C2H4+2H2;(3)在金属活动性顺序中,只有排在氢前的金属才可以和稀酸溶液反应生成氢气,而且越靠前的金属活动性就越强,和稀酸溶液反应时现象就越剧烈,所以A、铜不能与酸发生反应,铜可以将硝酸银中的银置换出来,所以不能说铜不会发生置换反应,错误;B、镁表面的气泡产生最剧烈,所以四种金属中金属活动性最强的是Mg,正确;C、每65份质量的锌会生成2份质量的氢气,每56份质量的铁会生成2份质量的氢气,所以等质量的锌和铁分别与足量的盐酸反应生成气体质量:Zn比Fe少,错误。故选AC。

 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案【题目】将一小块银白色的金属钠放置在空气中会发生下列变化:
![]()
[查阅资料]
I.钠的氧化物有氧化钠(Na2O)和过氧化钠(Na2O2),都能与水反应,反应化学方程式如下:Na2O + H2O = 2NaOH 2Na2O2 + 2H2O = 4NaOH + O2↑
II. CaCl2溶液呈中性;碳酸钠溶液能与CaCl2溶液或Ca(OH)2溶液发生复分解反应;
碳酸钠溶液与盐酸反应方程式有:Na2CO3 +HCl=NaHCO3 +NaCl、Na2CO3+2HCl=2NaCl+H2O+CO2↑
(1)为检验常温下钠与氧气反应的产物,是Na2O还是Na2O2,完成实验方案:
选取试剂 | 实验现象 | 实验结论 |
__________________ | __________________________ | 产物为Na2O |
⑵ 钠在空气中放置一段时间得到白色固体的成分
猜想1:Na2CO3 猜想2:NaOH 猜想3:Na2CO3和NaOH
[实验过程]
[实验1] 取少量白色固体加水配成溶液,再滴入几滴稀盐酸,无气泡产生。
化学小组认为:据此现象,还不能得出猜想2成立。理由是________________。
[实验2] 化学小组进行如下实验
实验操作 | 实验现象 | 实验结论 |
①取少量白色固体配成溶液,加入足量_______; | _______ | 猜想3成立 |
②过滤,取少量滤液滴入________________。 | _________ |