题目内容
【题目】某化学小组进行了如下实验探究。
(提出问题)溶液中复分解反应的实质是什么?
(查阅资料)
①电导率传感器用于测量溶液的导电性强弱,能反应离子浓度大小。
②相同温度下同种溶液电导率越大,离子浓度越大。
(实验一)测定四种溶液的电导率
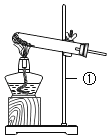
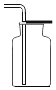
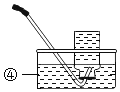
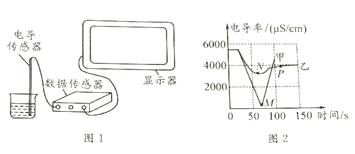
室温下,分别取20mL下列液体于烧杯中,插入电导率传感器如图1,测得数据如下表:(烧杯中的物质静置于空气中备用)
物质 | ①蒸馏水 | ②稀硫酸 | ③氢氧化钠溶液 | ④硫酸钡悬浊液 |
电导率/(μS/cm) | 3 | 5923 | 6316 | 3 |
(1)测出物质①④与物质②③的电导率数据差异巨大的原因是_________。
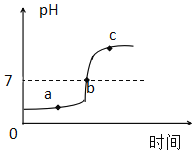
(实验二)测定氢氧化钡与稀硫酸反应过程中的电导率
室温下,将上述烧杯中的氢氧化钡溶液倒出10mL于另一烧杯中,向其中滴加2-3滴无色酚酞试液,插入电导率传感器,然后滴加稀硫酸,测得溶液的电导率变化如图2中甲曲线所示。
(2)写出氢氧化钡与硫酸反应的化学方程式:___________。
(3)M点时电导率几乎为零的原因是__________.
(4)通过对甲曲线的分析,下列说法错误的是_______(填字母序号)。
A M点前曲线下滑的过程中,H+和OH-结合成H2O,Ba2+和SO42-结合成BaSO4
B M点后溶液电导率逐渐增大,是由于BaSO4进一步解离出Ba2+和SO42-
(实验三)测定氢氧化钡与硫酸钠反应过程中的电导率
室温下,将实验二中稀硫酸改为硫酸钠溶液,重复上述实验,测得溶液的电导率变化如图2中乙曲线所示。
(5)写出硫酸钠与氢氧化钡反应的化学方程式____________。
(6)对比两曲线的最低点,N点比M点明显高的原因是_____,P点时溶液中大量含有的离子是_____(填离子符号)。
(结论)
(7)通过比较分析,结合已学知识可知,溶液中复分解反应的实质是参与反应的离子结合生成了沉淀、气体或水,导致其浓度_______(填“增大”或“减小”)。
(拓展与反思)
(8)向一定量饱和澄清石灰水中持续通入过量的二氧化碳气体,溶液先变浑浊后浑浊逐渐消失。推测此过程的溶液中Ca2+的浓度变化情况是____________。
(9)实验二中刚开始时,氢氧化钡溶液的电导率小于实验一中测得的6316μS/cm,原因可能是________。
(10)若用实验一中物质②与③反应来测定电导率随时间的变化情况,你推测溶液的变化曲线可能是_____________(填“甲”或“乙”)。
【答案】物质②③溶液中离子浓度远远大于物质①④ ![]() 生成物水和硫酸钡,硫酸钡为难溶物,在M点时,两溶液恰好反应完全,此时溶液中离子浓度最低,故M处电导率几乎为零 B
生成物水和硫酸钡,硫酸钡为难溶物,在M点时,两溶液恰好反应完全,此时溶液中离子浓度最低,故M处电导率几乎为零 B ![]() 硫酸钠与氢氧化钡反应的产物除了难溶物BaSO4以外,还有易溶于水的NaOH,所以N点处离子浓度明显大于N点 Na+、OH-、SO42- 减小 Ca2+浓度先变小后变大 Ba(OH)2溶液中的离子浓度小于实验1中的NaOH溶液离子浓度 乙。
硫酸钠与氢氧化钡反应的产物除了难溶物BaSO4以外,还有易溶于水的NaOH,所以N点处离子浓度明显大于N点 Na+、OH-、SO42- 减小 Ca2+浓度先变小后变大 Ba(OH)2溶液中的离子浓度小于实验1中的NaOH溶液离子浓度 乙。
【解析】
(1)根据题中给出的信息可知,测出物质①④与物质②③的电导率数据差异巨大的原因是:物质②③溶液中离子浓度远远大于物质①④;
(2)Ba(OH)2与H2SO4反应生成硫酸钡沉淀和水,反应的化学方程式为![]() ;
;
(3)M点时二者恰好完全反应,生成物水和硫酸钡,硫酸钡为难溶物,离子浓度几乎为零,相同温度下同种溶液电导率越大,离子浓度越大,所以M点时电导率几乎为零;
(4)A M点前曲线下滑的过程中,H+和OH-结合成H2O,Ba2+和SO42-结合成BaSO4,正确;
B M点后溶液电导率逐渐增大,是因为恰好完全反应后,离子浓度几乎为零,继续加入稀硫酸,离子浓度增大,电导率增大,故选项说法错误;
故选:B。
(5)氢氧化钡和硫酸钠反应生成硫酸钡沉淀和氢氧化钠,反应方程式为:![]() ;
;
(6)硫酸钠与氢氧化钡反应的产物除了难溶物BaSO4以外,还有易溶于水的NaOH,所以N点处离子浓度明显大于M点;
N点时,溶液中含有氢氧化钠和过量的硫酸钠,故含有的离子是Na+、OH-、SO42-;
(7)溶液中复分解反应的实质是参与反应的离子,结合生成了沉淀、气体或水,导致其浓度减小。
(8)向一定量饱和澄清石灰水中持续通入过量的CO2气体,溶液先变浑浊,是因为生成了难溶的碳酸钙,继续通入二氧化碳又变澄清,是因为碳酸钙和二氧化碳、水生成了可溶的碳酸氢钙,溶液变浑浊过程中钙离子浓度逐渐减小,浑浊逐渐消失的过程中钙离子的浓度逐渐增大。
(9)实验二中刚开始时,氢氧化钡溶液的电导率小于实验一中测得的6316μS/cm,原因可能是Ba(OH)2溶液中的离子浓度小于实验1中的NaOH溶液离子浓度;
(10)稀硫酸和氢氧化钠反应生成硫酸钠和水,硫酸钠易溶于水,反应后离子浓度会降低,但不会变化特别大,不至于几乎为零,所以会与曲线乙走势接近。

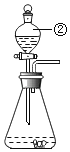
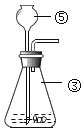
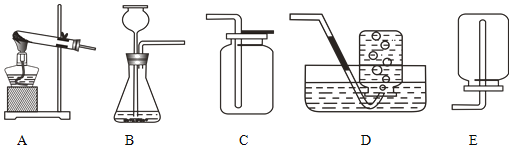
【题目】如图是实验室制取气体常用的发生装置和收集装置图示,请结合实验装置图示,完成下列问题:
气体发生装置 | 气体收集装置 | ||||
|
|
|
|
|
|
A | B | C | D | E | F |
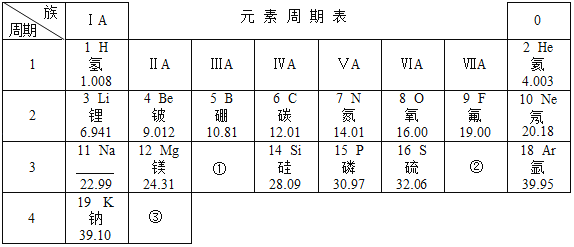
(1)写出仪器标号的仪器名称:①_____②_____③_____④_____
(2)若用装置A制取氧气,反应的化学符号表达式_____。
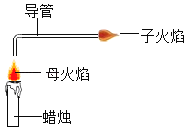
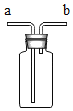
(3)如用绿色制取氧气的方法,不仅能节约药品,还可以控制反应进行,应选用的气体发生装置是_____(填编号),写出该反应的化学符号表达式_____,如用E来收集O2,氧气应从_____(填“a或b”)端通入,如何验满_____。
(4)制取气体,装入药品前,先检查气密性,检查装置C气密性的方法是_____,说明装置不漏气。
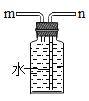
(5)常温下,硫化氢(H2S)是一种有臭鸡蛋气味的气体,能溶于水,密度大于空气,实验室通常在常温下用硫化亚铁固体(FeS)和稀硫酸反应制得,同时生成硫酸亚铁,则从上面装置中最好选择的发生装置是_____。选择的收集装置是_____,理由是_____
(6)常温下用块状电石(CaC2)与水反应制取难溶于水的乙炔气体(C2H2)并生成了氢氧化钙,请你认真写出该反应的化学符号表达式_____。实验室制取并收集纯净的乙炔,该反应非常剧烈,必须控制反应的速度。你选择的发生装置是_____和收集装置是_____如果用如图所示装置收集乙炔,气体应从_____(填“m”或“n”)端管口通入。