题目内容
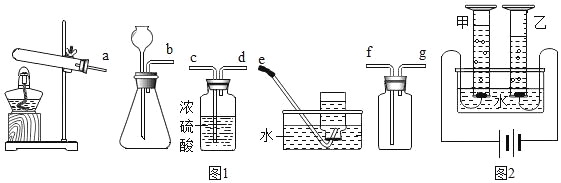
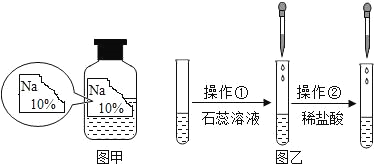
【题目】(一)某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题。
(猜想与假设)
其溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种。
(资料查阅)上述四种物质的相关信息如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下某稀溶液的pH | 7 | 13 | 11 | 9 |
(探究过程)
如图乙所示,在操作①后可确定溶质不是NaCl,则实验过程和实验现象应是_____;在进行操作②时有无色无味得到气体产生,由此又可排除假设物质中的_____。
(探究结论)
你认为该溶液中的溶质可能是上述假设物质中的_____,你的判断依据是_____。
(探究反思)
(1)若上述探究结论是正确的,操作②产生的气体应是_____(写化学式),实验室检验该气体的实验操作及现象是_____。
(2)另有同学猜想其中的溶质还可能是Na2SO4,但又没有Na2SO4的上述表列信息。
请你根据以上实验操作的相关现象,判断该溶液中的溶质是否是Na2SO4,并叙述理由:_____。
(二)兴趣小组的同学在做镁条和盐酸反应实验时发现,试管外壁很烫,试管口出现白雾。白雾是什么呢?
Ⅰ.同学们作出猜想
猜想一:是小水滴。因为盐酸溶液中的水受热会汽化上升,在试管口_____(填物态变化名称)成小水滴。
猜想二:是盐酸小液滴。因为浓盐酸具有_____性,可能实验中使用的盐酸浓度过高,试管口就会形成盐酸小液滴。
同学们将干燥的蓝色石蕊试纸放在内有正在反应的镁条和盐酸的试管口,试纸变红,证明猜想二是合理的。
Ⅱ.小柯提出质疑
为什么刚才打开盛放实验所用盐酸的试剂瓶,瓶口没有白雾,却在反应过程中出现白雾?
小柯联系反应时试管外壁很烫,于是猜想:白雾的形成可能与温度有关。
他用试管取少量盐酸,将干燥的蓝色石蕊试纸放在试管口,试纸不变红;然后_____(填操作),试纸变红。
得出结论:这种盐酸浓度并不高,是因_____促使盐酸形成白雾。
【答案】滴加石蕊试液会变成蓝色 氢氧化钠 碳酸钠 碳酸氢钠饱和溶液的质量分数不可能达到10%,而碳酸钠溶液可以 CO2 将生成的气体通入澄清石灰水中,溶液变浑浊,说明该气体是二氧化碳 若滴加石蕊试液变成蓝色,则不含有硫酸钠 液化 挥发 加热试管,将干燥的蓝色石蕊试纸放在试管口 放热
【解析】
(一)[探究观察]NaCl、NaOH、Na2CO3和NaHCO3中只有氯化钠溶液为中性,而其余的溶液都显碱性,若溶质不是NaCl,则石蕊试液会变成蓝色;在进行操作②滴加稀盐酸时有无色无味的气体产生,说明不是氢氧化钠,因为氢氧化钠和盐酸反应无明显现象,故填:滴另石蕊试液会变成蓝色 氢氧化钠;
[探究结论]根据计算可以知道在20℃时饱和碳酸氢钠的质量分数为:![]() ×100%=8.8%,而题目中标注的溶液的质量分数为10%,所以这瓶试剂不可能的是碳酸氢钠溶液,而碳酸钠溶液的溶质质量分数可以等于10%,因此可能是碳酸钠,故填:碳酸钠 碳酸氢钠饱和溶液的质量分数不可能达到10%,而碳酸钠溶液可以;
×100%=8.8%,而题目中标注的溶液的质量分数为10%,所以这瓶试剂不可能的是碳酸氢钠溶液,而碳酸钠溶液的溶质质量分数可以等于10%,因此可能是碳酸钠,故填:碳酸钠 碳酸氢钠饱和溶液的质量分数不可能达到10%,而碳酸钠溶液可以;
[探究反思](1)假设碳酸钠成立,则碳酸钠和盐酸反应会产生二氧化碳,检验二氧化碳可以将气体通入石灰水,石灰水变浑浊,故填:CO2 将生成的气体通入澄清石灰水中,溶液变浑浊,说明该气体是二氧化碳;
(2)硫酸钠溶液为中性溶液,因此若滴加石蕊试液变成蓝色,则说明不含有硫酸钠,故填:若滴加石蕊试液变成蓝色,则不含有硫酸钠;
(二)Ⅰ、猜想一:水受热,由液态转化为气态,在试管口遇冷液化为液态的水,故填:液化;
猜想二:浓盐酸具有挥发性,挥发出来的氯化氢气体与空气中的水蒸气结合成盐酸的小液滴,故填:挥发;
Ⅱ、根据猜想可知,升高温度后,将干燥的蓝色石蕊试纸放在试管口观察是否变红色来检验,故填:加热试管,将干燥的蓝色石蕊试纸放在试管口;
得出结论:这种盐酸浓度并不高,是因放热促使盐酸形成白雾,故填:放热。

 阅读快车系列答案
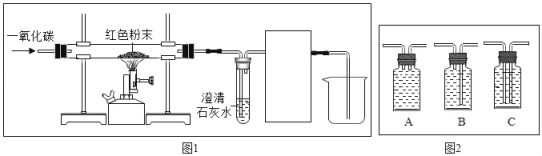
阅读快车系列答案【题目】小明同学欲通过实验证明“二氧化锰是氯酸钾受热分解的催化剂”这一命题.他设计并完成了下表所示的探究实验:
实验操作 | 实验现象 | 实验结论或总结 | ||
各步骤结论 | 总结 | |||
实验 一 | 将氯酸钾加热至融化,伸入带火星的木条 | 木条复燃 | 氯酸钾受热分解产生氧气,但____________, 反应的文字表达式:___________________ | 二氧化锰是氯酸钾 受热分解的催化剂 |
实验二 | 加热二氧化锰,伸入带火星的木条 | 木条不复燃 | 二氧化锰受热不产生氧气 | |
实验三 | ____________ | 木条迅速复燃 | 二氧化锰能加快氯酸钾的分解 | |
(1)请你帮助小明同学填写上表中未填完的空格;
(2)在小明的探究实验中,实验一和实验二起的作用是_____;
(3)小英同学认为仅由上述实验不能完全得出表内“总结”,她补充设计了 两个方面的探究实验,最终完成了对“命题”的实验证明.
第一方面的实验操作中包含了两次称量,其目的是_____;
第二方面的实验是要_____(写实验目的).
第二方面的实验目的已经明确,如何设计实验加以证明?请写出实验步骤,现象,结论:
步骤:_____.
现象:_____.
结论:_____.