题目内容
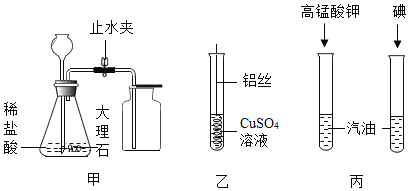
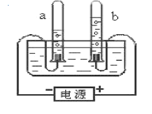
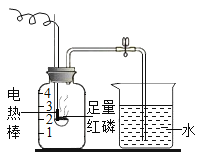
【题目】兴趣小组的同学按照课本上的实验装置做“空气中氧气含量”的测定实验(如图所示),但测出的氧气的体积分数明显小于![]() .
.
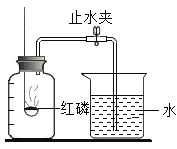
请你参与探究:
(提出问题)造成误差的原因是什么?如何改进课本上的实验装置?
(查阅资料)红磷、白磷的一些性质如下表:
颜色、状态 | 熔点/℃ | 着火点/℃ | 密度/( | |
红磷 | 暗红色固体 | 590 | 240 | 2.34 |
白磷 | 白色或黄色固体 | 44.1 | 40 | 1.82 |
(猜想与假设)
甲同学:可能是导管内残留有吸入的水,影响实验的准确性。乙同学:可能是装置气密性不好。你还能做出的猜想是________________。
(交流与讨论)
(1)丙同学认为用木炭代替红磷,就可以消除误差,大家认为他的猜想不合理,理由是____________。
(2)他们对课本上的实验装置进行了图所示的改进(其他仪器忽略).
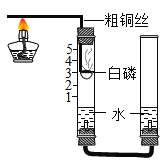
①白磷燃烧的现象__________________(与红磷相同)。
②该实验准确得出了空气中氧气含量的结论。其现象是_____________。
③与课本上的实验装置相比较,该装置的一个优点是______________。
④通过粗铜丝来点燃玻璃管内的白磷,这是利用了金属的____________性。
【答案】红磷量不足(未等冷却室温就打开了弹簧夹也可) 木炭燃烧消耗氧气,生成二氧化碳,使瓶内气压无明显变化 产生大量白烟,放出热量 左侧的玻璃管内液面上升到刻度“1”处 装置始终密封,不污染空气(或误差小也合理) 导热
【解析】
[猜想与假设]
甲同学:可能是导管内残留有吸入的水,影响实验的准确性。乙同学:可能是装置气密性不好。还有可能是红磷量不足(未等冷却室温就打开了弹簧夹也可)。
故填:红磷量不足(未等冷却室温就打开了弹簧夹也可)。
[交流与讨论]
(1)不能用木炭代替红磷,理由是木炭燃烧消耗氧气,生成二氧化碳,使瓶内气压无明显变化。
故填:木炭燃烧消耗氧气,生成二氧化碳,使瓶内气压无明显变化。
(2)
①白磷燃烧的现象产生大量白烟,放出热量。故填:产生大量白烟,放出热量。
②该实验准确得出了空气中氧气含量的结论。因为氧气约占空气体积的五分之一,其现象是左侧的玻璃管内液面上升到刻度“1”处。故填:左侧的玻璃管内液面上升到刻度“1”处。
③与课本上的实验装置相比较,该装置的一个优点是装置始终密封,不污染空气(或误差小也合理)。故填:装置始终密封,不污染空气(或误差小也合理)。
④通过粗铜丝来点燃玻璃管内的白磷,这是利用了金属的导热性。故填:导热。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】实验室有一小瓶实验课后剩余的固体![]() ,其中可能混有少量
,其中可能混有少量![]() 、
、![]() 、
、![]() 、
、![]() 中的一种或两种杂质。为了不浪费药品,实验小组在老师的指导下进行了如下实验。下图为同学们可能进行过的一些操作
中的一种或两种杂质。为了不浪费药品,实验小组在老师的指导下进行了如下实验。下图为同学们可能进行过的一些操作
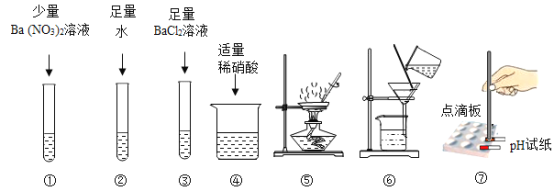
(实验一)取少量固体于试管中,依次进行以下实验确定杂质的成分
步骤 | 上图实验编号 | 实验现象 |
1 | ____________ | 得到无色澄清溶液 |
2 | ③、④ | 开始有白色沉淀,后来不再产生白色沉淀 |
3 | ①或_______ | (略) |
实验结论:![]() 固体中只有
固体中只有![]() 和
和![]() 两种杂质。
两种杂质。
(实验二)除去杂质,得到![]() 溶液作为氮肥施用到校园的花园里。
溶液作为氮肥施用到校园的花园里。
同学们经过讨论认为实验过程中加入的稀硝酸必须足够但不宜过多,为更好地控制稀硝酸的用量,应采用以下具体操作:
把瓶内固体全部倒入烧杯中,加足量水使固体全部溶解,先进行上图实验__________(填编号),再进行上图实验④至____________________________________________________(填现象)。
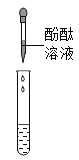
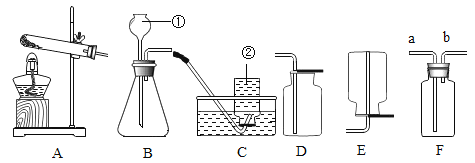
【题目】某化学兴趣小组同学取某地的石灰石和一定浓度的稀盐酸来制备二氧化碳。请你参与研究并按要求回答下列问题:
(1)下面是实验桌上摆放好的该实验所需的仪器,小明发现其中缺少了一种必需的玻璃仪器是__________;若要组装一套制取并收集二氧化碳的装置,还要选择的仪器是_______________(填仪器下方的字母),此装置还可以用于实验室制取氧气,其化学方程式为____________________。
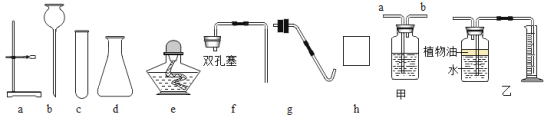
(2)若用上图甲装置干燥生成的![]() ,甲瓶中应该装入的药品是____________;若用乙装置测量二氧化碳气体的体积,乙中植物油作用是____________________。
,甲瓶中应该装入的药品是____________;若用乙装置测量二氧化碳气体的体积,乙中植物油作用是____________________。
(3)小明想弄清楚这种石灰石的纯度,于是取10![]() 石灰石样品粉碎后放入锥形瓶中,并加入了86.6
石灰石样品粉碎后放入锥形瓶中,并加入了86.6![]() 10%的稀盐酸(杂质不与酸反应,也不溶于水),充分反应后锥形瓶中的剩余物的质量为93.3
10%的稀盐酸(杂质不与酸反应,也不溶于水),充分反应后锥形瓶中的剩余物的质量为93.3![]() 。小明提出了如下计算思路:用加入盐酸的质量乘以盐酸的质量分数,求出盐酸的溶质质量,进而利用化学方程式求出石灰石中碳酸钙的质量。你认为小明的思路是否可行,理由是____________________。
。小明提出了如下计算思路:用加入盐酸的质量乘以盐酸的质量分数,求出盐酸的溶质质量,进而利用化学方程式求出石灰石中碳酸钙的质量。你认为小明的思路是否可行,理由是____________________。
通过讨论后,你计算出此石灰石中碳酸钙的质量分数为____________________。
(4)老师利用同学们制取的![]() 表演了“通气生火”的魔术。用棉花将一种淡黄色的固体包裹其中,将导气管插入棉花团中通入
表演了“通气生火”的魔术。用棉花将一种淡黄色的固体包裹其中,将导气管插入棉花团中通入![]() 气体,稍后棉花团剧烈燃烧起来。同学们为了揭开这个魔术的秘密,进行了如下探究。
气体,稍后棉花团剧烈燃烧起来。同学们为了揭开这个魔术的秘密,进行了如下探究。
(相关信息)①淡黄色固体成分是过氧化钠(![]() )。
)。
②通入的气体主要成分有二氧化碳和水蒸气。
(提出猜想)同学们发现残留固体呈白色,对该固体成分进行猜想:
猜想Ⅰ:固体成分是![]() ,
,![]() 参加反应。
参加反应。
猜想Ⅱ:固体成分是![]() ,
,![]() 参加反应。
参加反应。
猜想Ⅲ:固体成是______________________________,![]() 和
和![]() 均参加反应。
均参加反应。
(实验探究)同学们取白色固体于试管中配成溶液,设计实验对猜想进行验证。
验证Ⅰ:向溶液中滴加稀盐酸,发现有气泡产生。有同学认为固体成分仅含有![]() 。
。
验证Ⅱ:蘸取少量溶液滴到pH试纸上,与标准与色卡比较,pH大于7。有同学认为固体是![]() ,请问此结论是否正确?原因是:____________________。
,请问此结论是否正确?原因是:____________________。
验证Ⅲ:请你设计实验验证猜想Ⅲ。
步骤 | 现象 | 结论 |
①___________; ②__________。 | ①有白色沉淀到生成; ②__________________。 | 猜想Ⅲ是正确的 |
(实验反思)由验证Ⅲ的结果可知,验证Ⅰ的结论错误,因为它不能排除____________________的存在。
【题目】火锅是我国独创的美食,历史悠久。火锅常用的一种燃料是固体酒精。某化学兴趣小组的同学对“固体酒精”产生了好奇,对其成分进行探究。请你回答下列问题。
(查阅资料)
a. 固体酒精是用酒精、氢化钙和氢氧化钠按一定的质量比混合制成。
b. 氯化钙、氯化钠溶液均呈中性。

(提出问题)
①酒精中是否含有碳元素? ②固体酒精中的氢氧化钠是否变质?
(实验探究)
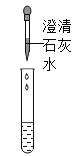
①按上图所示进行实验,发现烧杯内壁有一层白膜,可得出酒精精中含有碳元素的结论,理由是__________。
②取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,请用化学方程式表示该沉淀是如何形成的:__________________________,由此说明氢氧化钠已变质。
③为进一步确定氢氧化钠的变质程度,分组进行探究。
甲组同学取烧杯上层清液于两支试管中,按如图所示方案进行实验。
实验方案 |
|
|
实验现象 | 溶液变红 | 产生_____________ |
实验结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |
乙组同学认为甲组同学实验不能证明清液中一定含有氢氧化钠,理由是_____________________。乙组同学另取烧杯中上层清液,加足量氯化钙溶液,充分反应后,静置,取上层清液,滴加酚酞溶液,酚酞溶液变红。
(反思交流)
乙组实验中加足量氯化钙溶液的目的是_______________。
(实验结论)
甲乙两小组同学经过讨论,一致认为该固体酒精中的氢氧化钠________(填“没有”、“部分”或“全部”)变质。