ΧβΡΩΡΎ»ί
ΓΨΧβΡΩΓΩΡ≥Μ·―ß–Υ»Λ–ΓΉιΆ§―ß»ΓΡ≥ΒΊΒΡ ·Μ“ ·ΚΆ“ΜΕ®≈®Ε»ΒΡœΓ―ΈΥαά¥÷Τ±ΗΕΰ―θΜ·ΧΦΓΘ«κΡψ≤Έ”κ―–ΨΩ≤ΔΑ¥“Σ«σΜΊ¥πœ¬Ν–Έ ΧβΘΚ
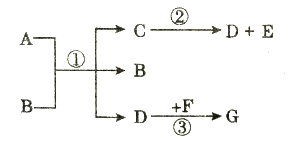
Θ®1Θ©œ¬Οφ « Β―ιΉά…œΑΎΖ≈ΚΟΒΡΗΟ Β―ιΥυ–ηΒΡ“«ΤςΘ§–ΓΟςΖΔœ÷Τδ÷–»±…ΌΝΥ“Μ÷÷±Ί–ηΒΡ≤ΘΝß“«Τς «__________ΘΜ»τ“ΣΉιΉΑ“ΜΧΉ÷Τ»Γ≤Δ ’Φ·Εΰ―θΜ·ΧΦΒΡΉΑ÷ΟΘ§ΜΙ“Σ―Γ‘ώΒΡ“«Τς «_______________Θ®Χν“«Τςœ¬ΖΫΒΡΉ÷ΡΗΘ©Θ§¥ΥΉΑ÷ΟΜΙΩ…“‘”Ο”Ύ Β―ι “÷Τ»Γ―θΤχΘ§ΤδΜ·―ßΖΫ≥Χ ΫΈΣ____________________ΓΘ
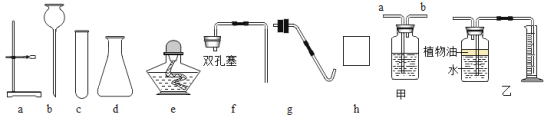
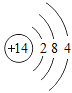
Θ®2Θ©»τ”Ο…œΆΦΦΉΉΑ÷ΟΗ…‘ο…ζ≥…ΒΡ![]() Θ§ΦΉΤΩ÷–”ΠΗΟΉΑ»κΒΡ“©ΤΖ «____________ΘΜ»τ”Ο““ΉΑ÷Ο≤βΝΩΕΰ―θΜ·ΧΦΤχΧεΒΡΧεΜΐΘ§““÷–÷≤Έο”ΆΉς”Ο «____________________ΓΘ
Θ§ΦΉΤΩ÷–”ΠΗΟΉΑ»κΒΡ“©ΤΖ «____________ΘΜ»τ”Ο““ΉΑ÷Ο≤βΝΩΕΰ―θΜ·ΧΦΤχΧεΒΡΧεΜΐΘ§““÷–÷≤Έο”ΆΉς”Ο «____________________ΓΘ
Θ®3Θ©–ΓΟςœκ≈Σ«ε≥ΰ’β÷÷ ·Μ“ ·ΒΡ¥ΩΕ»Θ§”Ύ «»Γ10![]() ·Μ“ ·―υΤΖΖέΥιΚσΖ≈»κΉΕ–ΈΤΩ÷–Θ§≤ΔΦ”»κΝΥ86.6
·Μ“ ·―υΤΖΖέΥιΚσΖ≈»κΉΕ–ΈΤΩ÷–Θ§≤ΔΦ”»κΝΥ86.6![]() 10%ΒΡœΓ―ΈΥαΘ®‘”÷ ≤Μ”κΥαΖ¥”ΠΘ§“≤≤Μ»ή”ΎΥ°Θ©Θ§≥δΖ÷Ζ¥”ΠΚσΉΕ–ΈΤΩ÷–ΒΡ Θ”ύΈοΒΡ÷ ΝΩΈΣ93.3
10%ΒΡœΓ―ΈΥαΘ®‘”÷ ≤Μ”κΥαΖ¥”ΠΘ§“≤≤Μ»ή”ΎΥ°Θ©Θ§≥δΖ÷Ζ¥”ΠΚσΉΕ–ΈΤΩ÷–ΒΡ Θ”ύΈοΒΡ÷ ΝΩΈΣ93.3![]() ΓΘ–ΓΟςΧα≥ωΝΥ»γœ¬ΦΤΥψΥΦ¬ΖΘΚ”ΟΦ”»κ―ΈΥαΒΡ÷ ΝΩ≥Υ“‘―ΈΥαΒΡ÷ ΝΩΖ÷ ΐΘ§«σ≥ω―ΈΥαΒΡ»ή÷ ÷ ΝΩΘ§ΫχΕχάϊ”ΟΜ·―ßΖΫ≥Χ Ϋ«σ≥ω ·Μ“ ·÷–ΧΦΥαΗΤΒΡ÷ ΝΩΓΘΡψ»œΈΣ–ΓΟςΒΡΥΦ¬Ζ «ΖώΩ…––Θ§άμ”… «____________________ΓΘ
ΓΘ–ΓΟςΧα≥ωΝΥ»γœ¬ΦΤΥψΥΦ¬ΖΘΚ”ΟΦ”»κ―ΈΥαΒΡ÷ ΝΩ≥Υ“‘―ΈΥαΒΡ÷ ΝΩΖ÷ ΐΘ§«σ≥ω―ΈΥαΒΡ»ή÷ ÷ ΝΩΘ§ΫχΕχάϊ”ΟΜ·―ßΖΫ≥Χ Ϋ«σ≥ω ·Μ“ ·÷–ΧΦΥαΗΤΒΡ÷ ΝΩΓΘΡψ»œΈΣ–ΓΟςΒΡΥΦ¬Ζ «ΖώΩ…––Θ§άμ”… «____________________ΓΘ
Ά®ΙΐΧ÷¬έΚσΘ§ΡψΦΤΥψ≥ω¥Υ ·Μ“ ·÷–ΧΦΥαΗΤΒΡ÷ ΝΩΖ÷ ΐΈΣ____________________ΓΘ
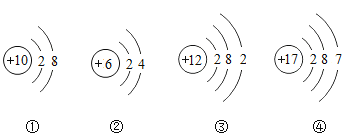
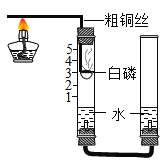
Θ®4Θ©άœ Πάϊ”ΟΆ§―ßΟ«÷Τ»ΓΒΡ![]() ±μ―ίΝΥΓΑΆ®Τχ…ζΜπΓ±ΒΡΡß θΓΘ”ΟΟόΜ®ΫΪ“Μ÷÷Β≠ΜΤ…ΪΒΡΙΧΧεΑϋΙϋΤδ÷–Θ§ΫΪΒΦΤχΙή≤ε»κΟόΜ®Ά≈÷–Ά®»κ
±μ―ίΝΥΓΑΆ®Τχ…ζΜπΓ±ΒΡΡß θΓΘ”ΟΟόΜ®ΫΪ“Μ÷÷Β≠ΜΤ…ΪΒΡΙΧΧεΑϋΙϋΤδ÷–Θ§ΫΪΒΦΤχΙή≤ε»κΟόΜ®Ά≈÷–Ά®»κ![]() ΤχΧεΘ§…‘ΚσΟόΜ®Ά≈ΨγΝ“»Φ…’Τπά¥ΓΘΆ§―ßΟ«ΈΣΝΥΫ“ΩΣ’βΗωΡß θΒΡΟΊΟήΘ§Ϋχ––ΝΥ»γœ¬ΧΫΨΩΓΘ
ΤχΧεΘ§…‘ΚσΟόΜ®Ά≈ΨγΝ“»Φ…’Τπά¥ΓΘΆ§―ßΟ«ΈΣΝΥΫ“ΩΣ’βΗωΡß θΒΡΟΊΟήΘ§Ϋχ––ΝΥ»γœ¬ΧΫΨΩΓΘ
Θ®œύΙΊ–≈œΔΘ©ΔΌΒ≠ΜΤ…ΪΙΧΧε≥…Ζ÷ «Ιΐ―θΜ·ΡΤΘ®![]() Θ©ΓΘ
Θ©ΓΘ
ΔΎΆ®»κΒΡΤχΧε÷ς“Σ≥…Ζ÷”–Εΰ―θΜ·ΧΦΚΆΥ°’τΤχΓΘ
Θ®Χα≥ω≤¬œκΘ©Ά§―ßΟ«ΖΔœ÷≤–ΝτΙΧΧε≥ ΑΉ…ΪΘ§Ε‘ΗΟΙΧΧε≥…Ζ÷Ϋχ––≤¬œκΘΚ
≤¬œκΔώΘΚΙΧΧε≥…Ζ÷ «![]() Θ§
Θ§![]() ≤ΈΦ”Ζ¥”ΠΓΘ
≤ΈΦ”Ζ¥”ΠΓΘ
≤¬œκΔρΘΚΙΧΧε≥…Ζ÷ «![]() Θ§
Θ§![]() ≤ΈΦ”Ζ¥”ΠΓΘ
≤ΈΦ”Ζ¥”ΠΓΘ
≤¬œκΔσΘΚΙΧΧε≥… «______________________________Θ§![]() ΚΆ
ΚΆ![]() Ψυ≤ΈΦ”Ζ¥”ΠΓΘ
Ψυ≤ΈΦ”Ζ¥”ΠΓΘ
Θ® Β―ιΧΫΨΩΘ©Ά§―ßΟ«»ΓΑΉ…ΪΙΧΧε”Ύ ‘Ιή÷–≈δ≥…»ή“ΚΘ§…ηΦΤ Β―ιΕ‘≤¬œκΫχ––―ι÷ΛΓΘ
―ι÷ΛΔώΘΚœρ»ή“Κ÷–ΒΈΦ”œΓ―ΈΥαΘ§ΖΔœ÷”–Τχ≈ί≤ζ…ζΓΘ”–Ά§―ß»œΈΣΙΧΧε≥…Ζ÷ΫωΚ§”–![]() ΓΘ
ΓΘ
―ι÷ΛΔρΘΚ’Κ»Γ…ΌΝΩ»ή“ΚΒΈΒΫpH ‘÷Ϋ…œΘ§”κ±ξΉΦ”κ…ΪΩ®±»ΫœΘ§pH¥σ”Ύ7ΓΘ”–Ά§―ß»œΈΣΙΧΧε «![]() Θ§«κΈ ¥ΥΫα¬έ «Ζώ’ΐ»ΖΘΩ‘≠“ρ «ΘΚ____________________ΓΘ
Θ§«κΈ ¥ΥΫα¬έ «Ζώ’ΐ»ΖΘΩ‘≠“ρ «ΘΚ____________________ΓΘ
―ι÷ΛΔσΘΚ«κΡψ…ηΦΤ Β―ι―ι÷Λ≤¬œκΔσΓΘ
≤Ϋ÷η | œ÷œσ | Ϋα¬έ |
ΔΌ___________ΘΜ ΔΎ__________ΓΘ | ΔΌ”–ΑΉ…Ϊ≥ΝΒμΒΫ…ζ≥…ΘΜ ΔΎ__________________ΓΘ | ≤¬œκΔσ «’ΐ»ΖΒΡ |
Θ® Β―ιΖ¥ΥΦΘ©”…―ι÷ΛΔσΒΡΫαΙϊΩ…÷ΣΘ§―ι÷ΛΔώΒΡΫα¬έ¥μΈσΘ§“ρΈΣΥϋ≤ΜΡή≈≈≥ΐ____________________ΒΡ¥φ‘ΎΓΘ
ΓΨ¥πΑΗΓΩΦ·ΤχΤΩ abcfhΘ®ΜρbdfhΘ© ![]() ≈®ΝρΥα Ζά÷ΙΕΰ―θΜ·ΧΦ»ή”ΎΥ° ≤ΜΩ…––Θ§Φ”»κΒΡ―ΈΥαΟΜ”–Ζ¥”ΠΆξΘ®Μρ―ΈΥα”– Θ”ύΜρ―ΈΥαΙΐΝΩΘ© 75%
≈®ΝρΥα Ζά÷ΙΕΰ―θΜ·ΧΦ»ή”ΎΥ° ≤ΜΩ…––Θ§Φ”»κΒΡ―ΈΥαΟΜ”–Ζ¥”ΠΆξΘ®Μρ―ΈΥα”– Θ”ύΜρ―ΈΥαΙΐΝΩΘ© 75% ![]() ΚΆ
ΚΆ![]() ≤Μ’ΐ»ΖΘ§ΧΦΥαΡΤ»ή“Κœ‘Φν–‘ ≤Ϋ÷η ΔΌ »Γ―υΤΖ…Ό–μ”Ύ ‘Ιή÷–Θ§ΒΈΦ”ΉψΝΩΒΡCaCl2»ή“ΚΘ§’ώΒ¥ »ΓΔΌ÷–ΒΡ…œ≤ψ«ε“Κ”Ύ ‘Ιή÷–Θ§ΒΈΦ”Έό…ΪΖ”ΧΣ»ή“ΚΘ®ΚœάμΦ¥Ω…Θ© Έό…ΪΖ”ΧΣ»ή“Κ±δ≥…Κλ…Ϊ
≤Μ’ΐ»ΖΘ§ΧΦΥαΡΤ»ή“Κœ‘Φν–‘ ≤Ϋ÷η ΔΌ »Γ―υΤΖ…Ό–μ”Ύ ‘Ιή÷–Θ§ΒΈΦ”ΉψΝΩΒΡCaCl2»ή“ΚΘ§’ώΒ¥ »ΓΔΌ÷–ΒΡ…œ≤ψ«ε“Κ”Ύ ‘Ιή÷–Θ§ΒΈΦ”Έό…ΪΖ”ΧΣ»ή“ΚΘ®ΚœάμΦ¥Ω…Θ© Έό…ΪΖ”ΧΣ»ή“Κ±δ≥…Κλ…Ϊ ![]()
ΓΨΫβΈωΓΩ
Θ®1Θ©œ¬Οφ « Β―ιΉά…œΑΎΖ≈ΚΟΒΡΗΟ Β―ιΥυ–ηΒΡ“«ΤςΘ§–ΓΟςΖΔœ÷Τδ÷–»±…ΌΝΥ“Μ÷÷±Ί–ηΒΡ≤ΘΝß“«Τς «Φ·ΤχΤΩΘΜ»τ“ΣΉιΉΑ“ΜΧΉ÷Τ»Γ≤Δ ’Φ·Εΰ―θΜ·ΧΦΒΡΉΑ÷ΟΘ§ΜΙ“Σ―Γ‘ώΒΡ“«Τς «abcfhΜρ bdfhΘ§¥ΥΉΑ÷ΟΜΙΩ…“‘”Ο”Ύ Β―ι “÷Τ»Γ―θΤχΘ§”…”Ύ≤Μ–η“ΣΦ”»»Θ§”ΠΗΟ «άϊ”ΟΙΐ―θΜ·«βΚΆΕΰ―θΜ·ΟΧ÷Τ»Γ―θΤχΘ§Ιΐ―θΜ·«β‘ΎΕΰ―θΜ·ΟΧ¥ΏΜ·Ής”Οœ¬Ζ÷Ϋβ…ζ≥…Υ°ΚΆ―θΤχΘ§ΤδΜ·―ßΖΫ≥Χ ΫΈΣΘΚ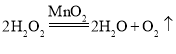 ΘΜ
ΘΜ
Θ®2Θ©»τ”ΟΆΦΦΉΉΑ÷ΟΗ…‘ο…ζ≥…ΒΡCO2Θ§ΦΉΤΩ÷–”ΠΗΟΉΑ»κΒΡ“©ΤΖ «≈®ΝρΥαΘΜ»τ”Ο““ΉΑ÷Ο≤βΝΩΕΰ―θΜ·ΧΦΤχΧεΒΡΧεΜΐΘ§““÷–÷≤Έο”ΆΉς”Ο «Ζά÷ΙΕΰ―θΜ·ΧΦ»ή”ΎΥ°ΘΜ
Θ®3Θ©–ΓΟςΒΡΥΦ¬Ζ≤ΜΩ…––Θ§άμ”… «Φ”»κΒΡ―ΈΥαΙΐΝΩΘΜ…ηΧΦΥαΗΤΉψΝΩΈΣxΘ§Ζ¥”Π…ζ≥…Εΰ―θΜ·ΧΦ÷ ΝΩΘΚ10g+86.6g -93.3g=3.3gΘ§
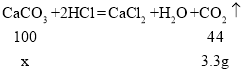
![]()
x=7.5gȧ
¥Υ ·Μ“ ·÷–ΧΦΥαΗΤΒΡ÷ ΝΩΖ÷ ΐΈΣΘΚ![]() ΓΝ100%=75%ΘΜ
ΓΝ100%=75%ΘΜ
Θ®4Θ©[Χα≥ω≤¬œκ]≤¬œκ1ΘΚΙΧΧε≥…Ζ÷ «Na2CO3ΓΔCO2≤ΈΦ”Ζ¥”ΠΘΜ
≤¬œκΔρΘΚΙΧΧε≥…Ζ÷ «NaOHΘ§H2O≤ΈΦ”Ζ¥”ΠΘΜ
≤¬œκΔσΘΚΙΧΧε≥…Ζ÷ «Na2CO3ΓΔNaOHΘ§CO2ΚΆH2O2Ψυ≤ΈΦ”Ζ¥”ΠΘΜ
[ Β―ιΧΫΨΩ]―ι÷ΛΔρΘΚ¥ΥΫα¬έ≤Μ’ΐ»ΖΘΩ‘≠“ρ «ΘΚΧΦΥαΡΤ»ή“Κœ‘Φν–‘Θ§pH“≤¥σ”Ύ7ΘΜ
―ι÷ΛΔσΘΚΔΌ”–ΑΉ…Ϊ≥ΝΒμ…ζ≥…Θ§ «“ρΈΣΧΦΥαΡΤΚΆ¬»Μ·ΗΤΖ¥”Π…ζ≥…ΑΉ…Ϊ≥ΝΒμΧΦΥαΗΤΘ§Ι ≤Ϋ÷ηΔΌΈΣ»Γ―υΤΖ…Ό–μ”Ύ ‘Ιή÷–Θ§ΒΈΦ”ΉψΝΩΒΡCaCl2»ή“ΚΘ§’ώΒ¥ΘΜ
ΔΎΉψΝΩΒΡCaCl2»ή“ΚΫΪΧΦΥαΡΤ»ή“ΚΖ¥”ΠΆξΘ§ Θ”ύ«β―θΜ·ΡΤ»ή“ΚΘ§«β―θΜ·ΡΤ»ή“Κ”ωΈό ΙΖ”ΧΣ»ή“Κ±δΚλ…ΪΘ§Ι ≤Ϋ÷ηΔΎΈΣ»ΓΔΌ÷–ΒΡ…œ≤ψ«ε“Κ”Ύ ‘Ιή÷–Θ§ΒΈΦ”Έό…ΪΖ”ΧΣ»ή“ΚΘ®ΚœάμΦ¥Ω…Θ©Θ§œ÷œσΔΎΈΣΈό…ΪΖ”ΧΣ»ή“Κ±δ≥…Κλ…ΪΘΜ
[ Β―ιΖ¥ΥΦ]”…―ι÷ΛΔσΒΡΫαΙϊΩ…÷ΣΘ§―ι÷Λ1ΒΡΫα¬έ¥μΈσΘ§“ρΈΣΥϋ≤ΜΡή≈≈≥ΐ«β―θΜ·ΡΤΒΡ¥φ‘ΎΓΘ

ΓΨΧβΡΩΓΩ≥ΘΈ¬œ¬Θ§œ¬±μΈο÷ ΖϊΚœΆΦ÷–ΉΣΜ·ΙΊœΒΒΡ «Θ®ΓΓΓΓΘ©
―Γœν | ΦΉ | ““ | ±ϊ | ΉΣΜ·ΙΊœΒΆΦ |
A | CaCO3 | CaΘ®OHΘ©2 | CaCl2 |
|
B | CuO | H2O | O2 | |
C | NaCl | NaNO3 | NaOH | |
D | CO2 | H2O | H2CO3 |
A.AB.BC.CD.D
ΓΨΧβΡΩΓΩ–Υ»Λ–ΓΉιΒΡΆ§―ßΑ¥’’ΩΈ±Ψ…œΒΡ Β―ιΉΑ÷ΟΉωΓΑΩ’Τχ÷–―θΤχΚ§ΝΩΓ±ΒΡ≤βΕ® Β―ιΘ®»γΆΦΥυ ΨΘ©Θ§ΒΪ≤β≥ωΒΡ―θΤχΒΡΧεΜΐΖ÷ ΐΟςœ‘–Γ”Ύ![]() .
.
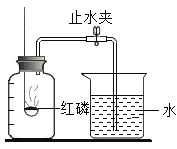
«κΡψ≤Έ”κΧΫΨΩΘΚ
Θ®Χα≥ωΈ ΧβΘ©‘λ≥…Έσ≤νΒΡ‘≠“ρ « ≤Ο¥ΘΩ»γΚΈΗΡΫχΩΈ±Ψ…œΒΡ Β―ιΉΑ÷ΟΘΩ
Θ®≤ι‘ΡΉ ΝœΘ©ΚλΝΉΓΔΑΉΝΉΒΡ“Μ–©–‘÷ »γœ¬±μΘΚ
―’…ΪΓΔΉ¥Χ§ | »έΒψ/Γφ | Ή≈ΜπΒψ/Γφ | ΟήΕ»/Θ® | |
ΚλΝΉ | ΑΒΚλ…ΪΙΧΧε | 590 | 240 | 2.34 |
ΑΉΝΉ | ΑΉ…ΪΜρΜΤ…ΪΙΧΧε | 44.1 | 40 | 1.82 |
Θ®≤¬œκ”κΦΌ…ηΘ©
ΦΉΆ§―ßΘΚΩ…Ρή «ΒΦΙήΡΎ≤–Ντ”–Έϋ»κΒΡΥ°Θ§”Αœλ Β―ιΒΡΉΦ»Ζ–‘ΓΘ““Ά§―ßΘΚΩ…Ρή «ΉΑ÷ΟΤχΟή–‘≤ΜΚΟΓΘΡψΜΙΡήΉω≥ωΒΡ≤¬œκ «________________ΓΘ
Θ®ΫΜΝς”κΧ÷¬έΘ©
Θ®1Θ©±ϊΆ§―ß»œΈΣ”ΟΡΨΧΩ¥ζΧφΚλΝΉΘ§ΨΆΩ…“‘œϊ≥ΐΈσ≤νΘ§¥σΦ“»œΈΣΥϊΒΡ≤¬œκ≤ΜΚœάμΘ§άμ”… «____________ΓΘ
Θ®2Θ©ΥϊΟ«Ε‘ΩΈ±Ψ…œΒΡ Β―ιΉΑ÷ΟΫχ––ΝΥΆΦΥυ ΨΒΡΗΡΫχΘ®ΤδΥϊ“«ΤςΚω¬‘Θ©.
ΔΌΑΉΝΉ»Φ…’ΒΡœ÷œσ__________________Θ®”κΚλΝΉœύΆ§Θ©ΓΘ
ΔΎΗΟ Β―ιΉΦ»ΖΒΟ≥ωΝΥΩ’Τχ÷–―θΤχΚ§ΝΩΒΡΫα¬έΓΘΤδœ÷œσ «_____________ΓΘ
Δέ”κΩΈ±Ψ…œΒΡ Β―ιΉΑ÷Οœύ±»ΫœΘ§ΗΟΉΑ÷ΟΒΡ“ΜΗω”≈Βψ «______________ΓΘ
ΔήΆ®Ιΐ¥÷Ά≠ΥΩά¥Βψ»Φ≤ΘΝßΙήΡΎΒΡΑΉΝΉΘ§’β «άϊ”ΟΝΥΫπ τΒΡ____________–‘ΓΘ