题目内容
【题目】[观察与问题]镁条在空气中久置表面会变黑,某小组同学设计并进行实验,探究镁条变黑的条件。
I.从生成物角度分析,进行探究
实验一:刮下镁条表面的黑色物质于试管中,加入足量的稀盐酸产生气体,把生成的气体通入澄清石灰水,观察到石灰水变浑浊。由此可知镁条变黑与空气中的_________有关,原因是_________。
II.从反应物角度分析,进行探究
[猜想与假设]在实验一的基础上猜想镁条变黑具体与空气中的哪些物质有关,甲、乙、丙、丁四位同学分别提出了如下猜想:
甲: CO2
乙: CO2 O2
丙: CO2 H2O
丁:_________。
[实验与探究]
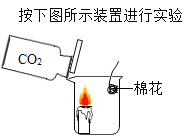
实验二:通过控制与镁条接触的物质,利用如图所示装置(镁条长度为3 cm,试管容积为20 mL),分别进行下列4个实验,并持续观察10天。请将下表中实验操作补充完整。
编号 | 主要实验操作 | 实验现象 |
① | 先收集满二氧化碳,再加入2ml浓硫酸 | 镁条始终无明显变化 |
② | 先集满体积比为1 : 1的二氧化碳和氧气的混合气体,再加 入__________ mL浓硫酸 | 镁条始终无明显变化 |
③ | 先收集满二氧化碳,再加入2mL蒸馏水 | 镁条始终无明显变化 |
④ | 先集满体积比为1 : 1的二氧化碳和氧气的混合气体,再加入2 mL蒸馏水 | 镁条第1天开始变黑至第10天全部变黑 |
[解释与结论]
(1)实验①和②中的浓硫酸的作用是___________。在这两个实验中____________(填“能”或“不能”)用烧碱代替浓硫酸,原因是_____________(用化学方程式表示)。
(2)实验③的目的__________。
(3)由上述实验可推知,镁条变黑的条件是________。
[反思与评价]
(4)在猜想与假设时,同学们认为镁条变黑与N2无关,其理由是__________。
【答案】二氧化碳 黑色物质中含碳元素,说明空气中的二氧化碳参加反应 CO2、H2O、O2 2 干燥装置内的气体 不能 ![]() 探究镁条在只和二氧化碳、水接触的情况下是否会变黑 镁条同时与CO2、O2和H2O接触 N2的化学性质不活泼,常温下很难与Mg反应
探究镁条在只和二氧化碳、水接触的情况下是否会变黑 镁条同时与CO2、O2和H2O接触 N2的化学性质不活泼,常温下很难与Mg反应
【解析】
I、澄清石灰水变浑浊,说明黑色物质与酸反应产生了二氧化碳,其中的碳元素来自空气中,空气中含有碳元素的成分只有二氧化碳,故镁条变黑与二氧化碳有关;
II、由前述分析可知,镁条变黑一定与二氧化碳有关,可能还与氧气和水蒸气有关,列出所有的可能,故丁的猜想应为CO2、H2O、O2;
②、根据控制单一变量的原则,浓硫酸的用量必须前后一致,故加入浓硫酸为2ml;
(1)浓硫酸具有吸水性,实验①和②中加入浓硫酸主要是为了除去装置中的水蒸气,干燥装置内的气体;烧碱具有潮解性,也可作为干燥剂,但烧碱溶液还能和二氧化碳反应生成碳酸钠和水,故不能使用烧碱作为该实验的干燥剂,反应的化学方程式为![]() ;
;
(2)实验条件为,镁条与二氧化碳和水接触,因此探究镁条在只和二氧化碳、水接触的情况下是否会变黑
(3) 镁条只与CO2、CO2+O2或CO2 +H2O接触时均不会变黑,只有镁条同时与CO2、O2和H2O才会变黑,由此可以得出实验结论,镁条同时与CO2、O2和H2O接触的情况下才会变黑;
(4) N2的化学性质不活泼,常温下很难与其他物质反应,因此氮气不能与镁反应。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案【题目】新年联欢晚会上,老师给同学们表演了一个魔术:大烧杯中盛有一只燃着的蜡烛和 一团包有过氧化钠 (Na2O2)的棉花,将一瓶二氧化碳倒入烧杯中,蜡烛慢慢的熄灭,然后棉花突然剧烈的燃烧起来。这出乎意料的现象引起了同学们的极大兴趣, 请你参与同学们的讨论和探究。
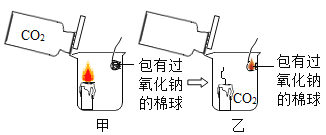
蜡烛熄灭的原因是 __________________。
(提出问题)棉花为什么会燃烧?
(提出猜想)
(1)可能是蜡烛燃烧引燃了棉花。
(2)可能是二氧化碳与过氧化钠反应生成了氧气。
(3)可能是二氧化碳与过氧化钠反应放出了热量。
(实验验证)
序号 | 实验操作 | 主要实验现象 | 实验结论及解释 |
① |
| 蜡烛慢慢熄灭 | 猜想(1)____(填“成立”或 “不成立”) |
② | 向盛满二氧化碳的集气瓶中加入适量的过氧化钠粉末,充分振荡,并将带火星木条伸入集气瓶中 | _____ | 二氧化碳与过氧化钠反应生成了氧气,猜想(2)成立 |
③ | _____ | _____ | 猜想(3)成立 |
(实验结论)
(1)CO2与 Na2O2反应生成了氧气与一种化合物,反应的化学方程式为__________。
(2)通常 CO2可作灭火剂,但有些物质(如 Na2O2)着火,不能用CO2熄灭。