题目内容
【题目】中和反应是一类重要的化学反应:
①能与稀硫酸发生中和反应的_____________
A 氢氢化钡 B 碳酸钠 C 镁带 D 氧化铜
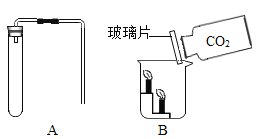
②小组同学将氢氧化钠溶液和稀盐酸混合反应。实验装置如图,采用无色酚酞试液作酸碱指示剂,用传感器分别测定溶液pH、溶液温度的变化情况。请写出该中和反应的化学方程式:____________。根据表格数据回答:

滴加液体的体积(毫升) | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
pH | 13.1 | 12.8 | 12.3 | 11.5 | 10.4 | 7.0 | 2.7 | 2.3 | 2.2 | 2.1 | 2.0 |
温度(℃) | 25.5 | 25.8 | 26.1 | 26.4 | 26.8 | 27.0 | 26.9 | 26.8 | 26.7 | 26.6 | 26.6 |
③混合前,烧杯内的是_______________溶液,判断的依据是________。
④当滴加液体体积为________________mL时,酸碱中和反应恰好完成。根据表格数据可判断;中和反应是____________(填“吸热”“放热”或“无变化”)的反应,理由是__________
⑤当滴加液体6mL时,烧杯中的溶质(除酚酞以外)有________(填化学式);若酚酞无色则滴加液体的体积可能是___________mL
A 4 B 8 C 10 D 14
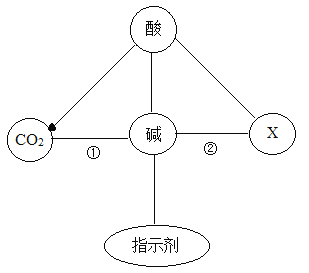
⑥有同学发现在实验过程中,开始时没有气泡,持续滴加液体后,观察到有气泡产生,请分析可能的原因________,并设计实验证明你的结论________________
⑦现有两杯质量相同、溶质质量分数相同的NaOH溶液和KOH溶液,在NaOH溶液中加入xg盐酸恰好中和;在KOH溶液中加入yg上述盐酸也能恰好中和,则x____________y
A > B < C = D 无法判断
【答案】A NaOH+HCl=NaCl+H2O 氢氧化钠 随着溶液的滴加,混合溶液的pH逐渐减小 10 放热 溶液的pH由13.1变为7的过程中溶液的温度逐渐升高 NaOH和NaCl CD 氢氧化钠变质 取少许溶液,滴入少量的氯化钙溶液或澄清的石灰水,观察到有白色沉淀生成 B
【解析】
①能与稀硫酸发生中和反应的物质属于碱,A 氢氢化钡属于碱,可以与酸发生中和反应,选项正确;
B 碳酸钠属于盐,虽然能与硫酸反应,但不属于中和反应,选项错误;
C 镁带与硫酸反应生成硫酸镁和氢气,是金属单质与酸的反应,不属于中和反应,选项错误;
D 氧化铜属于金属氧化物,与硫酸德 反应不属于中和反应,选项错误,故填A。
②氢氧化钠与盐酸反应生成氯化钠和水,故反应的化学方程式写为:NaOH+HCl=NaCl+H2O。
③由图可知,混合前烧杯内的溶液的pH为13.1,溶液显碱性,所以混合前的溶液是氢氧化钠溶液,故填氢氧化钠;
由图可知,随着溶液的滴加,混合溶液的pH逐渐减小,说明是将酸性溶液滴入碱性溶液中,故填随着溶液的滴加,混合溶液的pH逐渐减小。
④由图可知,当滴加液体体积为10mL时,溶液的pH为7,则酸碱中和反应恰好完成,故填10;
由图可知,中和反应是放热的反应,故填放热;
表中当溶液的pH由13.1变为7的过程中溶液的温度逐渐升高,证明中和反应是放热的反应,故填溶液的pH由13.1变为7的过程中溶液的温度逐渐升高。
⑤当滴加液体6mL时,溶液的pH为11.5,溶液显碱性,则溶液中的溶质烧杯中的溶质(除酚酞以外)还有未反应的氢氧化钠和反应生成的氯化钠,其化学式分别为NaOH和NaCl,故填NaOH和NaCl;
若酚酞无色,则溶液显酸性或中性,由图可知,A 当加入4mL液体时,溶液的pH为12.3,溶液显碱性,选项错误,B 当加入液体为8mL时,溶液的pH为10.4,溶液显碱性,选项错误,C 当加入液体为10mL时,溶液的pH为7,溶液显中性,选项正确,D 当加入液体14mL时,溶液的pH为2.3,溶液显酸性,选项正确,故填CD。
⑥持续滴加液体后,观察到有气泡产生是因为氢氧化钠与空气中的二氧化碳反应变质生成碳酸钠和水,碳酸钠能与盐酸反应生成氯化钠、水和二氧化碳,故填氢氧化钠变质;
取少许溶液,滴入少量的氯化钙溶液或澄清的石灰水,观察到有白色沉淀生成,说明氢氧化钠变质,故填取少许溶液,滴入少量的氯化钙溶液或澄清的石灰水,观察到有白色沉淀生成。
⑦解:质量相同、溶质质量分数相同的NaOH溶液和KOH溶液中NaOH与KOH的质量相同
设质量为m的氢氧化钠消耗的盐酸的质量为x
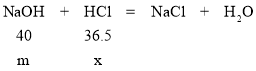
40:36.5=m:x x=![]()
设质量为m的氢氧化钾消耗的盐酸的质量为y
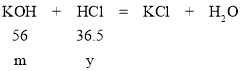
56:36.5=m:y y=![]()
![]() <
<![]() ,即x<y,故填B。
,即x<y,故填B。

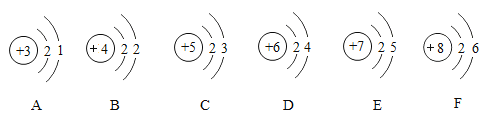
【题目】物质都是由微观粒子构成的。在构成下列四种物质的微粒示意图中, “○”和“![]() ”分别表示氢和氧两种元素的原子。
”分别表示氢和氧两种元素的原子。
物 质 | 甲 | 乙 | 丙 | 丁 |
构成该物质的粒子 |
|
|
|
|
(1)四种物质中,属于单质的是__________(填物质代号,下同)。
(2)四种物质中,不同种元素原子个数比为1:1的是___________,含有H2分子的是___________。
(3)甲物质在一定条件下反应可生成丙,该反应的化学方程式为______________,该反应属于________反应(填“化合”或“分解”)。