题目内容
【题目】如图表示碱与不同类别物质之间的性质关系(“—”表示相连物质能发生反应,“→”表示两种物质间的转化关系,部分物质和反应条件已省略),请回答问题。
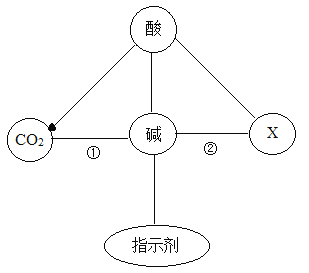
(1)X的物质类别____________。
(2)根据性质①写出检验CO2的化学反应方程式__________________________。
(3)根据性质②写出能体现碱的相似化学性质的反应方程式__________________。
【答案】盐 Ca(OH)2+CO2==CaCO3↓+H2O 2NH4Cl+ Ca(OH)2![]() CaCl2+2NH3↑+2H2O (符合题意即可)
CaCl2+2NH3↑+2H2O (符合题意即可)
【解析】
本题主要考察碱的通性
(1)由图可知:X的物质类别只能是盐类
(2)用石灰水检验CO2的反应原理:CO2+Ca(OH)2=CaCO3↓+H2O
(3)性质②中碱与盐反应:2NH4Cl+ Ca(OH)2![]() CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O

 名校课堂系列答案
名校课堂系列答案【题目】中和反应是一类重要的化学反应:
①能与稀硫酸发生中和反应的_____________
A 氢氢化钡 B 碳酸钠 C 镁带 D 氧化铜
②小组同学将氢氧化钠溶液和稀盐酸混合反应。实验装置如图,采用无色酚酞试液作酸碱指示剂,用传感器分别测定溶液pH、溶液温度的变化情况。请写出该中和反应的化学方程式:____________。根据表格数据回答:

滴加液体的体积(毫升) | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
pH | 13.1 | 12.8 | 12.3 | 11.5 | 10.4 | 7.0 | 2.7 | 2.3 | 2.2 | 2.1 | 2.0 |
温度(℃) | 25.5 | 25.8 | 26.1 | 26.4 | 26.8 | 27.0 | 26.9 | 26.8 | 26.7 | 26.6 | 26.6 |
③混合前,烧杯内的是_______________溶液,判断的依据是________。
④当滴加液体体积为________________mL时,酸碱中和反应恰好完成。根据表格数据可判断;中和反应是____________(填“吸热”“放热”或“无变化”)的反应,理由是__________
⑤当滴加液体6mL时,烧杯中的溶质(除酚酞以外)有________(填化学式);若酚酞无色则滴加液体的体积可能是___________mL
A 4 B 8 C 10 D 14
⑥有同学发现在实验过程中,开始时没有气泡,持续滴加液体后,观察到有气泡产生,请分析可能的原因________,并设计实验证明你的结论________________
⑦现有两杯质量相同、溶质质量分数相同的NaOH溶液和KOH溶液,在NaOH溶液中加入xg盐酸恰好中和;在KOH溶液中加入yg上述盐酸也能恰好中和,则x____________y
A > B < C = D 无法判断
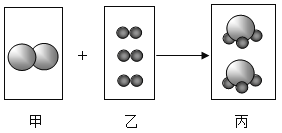
【题目】某CO气体中混有少量的CO2,为探究CO的性质,某同学在老师的指导下设计了以下实验装置,请填写下列空白.
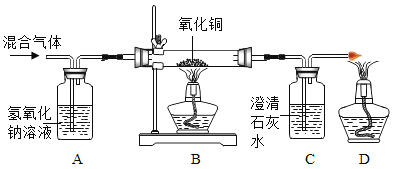
(1)A装置的作用是___________.B处玻璃管内的现象是___________.
(2)C处反应的化学方程式为___________;
(3)实验时,应___________(选填“先”或“后”)点燃B处的酒精灯;
(4)某同学对B处玻璃管内剩余固体成分产生浓厚兴趣.
(提出问题)B处玻璃管内的剩余固体是什么?
(假设猜想)猜想①:剩余固体全部是铜 猜想②:剩余固体是铜和氧化铜的混合物
(实验设计)
实验步骤 | 实验中可能出现的现象 | 结论 |
取B处玻璃管内少量剩余固体于试管中加入 ___________ | 现象一:固体不溶解,溶液不变色 | 猜想①___________(选填“成立”或“不成立”) |
现象二: ___________ | 猜想②成立 |
(拓展延伸)
(Ⅰ)D处酒精灯的作用是___________;
(Ⅱ)根据B处的反应原理,CO可用于___________.
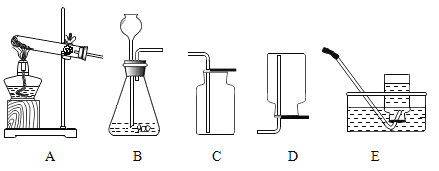
【题目】某化学兴趣小组同学以“比较铝和锌的金属活动性强弱”为课题进行探究,下面是小华同学和小明同学探究的主要过程:
(提出问题)铝和锌两种金属,哪一种金属活动性更强?
(实验原理)小华同学利用常温下两种金属与酸反应,测定收集等体积氢气所需的时间,判断金属活动性强弱;小明同学利用金属与盐溶液的反应比较金属活动性强弱。
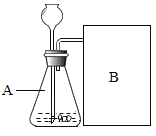
(进行实验)
实验一:上图是小华的实验装置图,实验中B处宜采用的气体收集方法是________。
实验编号 | 实验1 | 实验2 |
金属 | 1g表面未氧化的锌粒 | 1g表面打磨过的铝片 |
酸溶液 | 10mL10%的稀盐酸溶液 | 10mL10%的稀硫酸溶液 |
收集20mL氢气所需的时间 | 42s | 64s |
实验结论 | 根据实验现象,得出Zn____Al(填“>” “<”或“=” | |
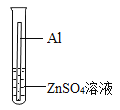
实验二:小明的实验方案
实验步骤 | 实验现象 | 实验结论 |
将表面打磨过的铝片插入硫酸锌溶液中
| ______ | 金属活动性:Al>Zn |
(分析与评价)
①写出铝与硫酸锌溶液反应的化学方程式_____________;
②两位同学的实验结论刚好相反,你判断______同学实验结论错误,理由是__________。
(实验延伸)为了研究金属与酸反应的其他影响因素,小明用纯锌和纯度为90%的粗锌在相同条件下反应,发现粗锌反应速率更快。
(查阅资料)粗锌中含有铜等与酸不反应的杂质
(猜想与假设)造成粗锌反应速率更快的原因可能是___________。
(设计实验)请设计合理的实验方案验证你的猜想。
实验步骤 | 实验可能的现象及结论 |
__________ | ___________ |