题目内容
【题目】下图一是某金属元素形成微粒的结构示意图。

请根据以上信息回答问题:
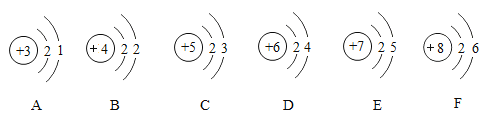
(1)图一所示微粒的符号为________;下图中与该金属元素的原子化学性质相似的是_____________。(填序号)
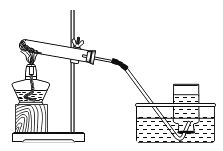
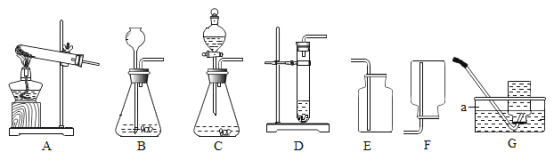
(2)利用图二所示实验装置制取氧气,能够用图二收集氧气的原因是________;若选择高锰酸钾制取氧气,写出高锰酸钾的化学式并标出锰元素化合价________
【答案】Mg2+ B 氧气不易溶于水 ![]()
【解析】
(1)图一所示微粒中质子数大于电子数,为镁离子,符号为Mg2+;故填:Mg2+。
(2)镁原子的最外层电子数为2,元素的化学性质与原子的最外层的电子数有关, B原子的最外层电子数是2,故与镁原子的化学性质相似,故填:B。
(2)能用排水法收集氧气的原因是氧气不易溶于水;高锰酸钾的化学式为KMnO4,其中锰元素的化合价为+7价,故填:氧气不易溶于水;![]() 。
。

 新题型全程检测期末冲刺100分系列答案
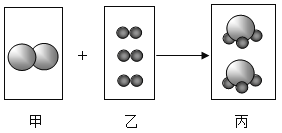
新题型全程检测期末冲刺100分系列答案【题目】在宏观、微观和符号之间建立联系是化学学科的特点。甲和乙反应生成丙和丁的化学方程式用下列微观示意图表示:
物质 | 甲 | 乙 | 丙 | 丁 |
|
微观 示意图 |
| ||||
①请写出丙物质的化学式_____;下列属于丁物质的微观示意图的是_____。
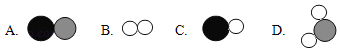
②能保持甲化学性质的微粒是_____(填“分子”或“原子”),四种物质中属于氧化物的有_____(填甲、乙、丙、丁)。
③从上述反应重能获得的信息有_____(填一条即可)。
④上述微观示意图表示的化学方程式是:_____。
【题目】下列实验设计不合理的是 ( )
选项 | 实验目的 | 操作或所用试剂 |
A | 鉴别NaOH溶液、Na2CO3溶液 | 无色酚酞 |
B | 鉴别NaCl、KCl | 焰色反应 |
C | 除去CO中的 | NaOH溶液、浓 |
D | 除去氯化钠固体中混有的泥沙 | 溶解、过滤、蒸发 |
A.AB.BC.CD.D
【题目】中和反应是一类重要的化学反应:
①能与稀硫酸发生中和反应的_____________
A 氢氢化钡 B 碳酸钠 C 镁带 D 氧化铜
②小组同学将氢氧化钠溶液和稀盐酸混合反应。实验装置如图,采用无色酚酞试液作酸碱指示剂,用传感器分别测定溶液pH、溶液温度的变化情况。请写出该中和反应的化学方程式:____________。根据表格数据回答:

滴加液体的体积(毫升) | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
pH | 13.1 | 12.8 | 12.3 | 11.5 | 10.4 | 7.0 | 2.7 | 2.3 | 2.2 | 2.1 | 2.0 |
温度(℃) | 25.5 | 25.8 | 26.1 | 26.4 | 26.8 | 27.0 | 26.9 | 26.8 | 26.7 | 26.6 | 26.6 |
③混合前,烧杯内的是_______________溶液,判断的依据是________。
④当滴加液体体积为________________mL时,酸碱中和反应恰好完成。根据表格数据可判断;中和反应是____________(填“吸热”“放热”或“无变化”)的反应,理由是__________
⑤当滴加液体6mL时,烧杯中的溶质(除酚酞以外)有________(填化学式);若酚酞无色则滴加液体的体积可能是___________mL
A 4 B 8 C 10 D 14
⑥有同学发现在实验过程中,开始时没有气泡,持续滴加液体后,观察到有气泡产生,请分析可能的原因________,并设计实验证明你的结论________________
⑦现有两杯质量相同、溶质质量分数相同的NaOH溶液和KOH溶液,在NaOH溶液中加入xg盐酸恰好中和;在KOH溶液中加入yg上述盐酸也能恰好中和,则x____________y
A > B < C = D 无法判断
【题目】某化学兴趣小组同学以“比较铝和锌的金属活动性强弱”为课题进行探究,下面是小华同学和小明同学探究的主要过程:
(提出问题)铝和锌两种金属,哪一种金属活动性更强?
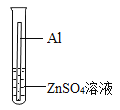
(实验原理)小华同学利用常温下两种金属与酸反应,测定收集等体积氢气所需的时间,判断金属活动性强弱;小明同学利用金属与盐溶液的反应比较金属活动性强弱。
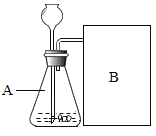
(进行实验)
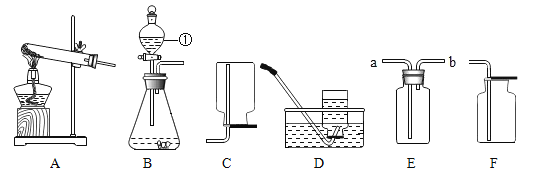
实验一:上图是小华的实验装置图,实验中B处宜采用的气体收集方法是________。
实验编号 | 实验1 | 实验2 |
金属 | 1g表面未氧化的锌粒 | 1g表面打磨过的铝片 |
酸溶液 | 10mL10%的稀盐酸溶液 | 10mL10%的稀硫酸溶液 |
收集20mL氢气所需的时间 | 42s | 64s |
实验结论 | 根据实验现象,得出Zn____Al(填“>” “<”或“=” | |
实验二:小明的实验方案
实验步骤 | 实验现象 | 实验结论 |
将表面打磨过的铝片插入硫酸锌溶液中
| ______ | 金属活动性:Al>Zn |
(分析与评价)
①写出铝与硫酸锌溶液反应的化学方程式_____________;
②两位同学的实验结论刚好相反,你判断______同学实验结论错误,理由是__________。
(实验延伸)为了研究金属与酸反应的其他影响因素,小明用纯锌和纯度为90%的粗锌在相同条件下反应,发现粗锌反应速率更快。
(查阅资料)粗锌中含有铜等与酸不反应的杂质
(猜想与假设)造成粗锌反应速率更快的原因可能是___________。
(设计实验)请设计合理的实验方案验证你的猜想。
实验步骤 | 实验可能的现象及结论 |
__________ | ___________ |