题目内容
【题目】化学兴趣小组的同学设计并进行了CO2的制取与性质的实验。
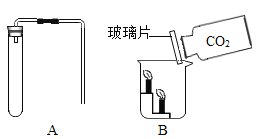
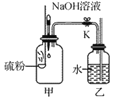
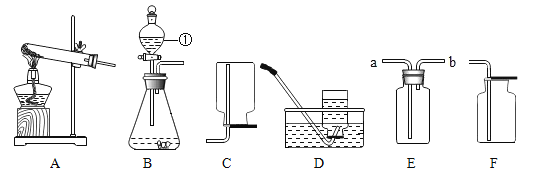
制取与性质:如图A,检查装置的气密性,操作为_____,观察到导管口有气泡冒出。然后加入药品,固定装置,制取CO2,有关化学方程式_____。如图B,现象为_____,说明CO2的性质是_____。由此推知,一般情况下可燃物燃烧的条件之一是_____。
反思与交流:(1)制备气体时选择发生装置需考虑的因素有_____。
(2)欲证明人吸入的空气与呼出的气体中CO2的含量不同,你的实验操作是:取一瓶空气、一瓶等体积的呼出气体,_____。
【答案】导管末端放入水中,手握试管 CaCO3+2HCl=CaCl2+H2O+CO2↑ 下层蜡烛先灭,上层蜡烛后灭 不能燃烧,不支持燃烧,密度比空气大 与O2(或空气)接触 反应物的状态和反应条件 加入等体积等浓度(等溶质质量分数或饱和)澄清石灰水,振荡
【解析】
检查A装置的气密性,操作为将导管末端放入水中,手紧握试管外壁,观察到导管口有气泡冒出,说明装置气密性良好。实验室用石灰石与稀盐酸制取二氧化碳,石灰石主要成分是碳酸钙,制取CO2的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑。图B中的现象为下层蜡烛先灭,上层蜡烛后灭,说明CO2不能燃烧,不支持燃烧,密度比空气大。由此推知,一般情况下可燃物燃烧的条件之一是与O2(或空气)接触。
反思与交流:(1)制备气体时选择发生装置需考虑的因素有:反应物的状态和反应条件,根据反应物的状态及反应条件来选择发生装置。(2)检验二氧化碳用澄清石灰水,故欲证明人吸入的空气与呼出的气体中CO2的含量不同,实验操作是:取一瓶空气、一瓶等体积的呼出气体,加入等体积、等浓度(等溶质质量分数或饱和)的澄清石灰水,振荡,先变浑浊的则二氧化碳含量高。

【题目】下列实验设计不合理的是 ( )
选项 | 实验目的 | 操作或所用试剂 |
A | 鉴别NaOH溶液、Na2CO3溶液 | 无色酚酞 |
B | 鉴别NaCl、KCl | 焰色反应 |
C | 除去CO中的 | NaOH溶液、浓 |
D | 除去氯化钠固体中混有的泥沙 | 溶解、过滤、蒸发 |
A.AB.BC.CD.D
【题目】中和反应是一类重要的化学反应:
①能与稀硫酸发生中和反应的_____________
A 氢氢化钡 B 碳酸钠 C 镁带 D 氧化铜
②小组同学将氢氧化钠溶液和稀盐酸混合反应。实验装置如图,采用无色酚酞试液作酸碱指示剂,用传感器分别测定溶液pH、溶液温度的变化情况。请写出该中和反应的化学方程式:____________。根据表格数据回答:

滴加液体的体积(毫升) | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
pH | 13.1 | 12.8 | 12.3 | 11.5 | 10.4 | 7.0 | 2.7 | 2.3 | 2.2 | 2.1 | 2.0 |
温度(℃) | 25.5 | 25.8 | 26.1 | 26.4 | 26.8 | 27.0 | 26.9 | 26.8 | 26.7 | 26.6 | 26.6 |
③混合前,烧杯内的是_______________溶液,判断的依据是________。
④当滴加液体体积为________________mL时,酸碱中和反应恰好完成。根据表格数据可判断;中和反应是____________(填“吸热”“放热”或“无变化”)的反应,理由是__________
⑤当滴加液体6mL时,烧杯中的溶质(除酚酞以外)有________(填化学式);若酚酞无色则滴加液体的体积可能是___________mL
A 4 B 8 C 10 D 14
⑥有同学发现在实验过程中,开始时没有气泡,持续滴加液体后,观察到有气泡产生,请分析可能的原因________,并设计实验证明你的结论________________
⑦现有两杯质量相同、溶质质量分数相同的NaOH溶液和KOH溶液,在NaOH溶液中加入xg盐酸恰好中和;在KOH溶液中加入yg上述盐酸也能恰好中和,则x____________y
A > B < C = D 无法判断