题目内容
【题目】NH4C1和Na2SO4的溶解度表及溶解度曲线如下。下列说法正确的是( )
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度S/g | NH4C1 | 3.33 | 37.2 | 41.4 | 45.8 | 50.4 | 60.2 |
Na2SO4 | 9.6 | 20.2 | 40.8 | 48.4 | 47.5 | 47.0 | |
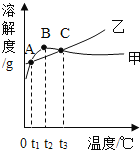
A.甲为NH4C1的溶解度曲线
B.两种物质的溶解度均随温度升高而增大
C.甲、乙饱和溶液从t3降温到t2,溶质的质量分数都变小
D.等质量的甲、乙饱和溶液从t1升温到t3,为使其溶液恰好饱和,加入的甲、乙固体质量相等
【答案】D
【解析】
A. 根据NH4C1和Na2SO4的溶解度表可知,NH4C1的溶解度随温度升高而增大,Na2SO4的溶解度随温度升高先增大后减小,所以溶解度曲线中甲是Na2SO4的溶解度曲线,不符合题意;
B. NH4C1的溶解度随温度升高而增大,Na2SO4的溶解度随温度升高先增大后减小,不符合题意;
C. 甲、乙饱和溶液从t3降温到t2,甲的溶解度增大,所以不会有晶体析出,溶质的质量分数不变,乙的溶解度减小,有晶体析出,溶质的质量分数减小,不符合题意;
D. t1时, 甲、乙的溶解度相等,所以等质量的甲、乙饱和溶液中溶质质量相等,t3时,甲、乙的溶解度仍然相等,为了使甲、乙溶液还是饱和溶液,那么加入的甲、乙固体质量也相等,符合题意。故选D。

【题目】化学实验探究总是能引起同学们的兴趣。某化学兴趣小组在实验室实验时发现了一瓶标签缺损的溶液,如下图。为了确认其溶质成分,同学们进行了如下探究:
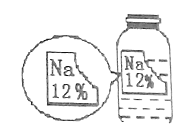
(提出猜想)猜想一:NaCl; 猜想二:Na2CO3;猜想三: NaHCO3 猜想四:NaOH
(设计实验一)
小明取少量溶液样品于试管中,用玻璃棒蘸取溶液滴在pH试纸上,读取数据,pH=9,得出结论,猜想四成立。
小王认为小明的结论不准确,理由是:________________。
从小明的实验结果中可以判断出猜想_________也一定是错误的。
(设计实验二)小红取适量稀盐酸于试管中,滴加少量此溶液,溶液中产生气泡。于是认为猜想二正确。
小王认为仍然不能确定,理由是_______________。
(查阅资料)常温下,碳酸钠和碳酸氢钠的溶解度为以下表格中的数据。
Na2CO3 | NaHCO3 | |
溶解度/g | 21.8 | 9.6 |
(分析结论)从资料显示的数据,再结合药品的标签,可以判断猜想_________不正确,理由是_____________________。
(问题交流)(1)Na2CO3和 NaHCO3在生活中被称为“苏打兄弟”,其中NaHCO3在生活中可用来_______________ (写出一条即可)。
(2)Na2CO3在空气中长期放置,会吸收空气中水蒸气和另一种气体而转变成 NaHCO3。请你写出反应方程式________________________。
[注意:若答对以下问题可奖励4分,化学试卷总分不超过60分。]
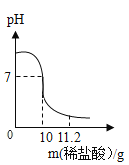
兴趣小组和老师一起继续实验,将盐酸滴加到Na2CO3溶液中进行反应,并用数字化实验装置pH传感器测定了溶液中pH的变化。采集数据得到曲线如下图所示。
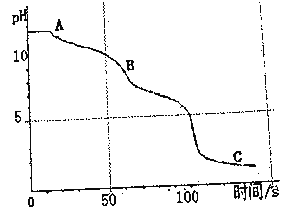
(3)0-50s时,同学们观察到溶液中并没有想象中的气泡产生,请你写出AB段发生反应的化学方程式:__________________。
(4)B点溶液pH大于7,是因为___________(填物质名称)的水溶液呈碱性。
(5)C点所得溶液的溶质是__________________。
【题目】镁条在空气中剧烈燃烧,发出耀眼的白光,生成白色固体,细心的小明同学发现,镁条燃烧除生成白色固体外,还有少量的淡黄色固体生成,经查阅资料得知:淡黄色固体是由镁条和空气中的氮气化合产生的,写出该反应的化学方程式__,产生的白色固体比淡黄色固体多的原因是__。他还发现镁条在空气中久置表面会变黑,实验小组同学设计并进行实验,探究镁条变黑的条件。
[猜想假设]常温下,镁条变黑可能与O2、CO2、水蒸气有关。
[查阅资料]常温下,亚硫酸钠(Na2SO3)可与O2发生化合反应。
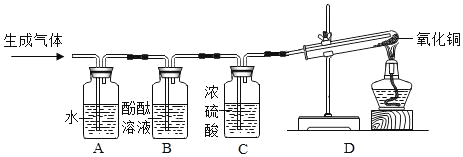
[设计实验]通过控制与镁条接触的物质,利用右图装置(镁条长度为3cm,试管容积为20mL) ,分别进行下列5个实验,并持续观察20天。

实验操作 | 实验现象 |
1.先充满用NaOH浓溶液洗涤过的空气,再加人2mL浓硫酸 | 镁条始终无明显变化 |
2.加人NaOH浓溶液 | 镁条始终无明显变化 |
3.先加人2mL浓硫酸,再通入约4mLCO2 | 镁条始终无明显变化 |
4.先加入4mL饱和Na2SO3溶液,再充满CO2 | 镁条始终无明显变化 |
5.先加入2mL蒸馏水,再通入约4mL CO2 | 镁条第3天开始变黑,至第20天全部变黑 |
[解释与结论]①实验1的目的是_;②实验3中,试管内气体主要含CO2和__;③得出“镁条变黑一定与CO2有关”结论,依据的两个实验是___(填序号);④由上述实验可知,镁条变黑的条件是__。
[反思与评价]①在猜想假设时,同学们认为镁条变黑与N2无关,理由是_____;
②实验1和实验2中,NaOH浓溶液的作用是__;③欲进一步证明镁条表面的黑色物质中含有碳酸盐,你的实验方案是__。