题目内容
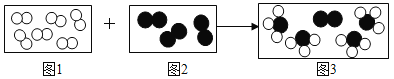
【题目】某探究小组的同学通过查阅资料得知:在加热条件下,镁不仅能与水反应还能与氯化铵溶液反应。小组同学对此产生兴趣,他们将砂纸打磨过的镁条加入氯化铵溶液中并加热,迅速产生大量气体。为确定生成气体的成分,他们进行如下探究:
(查阅资料)(1)镁与氯化铵溶液反应生成两种气体,每种气体只含有氮、氢两种元素中的一种或两种;
(2)镁与水在加热条件下反应生成氢氧化镁和氢气;
(3)氨气是一种极易溶于水的气体,能与酸反应。
(提出问题)该气体成分是什么?
(作出猜想)猜想一:H2和 N2
猜想二:N2和 NH3
猜想三:__________
(实验探究)
步骤一:小组同学闻气体气味,发现该气体有刺激性气味。则猜想_____________不成立。
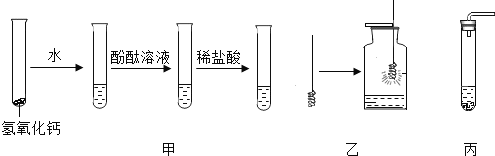
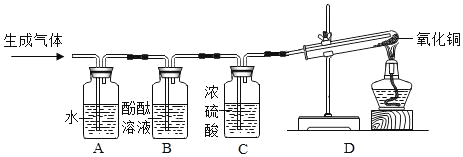
步骤二:同学们把产生的气体通入盛有水的 A 装置中除去___________,再将剩余气体依次通入 B、C、D 装置中,一会儿后,加热试管中的氧化铜,观察到 B 中溶液不变色,C 中无明显现象,D 中黑色粉末变成红色固体,试管口有小水珠。装置 C 的作用是____________(合理即可),装置 D 中发生反应的化学方程式为__________。
(得出结论)猜想________________成立。
【答案】H2和NH3 一 氨气 除去气体中的水分 H2+ CuO![]() Cu+ H2O 猜想三
Cu+ H2O 猜想三
【解析】
[做出猜想]猜想二:由于每种气体只含有氮、氢两种元素中的一种或两种,猜想该气体
的成分还可能是H2和NH3 ,故填:H2和NH3。
[进行实验]步骤一:由于该气体有刺激性气味,而H2和N2均无气味,故猜想一不成立;步骤二:由步骤一知该气体中含氨气,在根据氨气极易溶于水性质,利用盛有水的A装置可
将其除去;装置B中溶液不变色,说明氨气已经除尽,装置C中装有浓硫酸,浓硫酸具有吸水性,可将生成气体中含有的水分除去;因为D中黑色粉末变成红色固体,试管口有小水珠,知D中的氧化铜被氢气还原成铜,发生反应的化学方程式为:H2+ CuO![]() Cu+ H2O,故填:一;氨气;除去气体中水分;H2+ CuO
Cu+ H2O,故填:一;氨气;除去气体中水分;H2+ CuO![]() Cu+ H2O。
Cu+ H2O。
[得出结论]因为生成的气体具有刺激性气味,知该气体中含氨气,由于该气体又具有还原性,该气体中含氢气,故得出结论猜想三,正确,故填:猜想三。

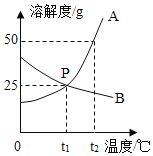
【题目】NH4C1和Na2SO4的溶解度表及溶解度曲线如下。下列说法正确的是( )
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度S/g | NH4C1 | 3.33 | 37.2 | 41.4 | 45.8 | 50.4 | 60.2 |
Na2SO4 | 9.6 | 20.2 | 40.8 | 48.4 | 47.5 | 47.0 | |
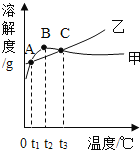
A.甲为NH4C1的溶解度曲线
B.两种物质的溶解度均随温度升高而增大
C.甲、乙饱和溶液从t3降温到t2,溶质的质量分数都变小
D.等质量的甲、乙饱和溶液从t1升温到t3,为使其溶液恰好饱和,加入的甲、乙固体质量相等