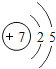题目内容
【题目】原子结构与元素的性质和物质的组成密切相关,请将答案填写在下面的横线上:
(1)镁原子的结构示意图为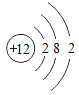 ,其在化学反应中易_________(填“得到”或“失去”)电子,其离子符号是___________。
,其在化学反应中易_________(填“得到”或“失去”)电子,其离子符号是___________。
(2)钠元素与氯元素组成的化合物是_________(化学式),构成该物质的微粒是_______(选填“分子”、“原子”、或“离子”);
(3)与元素化学性质关系最密切的是_________(填字母编号);
A 元素的相对原子质量 B 元素的核电荷数
C 原子的核外电子数 D 原子的最外层电子数
(4)金刚石、石墨都是由碳元素组成,它们的化学性质相似,物理性质却有很大差异。其原因是_______(填字母编号)。
A 构成它们的原子大小不同 B 构成它们的原子数目不同
C 金刚石、石墨由不同种原子组成 D 金刚石、石墨里碳原子排列方式不同
【答案】失去 Mg2+ NaCl 离子 D D
【解析】
(1)根据镁原子的结构示意图可知,其最外层电子数为2,在化学反应中易失去电子,带两个单位的正电荷,其离子符号为Mg2+。
(2)钠元素常见化合价为+1价,与氯元素化合时,氯元素显负价,氯元素常见的负价为-1价,则这两种元素组成的化合物的化学式为NaCl,构成氯化钠的微粒是离子,它是由钠离子和氯离子构成的;
(3)与元素化学性质关系最密切的是原子的最外层电子数,最外层电子数大于4时,在反应中易得到电子,最外层电子小于4时,在反应中易失去电子。故选D。
(4)金刚石、石墨都是由碳元素组成,它们的化学性质相似,物理性质却有很大差异。其原因是碳原子排列方式不同,金刚石中的碳原子呈立体网状结构,而石墨中的碳原子是平面片层状结构,导致它们的物理性质有很大差异。故选D。

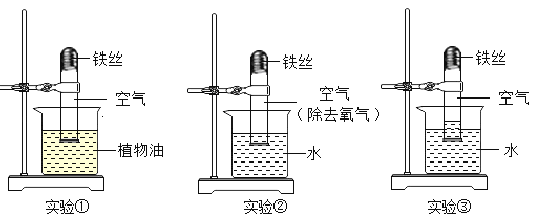
【题目】2012年1月,广西河池宜州市境内龙江河发生了镉浓度超标事件。根据该事件某化学活动小组开展了一次关于金属镉与铜、银活动性顺序的探究及镉污染事故处理方法的研讨活动。
查阅资料:①镉(Cd)是一种银白色金属,在化合物中通常表现为+2价 ②水体中镉元素通常以氯化镉的形式存在 ③氯化镉能溶于水,氢氧化镉难溶于水
(一)金属镉与铜、银活动性顺序的探究
实验步骤 | 实验现象 | 实验结论 |
取适量镉、铜、银于试管中,加入足量 | 镉表面有气泡产生,铜、银表面无气泡产生 | 镉的活动性顺序大于铜与银 |
取适量铜于试管中,加入少量硝酸银溶液 | , | 铜的活动性顺序大于银 |
实验结论:活动性顺序:镉>铜>银
(二)对镉污染事故处理方法的讨论
小聪认为可用向受污染河段抛撒过量烧碱固体的方法除去氯化镉,反应原理用化学方程式表示为 。小敏认为该方案虽然有效,但有缺陷,原因是 。受小聪与小敏启发,你认为可以用 (写俗称)代替烧碱。
【题目】实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如右图),为确认其中的溶质,同学们进行了如下的探究活动。请你参与到其中去,回答有关问题。

【进行猜想】猜想Ⅰ:该溶液的溶质是NaCl;
猜想Ⅱ:该溶液的溶质是NaOH;
猜想Ⅲ:该溶液的溶质是Na2CO3;
猜想IV:该溶液的溶质是NaHCO3.
【查阅资料】常温下物质的相关信息如下表:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下稀溶液的pH | 7 | 13 | 11 | 9 |
从物质的相关信息可知,该溶液的溶质不是NaHCO3,因为常温下NaHCO3溶液溶质的质量分数最大是
(精确到01.%)。
【进行实验】
(1)测定溶液的pH大于7,该溶液的溶质不是 (填化学式)。
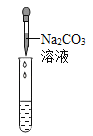
(2)同学们又进行了如下实验,实验过程如下:

①产生白色沉淀的化学方程式是 。
②实验可以判断原无色溶液中含有的溶质有 。
【获得结论】
该瓶原来装的无色溶液的溶质是NaOH,并且 (填“没有”、“部分”或“全部”)变质。
【拓展】
提纯该无色溶液的步骤是:先向无色溶液中加入适量的 ,然后过滤。反应化学方程式是 。
【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动。以下是教学片段,请你参与学习并帮助填写空格(包括表中空格)。
(演示实验)将一定量的稀H2SO4加入盛有NaOH溶液的小烧杯中。
(学生板演)该反应的化学方程式________________。
(提出问题)实验未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么?
(猜想假设)针对疑问,大家纷纷提出猜想。甲组同学的猜想如下:猜想一:只有Na2SO4;猜想二:有____________ ;猜想三:有Na2SO4和NaOH;猜想四:有Na2SO4、H2SO4和NaOH。乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的。不合理的猜想及其理由是_________。
(实验探究)
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有____________。
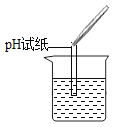
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaCl2溶液、Na2CO3溶液,进行如下三个方案的探究。
实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
实验操作 |
|
|
|
实验现象 | 试纸变色,对比比色卡,pH____7(选填“>”“<”或“=”) | _________ | 产生白色沉淀 |
实验结论 | 溶液中有H2SO4 | 溶液中有 H2SO4 | 溶液中有H2SO4 |
(得出结论)通过探究,全班同学一致确定猜想二是正确的。
(评价反思)老师对同学们用多种方法进行探究,并得出正确结论给予肯定。同时指出实验探究(2)中存在两处明显错误,请大家反思。同学们经过反思发现了两处错误:
(1)实验操作中的错误是 __________________ 。
(2)实验方案中有一个是错误的,写出能说明实验方案错误原因的化学方程式是 _______________。