题目内容
【题目】某气体可能由初中化学中常见的一种或多种气体组成,经测定其中只含有碳、氧两种元素,质量比为1:2,则关于该气体的正确说法是( )
A. 一定是纯净物
B. 一定是CO和CO2的混合物
C. 该气体最多的可能组成的2种
D. 该气体最多的可能组成有3种
【答案】D
【解析】
碳、氧两种元素可形成的初中化学常见的气体为一氧化碳、二氧化碳和氧气,而混合气体中碳、氧元素的质量比正处于一氧化碳与二氧化碳两气体之间。
根据题意,混合气体中碳、氧两元素的质量比为1:2,而CO2中碳、氧元素质量比为3:8,因此不可能只含有二氧化碳;而CO中碳、氧元素质量比为3:4,因此也不可能只含有CO气体;![]() 故混合气体可能为一氧化碳与氧气、一氧化碳与二氧化碳两种气体的混合物,也可能是一氧化碳、二氧化碳、氧气三种气体的混合物;若是二氧化碳和氧气的混合物,则碳氧元素质量比会小于
故混合气体可能为一氧化碳与氧气、一氧化碳与二氧化碳两种气体的混合物,也可能是一氧化碳、二氧化碳、氧气三种气体的混合物;若是二氧化碳和氧气的混合物,则碳氧元素质量比会小于![]() ,故选D。
,故选D。

【题目】下列化学方程式与对应反应类型均正确的是( )
化学方程式 | 反应类型 | |
A | H2O | 分解反应 |
B | 4Al+3O2=2Al2O3 | 化合反应 |
C | 2Fe+6HCl═2FeCl3 +3H2↑ | 置换反应 |
D | CO2 +2NaOH ═Na2CO3+H2O | 复分解反应 |
A. AB. BC. CD. D
【题目】“高质发展,后发先至”是连云港新一轮发展的主线,我市濒临黄海,拥有丰富的海洋资源。
(1)食用海鱼、海虾等海鲜可为人体提供的营养素主要是_____(填序号)
A 糖类 B 蛋白质 C 维生素 D 油脂
(2)从海水中获得粗盐的方法是采用蒸发结晶,而不是降温结晶,理由是_____;
(3)用氯化钠固体配制 100g 质量分数为 10%的氯化钠溶液。若测得所配制溶液的溶质质量分数偏小,其 原因可能是_____(填序号)。
A 氯化钠固体不纯 B 量取水时,俯视读数
C 溶解时,烧杯内壁有水 D 装瓶时,有少量溶液洒出
(4)某浓度的海水中主要离子的浓度如下:
离子 | Na+ | Mg2+ | Cl﹣ | SO 42﹣ |
浓度/g/L | 63.7 | 28.8 | 144.6 | 46.4 |
①从海水中提取 MgCl2,将 MgCl2 溶液在一定条件下蒸发结晶、熔融电解可制得金属镁,则 2L 该浓度的 海水理论上可得到金属镁的质量为_____g;
②将一定量的镁粉加入到适量硝酸亚铁和硝酸银的混合溶液中,充分反应后过滤,得到滤液和滤渣。取少 量滤液,加入稀盐酸溶液,无明显现象,则滤液中一定没有_____;取少量滤渣,加入足量稀盐酸, 有气泡产生,则滤渣中一定含有_____;
③净化水常用的方法有沉降、过滤、吸附和蒸馏,活性炭在净水器中能起到过滤和吸附的作用,这是由于 活性炭具有_____结构。
④电解水实验揭示了水的组成(如下图)。
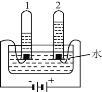
电解水的反应方程式为__________________, 实验过程中可加入稀硫酸以增强导电性,实验结束后,溶液 pH 将_______(填“增大”、 “减小”或“不变”)。
(5)常温下,氯酸钾的溶解度较小,在工业上可通过如下转化制得。
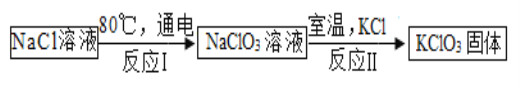
①实验室用氯酸钾制取氧气的化学方程式为_____ ;
②反应Ⅰ中,是将_____能转化成化学能;
③反应Ⅱ的基本反应类型为复分解反应,请写出反应方程式_____;
④该工业转化中可以循环利用的物质是_____ 。
【题目】下列实验操作能够达到实验目的是
序号 | 实验目的 | 主要操作 |
A | 鉴别加碘食盐和无碘食盐 | 各取少量样品,加入淀粉溶液,观察 |
B | 检验 | 将气体通入紫色石蕊试液,观察 |
C | 除 | 加入稀盐酸,充分溶解后,过滤 |
D | 除去氯化钠固体中的少量碳酸钠 | 加入适量稀盐酸,充分反应后,蒸发 |
A. AB. BC. CD. D