题目内容
【题目】多角度认识 “二氧化碳与氢氧化钠溶液”的反应。
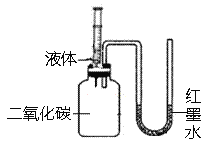
(1)从反应物角度如图所示,甲同学往集气瓶内注入氢氧化钠溶液,U型管右边液面________(填“升高”或“降低”),他认为二氧化碳和氢氧化钠发生反应。乙同学认为还须将针筒内液体换成_______(写物质名称)进行对比实验,才能说明二者发生反应。二氧化碳和氢氧化钠反应的化学方程式为___________________________________。
(2)从生成物角度
① 丙同学认为可用酚酞溶液验证二者发生反应,该方法_______(填“可行”或“不可行”),原因是_________________________________________。
② 丁同学建议,往反应后的溶液中滴加氯化钡溶液,观察到___________现象,该反应的化学方程式为_____________________,因此说明二氧化碳和氢氧化钠发生反应。
戊同学将氯化钡溶液换成不同类别的物质也能达到目的,该物质是___________(写化学式)。
【答案】 降低 水 CO2 + 2NaOH == Na2CO3 + H2O 不可行 氢氧化钠和碳酸钠溶液都呈碱性,都能使酚酞溶液变红色 白色沉淀 Na2CO3 + BaCl2 == BaCO3↓ + 2NaCl Ca(OH)2(或HCl合理均可)
【解析】本题主要考查碱的化学性质,盐的化学性质。可根据碱的化学性质,盐的化学性质分析。
(1)氢氧化钠与二氧化碳反应生成碳酸钠和水,二氧化碳减少,气压变小,U型管右边液面下降,氢氧化钠溶液中含有水,水也能与二氧化碳反应,所以做对比实验要成水,故填:下降 水 CO2 + 2NaOH == Na2CO3 + H2O
(2)①氢氧化钠与二氧化碳反应生成碳酸钠和水,氢氧化钠和碳酸钠溶液都是碱性,酚酞都变红色。所以不能用酚酞。故填:不可以 氢氧化钠和碳酸钠溶液都呈碱性,都能使酚酞溶液变红色
②氢氧化钠与二氧化碳反应生成碳酸钠和水,反应后的溶液中含有碳酸钠,滴加氯化钡与碳酸钠反应生成碳酸钡沉淀,故现象:白色沉淀 化学方程式:Na2CO3 + BaCl2 == BaCO3↓ + 2NaCl
碳酸钠与含钙的碱或盐都能反应生成沉淀,故可使用氢氧化钙或氯化钙。故填:氢氧化钙。

【题目】某石油化工厂化验室的实验员用15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,测得实验数据如表:
实验序号 | 消耗NaOH溶液的质量 | 洗涤后溶液的pH |
① | 30g | pH<7 |
② | 40g | pH=7 |
③ | 50g | pH>7 |
请回答下列问题:
(1)欲计算出一定量石油产品中所含H2SO4的质量,你觉得应该选择实验序号 的数据。
(2)若一定量石油产品中残余硫酸的质量为100g,请计算该残余硫酸的溶质质量分数(写出详细的计算过程)。