题目内容
【题目】金属具有广泛的应用。
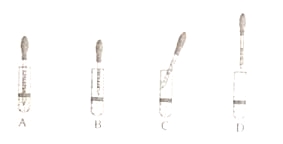
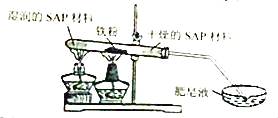
(1)下列金属制品中,利用金属导热性的是________(填字母)。

(2)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成,不能用铁质容器配制波尔多液的原因是__________________________________________(用化学方程式表示)。
(3)防止金属锈蚀是保护金属资源的有效途径之一。洁净的铁钉在下列情况下容易生锈的是________(填字母)。
A.在干燥的空气中
B.在潮湿的空气中
C.浸没在植物油中
(4)铝具有良好的抗腐蚀性能,原因是铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化。氧化铝难溶于水,却能溶于酸。写出氧化铝与稀硫酸反应生成硫酸铝和水的化学方程式:____________________________________________。
(5)向铁粉和氧化铜粉末的混合物中加入一定量的稀硫酸,微热,充分反应后过滤,得滤渣和滤液,向滤液中加一洁净铁片,未看到铁片有任何变化。则滤液中含有的溶质是______________(填化学式,下同),滤渣中一定含有的物质是__________。
【答案】 C Fe+CuSO4===FeSO4+Cu B Al2O3+3H2SO4===Al2(SO4)3+3H2O FeSO4 Cu
【解析】试题分析:
(1)铜制火锅是利用金属导热性;
(2)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成,不能用铁质容器配制波尔多液的原因是铁比铜活泼,能将铜从其溶液中置换出来,反应的化学方程式是:Fe+CuSO4= FeSO4 +Cu:
(3)铁生锈的条件是能与水、氧气接触,洁净的铁钉在潮湿的空气中容易生锈;
(4)氧化铝与稀硫酸反应生成硫酸铝和水,反应的化学方程式是:Al2O3+3H2SO4=Al2(SO4)3+3H2O。
(5)向铁粉和氧化铜粉末的混合物中加入一定量的稀硫酸,微热,铁与稀硫酸反应生成了硫酸亚铁和氢气,氧化铜能与稀硫酸反应生成了硫酸铜和水,铁能与硫酸铜反应生成了硫酸亚铁和铜。过滤得滤渣和滤液。向滤液中加一洁净铁片,未看到铁片有任何变化,说明了硫酸铜和稀硫酸完全反应了,则滤液中含有的溶质是FeSO4,滤渣中一定含有的物质是Cu。

 名师指导期末冲刺卷系列答案
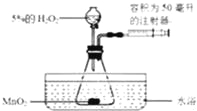
名师指导期末冲刺卷系列答案【题目】小金为了探究温度对H2O2分解反应速率的影响,借助如图所示实验装置(夹持装置略去),进行了两次实验,两次实验的部分设计如表所示:
实验1 | 实验2 | |
MnO2的质量/克 | 0.5 | 0.5 |
5%的H2O2的体积/毫升 | 40 | 待填 |
水浴温度/℃ | 20 | 80 |
(1)实验2中应加入5%H2O2 毫升。
(2)在两次实验中,可通过 来比较H2O2分解反应速率的大小。
(3)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因除锥形瓶内气体受热膨胀外,还有 。
(4)实验结束后若要将MnO2从混合物汇总分离出来,可采取的方法是 。