��Ŀ����
����Ŀ��������ճ�����������벻��ˮ��
��1������Ӳ�Ȼ����ȹ����ˮ�����������彡���������п�ͨ��_____����������ˮ��Ӳ�ȡ���ʵ�����ﳣ��_____���ⶨˮ�����ȣ�
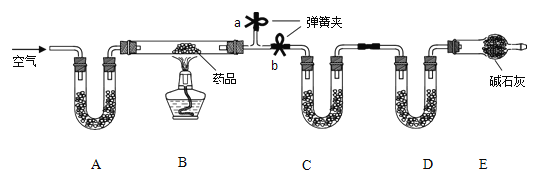
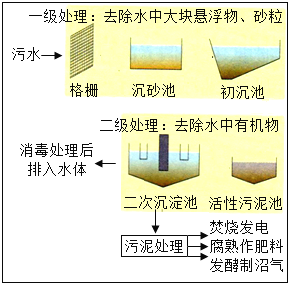
��2����ͼΪij����ˮ��������ʾ��ͼ��ˮͨ������դ����ȥ���ϴ�������Ư����൱�ڻ���ʵ������е�_____��������������_____��ѡ���������ѧ�����仯�������������ij��ɫ��ˮ���к��м��Σ�֤����ˮ��Ϊ�����ķ�����_____��д������������
��3�����ٲ���ˮ�������ض���������������õ�H+��OH����H+����ˮ�����γ�ˮ�������� ��H3O+������ˮ������ȣ����ж�ˮ����������������������_____������ĸ��ţ�
A ��Ԫ�صĻ��ϼ۷����˸ı�
B ���Ĺ��ɷ����˸ı�
C ���Ļ�ѧ���ʷ����˸ı�
D ���ĵ����������˸ı�
���𰸡�������� pH��ֽ ���� ��ѧ ��ˮ���������������ְ�ɫ���� AD
��������
��1������������ͨ��������У���ʵ��������ͨ������ķ�������ˮ��Ӳ�ȣ���ʵ�����ﳣ��pH��ֽ���ⶨˮ�����ȡ�
��2����ͼΪij����ˮ��������ʾ��ͼ��ˮͨ������դ����ȥ���ϴ�������Ư����൱�ڻ���ʵ������еĹ��ˣ������������ڻ�ѧ�仯��������ˮ����������Ϊˮ�����������м��ε�ˮ��������������ְ�ɫ���塣
��3��A ˮ������������Ԫ�صĻ��ϼ���Ϊ-2�����ϼ۲��䣬��ѡ�����
B һ��ˮ������������ԭ�Ӻ�һ����ԭ�ӹ��ɣ���һ��ˮ����������������ԭ�Ӻ�һ����ԭ�ӹ��ɣ����Ĺ��ɷ����˸ı䣬��ѡ����ȷ��
C ���Ľṹ�����˸ı䣬�������Ļ�ѧ���ʷ����˸ı䣬��ѡ����ȷ��
D H+����ˮ�����γ�ˮ�������� ��H3O+��ʱ�����ĵ��������䣬��ѡ�����ѡAD��

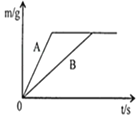
����Ŀ��ʵ��С���ͬѧ��ȡ30gij������Ʒ��ƽ���ֳ��������μ��뵽ʢ��100gϡ�������ƿ�У���ƿ������Ϊ60g����ÿ�γ�ַ�Ӧ����г�������ͼ��ʾ�����õ����������

��1�� | ��2�� | ��3�� | ��4�� | ��5�� | ��6�� | |
������Ʒ ������/g | 5 | 5 | 5 | 5 | 5 | 5 |
������ƽ ��ʾ��/g | 163.9 | 167.8 | 171.7 | 175.6 | 180.6 | 185.6 |
����㣺
��1�������μ�����Ʒ���ܹ����ɵĶ�����̼������_____g��
��2��������Ʒ��̼���Ƶ�����������_____��
����Ŀ��ij��ѧ��ȤС����һ��ʵ���з���þ���ƶ����ڴ����Ķ�����̼������ȼ�գ���Ӧ����ȴ��ƿ�׳����к�ɫ������ƿ���ϻ������Ű�ɫ���ʡ������飬��ɫ������̼�����Ƕ�þ�����ڶ�����̼������ȼ�պ����ɵİ�ɫ���ʷֱ����������̽����
��̽������һ��þ�ڴ����Ķ�����̼��ȼ�����ɵİ�ɫ������ʲô��
ͬѧ�������ų�����Mg(OH)2�Ŀ����ԣ�������_____��
���������룩��ɫ��������Ǣ�MgO����MgCO3����_____��
������ʵ�飩ȡ������ɫ���壬����������ϡ���ᣬ�۲쵽_____���������ȷ��
��ʵ����ۣ�þ�ڶ�����̼��ȼ�յĻ�ѧ����ʽ��_____��
��̽������������ڴ����Ķ�����̼��ȼ�����ɵİ�ɫ������ʲô��
���������ϣ���Ϣ1����������ˮ�������ҷ�Ӧ��
��Ϣ2��Na2O+H2O=2NaOH
��ʵ����ƣ����鷽����
ʵ�鲽�� | ʵ������ | ���� |
ȡ������ɫ�������Թ��У���ˮ�ܽ⣬��������Ba(OH)2��Һ | _____ | ��ɫ��������Na2CO3 |
���ú����ϲ���Һ�μӷ�̪��Һ | ��Һ��� | ��ɫ��������Na2O |
������ۣ���ɫ����ΪNa2O��Na2CO3�Ļ����
���鷽����
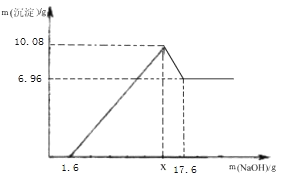
ȡ5.3�˰�ɫ������Ʒ�������в�����
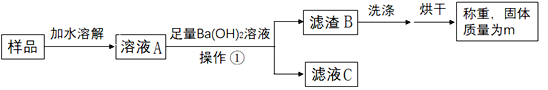
��1����������_____��
��2��Ba(OH)2��Һ����������Ŀ����_____��
����ͬѧ���m=9.85�ˣ������Ʒ�������з��������յó����ۣ���ɫ����ΪNa2CO3��
��ʵ�鷴˼��
��1��Ϊ�μס����������ý��۲������ijͬѧ������ָ�����鷽������ѧ��Ӧ�ý����鷽���е�Ba(OH)2��Һ��Ϊ_____��Һ�ź�����
��2�����ڶ�����̼��ȼ�յĻ�ѧ����ʽΪ_____��
����չӦ�ã�
ʵ�������ƵȽ�����ȼ����������ʱ������ѡ������ʽ��_____��
A����ˮ���� B����Һ̬������̼����� C����ɳ������
����Ŀ��ѧ�������֮��С��ͷ����һֱ���ɻ�Ϊʲô��ʦ˵�����˳����мء��ơ��ƺܻ��ã�ȴ�ֲ��ܰ����������������Һ���û������أ���������С���߽���ʵ���ҡ�
���������ϣ�����һ�ֻ��ý���������������������ˮ�����ʷ�����Ӧ������ˮ��Ӧ�Ļ�ѧ����ʽΪ2Na+2H2O��2NaOH+H2����
��ʵ��̽����С����ȡһ����������ͭ��Һ���ձ��У���ȡһС����Ͷ������ͭ��Һ�У���Ӧ���ȣ���ַ�Ӧ����ˣ��õ���Һ����ɫ������������ѧ֪ʶ���ƶ���ɫ����Ϊ������Һ�ijɷֽ���̽����
����������裩����һ��Na2SO4���������Na2SO4��NaOH��������_____�������ģ�Na2SO4��CuSO4��NaOH
С����Ϊ����_____��������������_____���û�ѧ����ʽ��ʾ����
���������ϣ�Na2SO4��Һ������
��ʵ������֤��
ʵ�� | ʵ����� | ʵ������ | ʵ����� |
ʵ��һ | ȡ������Һ���Թ��У���ϸ�۲����� | ��ҺΪ��ɫ | ����_____������ |
ʵ��� | ��ʵ��һ��ȡ��Һ�е����̪��Һ | _____ | ����һ������ |
����չ���죩�������˳������Ƽ�ǰ��Ľ���ȷʵ_____������������������������λ�ں���Ľ�������������Һ���û�������
������̽����С����4.6g��Ͷ�뵽��HCl 3.65g��ϡ�����У���Ӧ���Ӿ��ȣ�������Ϊ�Ƶ����ʺܻ��ã�������ʧȥ������һ�����Ӷ��γ�_____�������ù����в���H2������_____��