题目内容
【题目】化学实验能够从视觉直观的角度让我们发现化学变化的神奇,激发我们学习兴趣。请大家根据实验回答问题:
(一)教材实验集锦
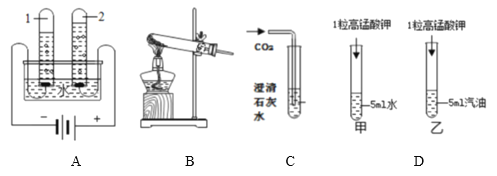
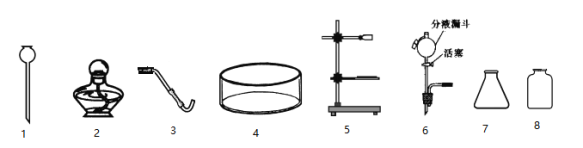
(1)A实验的试管1中产生的气体是_______
(2)B用于制取氧气,反应的化学方程式为_______
(3)C中观察到实验现象是__________________,该反应可用来_______
(4)D实验得到的结论是_______
(二)教材实验拓展
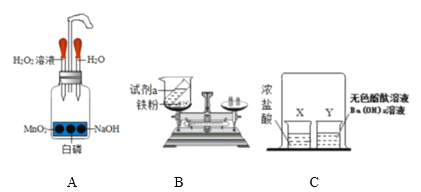
(1)课外小组的同学自制一块多槽铁板,设计如图A所示装置,用以探究燃烧的条件。(说明:金属板上白磷足量)。请回答下列问题
①证明可燃物燃烧需要一定温度的依据是_______
②将过氧化氢溶液滴入盛有MnO2的金属槽中,发生反应的化学方程式_______
③有同学提出“将NaOH换成水,然后将水换成浓硫酸,也可以完成探究活动",你认为可行吗,为什么?_______
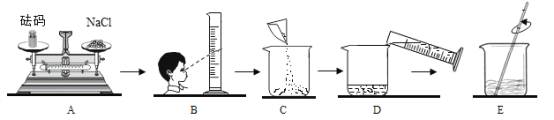
(2)如图B所示的装置进行验证质量守恒定律,试剂a可以是__________(写出一种即可)。证明质量守恒定律成立的现象是_______
(3)根据如图C所示实验,Y烧杯中溶液由红色变为无色。
①该实验可证明微粒具有的性质是__________。
②请用化学方程式表示红色变为无色的原因_______
③该实验得出氢氧化钡的化学性质有_______
【答案】H2 2KMnO4![]() K2MnO4 +MnO2 + O2↑ 变浑浊 检验二氧化碳 同种溶质在不同溶剂中溶解性不同 将胶头滴管的水滴入氢氧化钠前白磷不燃烧,滴入后白磷燃烧 2H2O2
K2MnO4 +MnO2 + O2↑ 变浑浊 检验二氧化碳 同种溶质在不同溶剂中溶解性不同 将胶头滴管的水滴入氢氧化钠前白磷不燃烧,滴入后白磷燃烧 2H2O2![]() 2H2O + O2↑ 不可行,浓硫酸稀释为稀硫酸后会与铁板反应 CuSO4溶液(能与铁反应且不生成气体合理即可) 铁表面有紫红色固体生成,溶液由蓝色变为浅绿色,天平仍保持平衡 微粒在不断运动 Ba(OH)2+2HCl =BaCl2+2H2O 碱性,能使无色酚酞变红,能与盐酸发生反应
2H2O + O2↑ 不可行,浓硫酸稀释为稀硫酸后会与铁板反应 CuSO4溶液(能与铁反应且不生成气体合理即可) 铁表面有紫红色固体生成,溶液由蓝色变为浅绿色,天平仍保持平衡 微粒在不断运动 Ba(OH)2+2HCl =BaCl2+2H2O 碱性,能使无色酚酞变红,能与盐酸发生反应
【解析】
(一)(1)电解水产生氢气、氧气,氢气的体积是氧气体积的2倍,A实验的试管1中产生的气体较多,是氢气。
(2)加热固体制取氧气,且试管口放了一团棉花,则是用高锰酸钾制取氧气,反应的化学方程式为:2KMnO4 ![]() K2MnO4 + MnO2 + O2↑。
K2MnO4 + MnO2 + O2↑。
(3)二氧化碳能使澄清石灰水变浑浊,C中可观察到澄清石灰水变浑浊,该反应可用来检验二氧化碳。
(4)由实验可知,高锰酸钾能溶于水,不能溶于汽油,D实验得到的结论是同种溶质在不同溶剂中溶解性不同。
(二)(1)①氢氧化钠溶于水放出热量,将水滴入氢氧化钠前,白磷不燃烧,滴入后白磷燃烧。②过氧化氢溶液在MnO2作催化剂的条件下,发生反应生成水、氧气。③不可行,浓硫酸稀释为稀硫酸,稀硫酸能与铁板反应。
(2)有气体参加或生成的反应来验证质量守恒定律,必须在密闭容器中进行,而如图B所示的装置是在敞口容器中进行的,所以实验过程中不能有气体,要进行验证质量守恒定律,试剂a可以是CuSO4,Fe+CuSO4=Cu+FeSO4,所以实验现象是铁表面有紫红色固体生成,溶液由蓝色变为浅绿色,天平仍保持平衡。
(3)①酚酞遇碱性溶液变红,Y烧杯中溶液由红色变为无色,表示溶液不是碱性了,说明X烧杯中的物质与Y烧杯中的物质发生了反应。没有直接接触却发生了反应,说明微粒在不断地运动。②Y烧杯中的液体由红色变为无色,是由于从X烧杯中挥发出来的氯化氢气体运动到Y烧杯中,与氢氧化钡溶液发生了化学反应,Ba(OH)2+2HCl =BaCl2+2H2O。③该实验得出氢氧化钡的化学性质是:氢氧化钡显碱性、能使酚酞试液变红、能与盐酸反应。

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案