题目内容
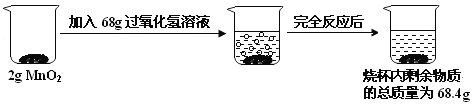
【题目】某学习小组对人体吸入的空气与呼出的气体,进行了如下探究
(提出问题)人体吸入的空气与呼出的气体组成有什么不同?
(查阅资料)(1)通常条件下,红磷的着火点为240℃,白磷的着火点为40℃。
(2)白磷与氢氧化钠溶液不反应。
(3)氢氧化钠溶液与澄清石灰水的性质相似,能与某些气体反应。
(4)金属铝能与氢氧化钠溶液反应 2Al+2NaOH+2H2O=2NaAlO2+3H2↑
(实验操作、记录、分析)
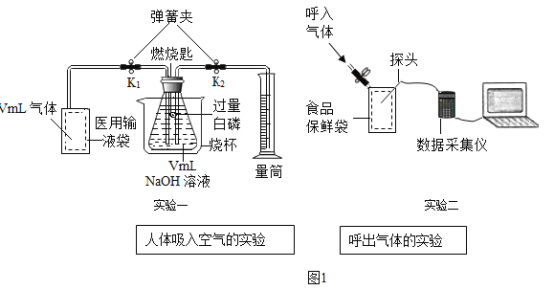
实验一:
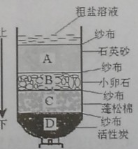
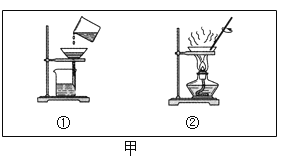
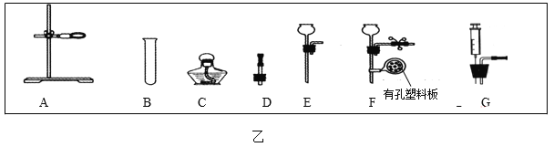
(1)先检查装置的_____,在锥形瓶中装入VmL氢氧化钠溶液,在医用输液袋中装入VmL人体吸入的空气
(2)打开弹簧夹K1、K2,缓慢将袋中的气体全部排除。读出量筒(量筒的容积远大于VmL)中液体体积为amL.请根据所学知识,在该步实验中,空气中某气体与氢氧化钠反应的化学方程式_____。
(3)关闭弹簧夹K1、K2,再_____(填操作方法),以促使白磷迅速燃烧。 燃烧的化学方程式为_____,能否使用红磷_____(填‘行’还是‘不行’)。待瓶中气体冷却至室温,打开K2.读出量筒中液体体积为bmL.从而推断该气体占气体总体积百分数约为_____(用字母表示)。
实验二:
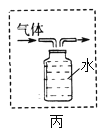
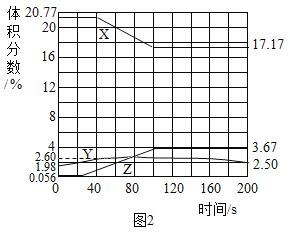
(4)把氧气、二氧化碳、水蒸气(测湿度)探头放入袋中,开始采集数据,然后向袋内呼出气体。采集的数据经处理如图2,图中曲线表示氧气体积分数变化的是_____(填“X”、“Y”、“Z”)。根据表格中曲线及相关数据,请解释寒冷冬天,紧闭教室内窗户玻璃上能用手指写出清晰的字_____,实验二中,200s时若体积为Vml食品保鲜袋中没有采集数据的所有气体的总体积约为_____mL。
(评价反思)
(5)通过实验一和实验二,同学们想想:人体吸入空气和呼出气体组成对比的结论是_____。
(6)实验一中把盛放白磷的铁质燃烧匙换为镁带缠绕。假设实验能安全进行完毕,请猜想实验结束后的呈现的现象是_____。
(7)连接装置前把铁质燃烧匙换为铝质的,则可能后果是_____,原因是_____。
(8)为使实验一的数据更精确,结合实验一和实验二思考,你有何建议?_____。
【答案】气密性 CO2+2NaOH=Na2CO3+H2O 向烧杯中加入热水(热水温度大于40°C) 4P+5O2![]() 2P2O5 不行
2P2O5 不行 ![]() ×100% X 寒冷冬天,室外温度低,教室内的水蒸气在玻璃上冷凝成液态的水 76.66%V 呼出气体中二氧化碳和水蒸气体积分数增大,氧气体积分数减少 镁与空气中氧气、二氧化碳、氮气均要反应,量筒中水倒吸入锥形瓶中,几乎充满 锥形瓶炸裂或胶塞被冲出 铝与氢氧化钠溶液反应生成氢气,氢气与氧气混合遇明火而发生爆炸性反应 使用实验二的数据采集器整套装置,测得的数据更精确
×100% X 寒冷冬天,室外温度低,教室内的水蒸气在玻璃上冷凝成液态的水 76.66%V 呼出气体中二氧化碳和水蒸气体积分数增大,氧气体积分数减少 镁与空气中氧气、二氧化碳、氮气均要反应,量筒中水倒吸入锥形瓶中,几乎充满 锥形瓶炸裂或胶塞被冲出 铝与氢氧化钠溶液反应生成氢气,氢气与氧气混合遇明火而发生爆炸性反应 使用实验二的数据采集器整套装置,测得的数据更精确
【解析】
氢氧化钠溶液易与二氧化碳反应生成可以溶于水的碳酸钠和水,磷与氧气在点燃的条件下反应生成五氧化二磷,铝与氢氧化钠溶液反应生成氢气。
(1)实验前应先检查装置的气密性,在锥形瓶中装入VmL氢氧化钠溶液,在医用输液袋中装入VmL人体吸入的空气。
(2)氢氧化钠溶液易与二氧化碳反应生成可以溶于水的碳酸钠和水,锥形瓶中氢氧化钠溶液的作用是吸收气体中的二氧化碳,利用减少的液体体积测出二氧化碳的含量,减少的气体体积为(V﹣a)mL,这就是空气中二氧化碳的体积;二氧化碳与氢氧化钠反应生成碳酸钠和水;化学方程式为CO2+2NaOH=Na2CO3+H2O。
(3)关闭弹簧夹K1、K2,再向烧杯中加入热水(热水温度大于40°C),以促使白磷迅速燃烧。磷与氧气在点燃的条件下反应生成五氧化二磷,化学方程式为 此温度没有达到红磷的着火点,所以红磷不能燃烧;待瓶中气体冷却至室温,打开K2.量筒中的水倒吸,读出量筒中液休体积为bmL.量筒内液体减少的体积即为消耗的氧气的体积,即
此温度没有达到红磷的着火点,所以红磷不能燃烧;待瓶中气体冷却至室温,打开K2.量筒中的水倒吸,读出量筒中液休体积为bmL.量筒内液体减少的体积即为消耗的氧气的体积,即![]() ,从而推断该气体占气体总体积百分数约为
,从而推断该气体占气体总体积百分数约为![]() 。
。
(4)把氧气、二氧化碳、水蒸气(测湿度)探头放入袋中,开始采集数据(如图1),然后向袋内吹入气体,采集的数据经处理得到图3,由于呼出气体中二氧化碳增多和水蒸气增多,氧气减少,表示氧气体积分数变化的是X,寒冷冬天,室外温度低,教室内的水蒸气在玻璃上冷凝成液态的水,所以紧闭教室内窗户玻璃上能用手指写出清晰的字;由图示可知:由图表中的数据可知,200s时没有采集数据的其余气体的总体积为:
![]() 。
。
(5)人体的新陈代谢需要消耗氧气,同时产生二氧化碳,因此呼出气体中所含的氧气的含量比人体吸入空气中氧气含量低,二氧化碳的含量比人体吸入空气中的二氧化碳多;故呼出气体中二氧化碳和水蒸气体积分数增大,氧气体积分数减少。
(6)镁与空气中氧气、二氧化碳、氮气均要反应,量筒中水倒吸入锥形瓶中,几乎充满。
(7)铝与氢氧化钠溶液反应生成氢气,氢气与氧气混合遇明火而发生爆炸性反应,可能会导致锥形瓶炸裂或胶塞被冲出。
(8)由实验装置、实验数据可知,使用实验二的数据采集器整套装置,测得的数据更精确。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案【题目】依据下列![]() 时的实验和数据回答。已知
时的实验和数据回答。已知![]() 时,NaCl和NaNO3的溶解度分别为36g和88g。
时,NaCl和NaNO3的溶解度分别为36g和88g。
| 序号 |
|
|
|
|
|
固体种类 | NaCl | NaCl | NaNO3 | NaNO3 | NaNO3 | |
固体的质量 | 30 | 60 | 30 | 60 | 90 | |
水的质量 | 100 | 100 | 100 | 100 | 100 |
下列关于![]() 所得溶液的说法不正确的是
所得溶液的说法不正确的是![]()
![]()
A. 溶质质量:![]()
B. 溶液质量:![]()
C. 溶质质量分数:![]()
D. ![]() 中溶质与溶剂的质量比为9:10
中溶质与溶剂的质量比为9:10