题目内容
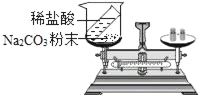
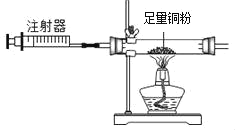
【题目】某化学兴趣小组欲测定一瓶过氧化氢溶液![]() 过氧化氢和水的混合物
过氧化氢和水的混合物![]() 中过氧化氢的质量,实验操作及相关数据如图所示:
中过氧化氢的质量,实验操作及相关数据如图所示:
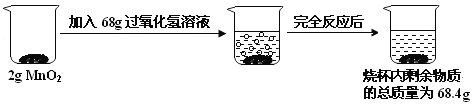
(1)生成氧气的质量______g,计算的依据是______
(2)这瓶过氧化氢溶液中过氧化氢的质量是_______?![]() 请根据方程式计算
请根据方程式计算![]()
【答案】1.6g 质量守恒定律 3.4g
【解析】
根据质量守恒定律可知,过程中质量的减少是因为生成了氧气,所以可以求算氧气的质量,根据氧气的质量和对应的化学方程式求算过氧化氢溶液中![]() 的质量。根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整。
的质量。根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整。
根据质量守恒定律可知,反应前后物质的总质量不变,生成的氧气的质量为![]()
设过氧化氢的质量为x

68/32=x/1.6g
X=3.4g
答:(1)生成氧气的质量![]() ,计算的依据是质量守恒定律;
,计算的依据是质量守恒定律;
(2)过氧化氢溶液中![]() 的质量为
的质量为![]() 。
。

【题目】某化学兴趣小组获得两包制作“跳跳糖”的添加剂,一包是柠檬酸晶体,另一包是标注为钠盐的白色粉末。将少量柠檬酸和这种白色粉末溶于水,混合后产生了使澄清石灰水变浑浊的气体,为确定白色粉末的化学成分,该小组进行了以下探究:
(提出猜想)猜想1.碳酸钠;猜想2.碳酸氢钠;猜想3.碳酸钠和碳酸氢钠。
(查阅资料)①碳酸钠溶液、碳酸氢钠溶液均呈碱性;
②碳酸氢钠受热分解生成碳酸钠、水和二氧化碳;碳酸钠受热不分解。
(实验探究1)小亮、小刚分别对有关猜想设计方案并进行实验
实验操作 | 实验现象 | 实验结论 | |
小亮 | 小亮将白色粉末溶于水后用pH试纸测定其酸碱度 | pH______(填“>”“<”或“=”)7 | 溶液呈碱性,猜想1成立 |
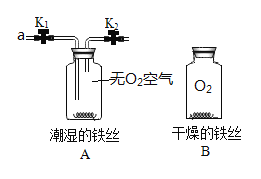
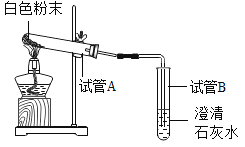
小刚 | 用如图所示的装置进行实验 | 试管A中有水珠产生,试管B中液体变___________。 | 猜想2成立,试管B中反应的化学方程式为__________。 |
(实验质疑)
(1)小红认为小亮的实验结论不正确,理由是____________(用文字叙述)。
(2)小明认为小刚的实验并不能得出猜想2成立,理由是______________(用文字叙述)。
(注意:若答对下列小题奖励4分,化学试卷总分不超过60分。)
(实验探究2)为了进一步确定白色粉末的化学成分,小戚称取10g白色粉末与足量稀盐酸反应,充分反应后生成二氧化碳的质量为mg,通过计算并分析实验数据确定猜想3成立,则m的取值范围为_______(计算结果用分数表示)
(结论分析)探究后他们查到该白色粉末的成分为碳酸氢钠,那么你认为白色粉末中的碳酸钠是如何产生的?写出产生碳酸钠的化学方程式_________。