题目内容
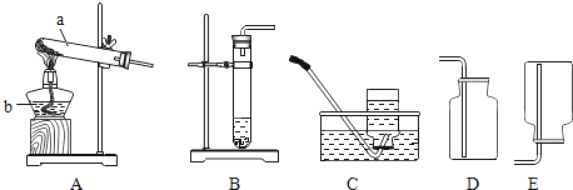
【题目】下图表示某些物质间转化关系。A是大理石的主要成分,C是气体,D是一种黑色的固态非金属单质;E由两种元素组成,其中D元素的质量分数为37.5%,与另一种元素原子个数之比为2:1;H是一种有刺激性气味的气体,M常用于制作糕点的发酵粉。

请回答下列问题。
(1)写出物质的化学式:D______,G_______。
(2)写出下列反应的化学方程式:①________________, ②________________。
(3)反应③能够发生的原因是____。
(4)此种塑料________(填“能”或“不能”)用于食品包装。
【答案】C NH4Cl CaCO3![]() CaO+CO2↑ CaC2+2H2O=C2H2 ↑ +Ca(OH)2 NaHCO3溶解度较小,结晶析出(或其他合理答案) 不能
CaO+CO2↑ CaC2+2H2O=C2H2 ↑ +Ca(OH)2 NaHCO3溶解度较小,结晶析出(或其他合理答案) 不能
【解析】
A是大理石的主要成分,A是碳酸钙,碳酸钙在高温的条件下生成氧化钙和二氧化碳,C是气体,所以C是二氧化碳,B是氧化钙;D是一种黑色的固态非金属单质,D可能是碳,碳与氧化钙反应生成E,E由两种元素组成,其中D元素的质量分数为37.5%,与另一种元素原子个数之比为2:1,根据质量守恒定律可知,E是CO2或者CaC2,CaC2中碳元素的质量分数=![]() ,CO2中碳元素的质量分数=
,CO2中碳元素的质量分数=![]() ,所以D是碳,碳和氧化钙在高温的条件下生成碳化钙,所以E是碳化钙;H是一种有刺激性气味的气体,H可能是氨气,M常用于制作糕点的发酵粉。M可能是碳酸氢钠,C(CO2)、H(NH3)、氯化钠溶液反应生成M(NaHCO3)和G,根据侯氏制碱法原理可知,NaCl + CO2+NH3+H2O=NaHCO3↓+NH4Cl,H是氨气,G是氯化铵;碳化钙和水反应生成乙炔和F,根据质量守恒定律可知,F可能是氢氧化钙,F与G加热时生成H(氨气),氢氧化钙与氯化铵加热时生成氯化钙、水和氨气,经过验证,推导正确。
,所以D是碳,碳和氧化钙在高温的条件下生成碳化钙,所以E是碳化钙;H是一种有刺激性气味的气体,H可能是氨气,M常用于制作糕点的发酵粉。M可能是碳酸氢钠,C(CO2)、H(NH3)、氯化钠溶液反应生成M(NaHCO3)和G,根据侯氏制碱法原理可知,NaCl + CO2+NH3+H2O=NaHCO3↓+NH4Cl,H是氨气,G是氯化铵;碳化钙和水反应生成乙炔和F,根据质量守恒定律可知,F可能是氢氧化钙,F与G加热时生成H(氨气),氢氧化钙与氯化铵加热时生成氯化钙、水和氨气,经过验证,推导正确。
根据以上分析可知:
(1)所以D是碳,化学式为:C,G是氯化铵,化学式为:NH4Cl;
(2)①是碳酸钙在高温的条件下生成氧化钙和二氧化碳,化学方程式为:CaCO3![]() CaO+CO2↑;②碳化钙和水反应生成乙炔和氢氧化钙,化学方程式为:CaC2+2H2O=C2H2↑+Ca(OH)2;
CaO+CO2↑;②碳化钙和水反应生成乙炔和氢氧化钙,化学方程式为:CaC2+2H2O=C2H2↑+Ca(OH)2;
(3)反应③能够发生的原因是:常温下,NaHCO3的溶解度较小而析出;
(4)乙炔和盐酸反应生成的塑料中含有氯元素,所以此种塑料不能用于食品包装。

 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案