题目内容
【题目】t2℃时,将甲、乙各80g分别放到盛有100g水的两个烧杯中,充分溶解后,恢复到t2℃,现象如图,甲和乙的溶解度曲线如图。请结合图示回答下列问题:
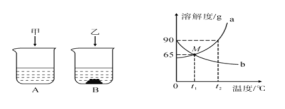
(1)能说明固体甲对应的溶解度曲线是a的证据是_______。
(2)下列关于t2 ℃时,甲、乙所得溶液的说法不正确的是______(填序号)。
A 溶质质量:甲<乙 B 乙为饱和溶液
C 溶质质量分数:甲=乙 D 将溶液降温至t1 ℃时,甲、乙的溶解度相等。
【答案】t2℃时,80g甲物质完全溶解,80g 乙物质仍有固体不溶物,t2℃时甲物质溶解度大于乙物质 AC
【解析】
(1)由溶解图像和溶解度曲线对比可知,t2℃ 时,a的溶解度为90g,b的溶解度小于60g,将甲、乙各80g分别放到盛有100g水的两个烧杯中,充分溶解后,恢复到t2℃,只有甲完全溶解,乙物质仍有固体不溶物,说明固体甲对应的溶解度曲线是a。故填: t2℃时,80g甲物质完全溶解,80g 乙物质仍有固体不溶物,t2℃时甲物质溶解度大于乙物质
(2)A、t2 ℃时,同质量的甲、乙,加入100g水中,甲完全溶解,乙有部分未溶解,所得溶液溶质质量:甲>乙,说法错误,故符合题意;
B、乙中仍有固体未溶解,故乙为饱和溶液,说法正确,故不符合题意;
C、t2 ℃时,同质量的甲、乙,加入100g水中,甲完全溶解,乙有部分未溶解,溶质质量分数:甲>乙,说法错误,故符合题意;
D、由溶解度曲线可知,t1 ℃时,甲乙的溶解度相等,说法正确,故不符合题意;
故选AC

【题目】化学实验小组同学在实验室用过氧化氢溶液制氧气。
(1)用过氧化氢和二氧化锰反应的化学方程式为:__________________________。
(2)同学们发现反应时有白雾产生,用如下两个装置来找原因,其目的是:___________。

同时又展开了下列思考与探究:
(3)催化剂MnO2的用量对反应速率是否有影响呢?
他们做了这样一组实验:每次均用30mL10%的H2O2溶液,采用不同质量MnO2粉末做催化剂,测定各次收集到500mL氧气所用的时间,结果如下:(其它实验条件均相同)
实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
MnO2粉末用量(克) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
所用时间(秒) | 17 | 8 | 6 | 3 | 2 | 2 | 2 | 2 | 2 | 2 |
请根据表中数据回答,MnO2粉末的用量对反应速率的影响是___________。
(4)H2O2溶液的溶质质量分数对反应速率是否有影响呢?小组同学又做了一组实验:
每次均取5mL30%的H2O2溶液,然后稀释成不同溶质质量分数的溶液进行实验。记录数据如下:(实验均在20℃室温下进行,其它实验条件均相同)
实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
H2O2溶液溶质质量分数 | 1% | 3% | 5% | 10% | 15% | 20% | 25% | 30% |
MnO2粉末用量(克) | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 |
收集到540mL气体时所用时间(秒) | 660 | 220 | 205 | 80 | 25 | 9 | 4 | 3 |
分析表中数据可得出的结论是___________。
(3)实验反思:MnO2颗粒的大小对反应速率是否有影响?请设计实验证明(语言叙述,不用画装置图)___________。