题目内容
【题目】五氧化二钒(V2O5)是工业上制取硫酸的催化剂,如图是制取V2O5的工艺流程
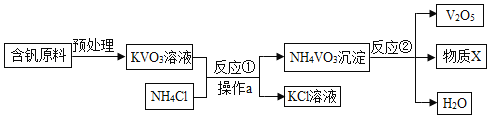
(1)操作a的名称是_____,该操作中玻璃棒起的作用是_____
(2)反应②的反应类型是_____反应,V2O5中钒的化合价是_____,物质X中一定含有的元素是_____
(3)工业上利用SO2与O2在加热并用V2O5作催化剂的条件下转化为SO3,再用SO3与水反应制取硫酸,请写出SO2转化为SO3的化学方程式_____。
【答案】过滤, 引流; 分解反应, +5, 氮元素; 2SO2+O2![]() 2SO3。
2SO3。
【解析】
(1)过滤可以将不溶性固体从溶液中分离出来,以及过滤操作中玻璃棒的作用,所以操作a的名称是过滤,该操作中玻璃棒起的作用是引流;
(2)反应②中,反应物是一种,生成物是多种,该反应属于分解反应,化合价代数和为零,氧元素通常显﹣2价,所以钒的化合价是+5,化学反应遵循质量守恒定律,即反应前后元素种类不变,原子种类、总个数和质量都不变,所以物质X中一定含有氮元素;
(3)二氧化硫和氧气在五氧化二钒的催化作用下加热生成三氧化硫,化学方程式为:2SO2+O2![]() 2SO3。
2SO3。

练习册系列答案
相关题目
【题目】某同学为测定黄铜屑(由锌和铜形成的合金)样品组.分四次取样品与稀盐酸反应,其实验数据记录见下表.
1 | 2 | 3 | 4 | |
取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
产生气体质量(g) | 0.4 | 0.8 | 1.0 | 1.0 |
试计算:
①第几次实验金属锌完全反应______.
②所用稀硫酸中溶质的质量分数_______?