题目内容
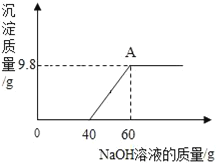
【题目】某兴趣小组为测定实验室中一瓶久置的过氧化氢溶液的溶质的质量分数,实验测得相关数据如图所示:

(1)反应生成氧气的质量为_____________g;
(2)计算该过氧化氢溶液中溶质质量分数_____________;
(3)实验表明硫酸铜溶液在该反应中也能起到二氧化锰的作用。若用5.6g无水硫酸铜代替二氧化锰进行本实验,计算剩余的溶液中溶质的质量分数_____________。(硫酸铜全部溶于水,计算时保留到0.1%)
【答案】1.6 5% 7.8%
【解析】
(1)生成氧气的质量为:68.0g+1.0g-67.4g=1.6g,故填:1.6。
(2)设过氧化氢的质量的质量为x,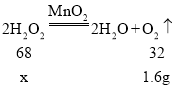
![]()
x=3.4g。
该过氧化氢溶液中溶质质量分数为:![]()
答:该过氧化氢溶液中溶质质量分数为5%。故填:5%。
(3)剩余的溶液中硫酸铜的质量分数为:![]() 。
。
答:剩余的溶液中硫酸铜的质量分数为7.8%。故填:7.8%。

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案
相关题目
【题目】有一包白色粉末,其中可能含有![]() 、
、![]() 、
、![]() 、
、![]() ,为确定该白色粉末的成分,同学们进行了有关实验,实验流程和现象如下:
,为确定该白色粉末的成分,同学们进行了有关实验,实验流程和现象如下:
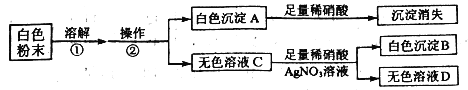
请回答以下问题。
(1)操作②的名称是________,①中发生反应的化学方程式是________。
(2)通过以上实验可知,此白色粉末中一定含有_____;一定不含_____;判断的理由是______。
(3)同学们利用下列两种方案继续对溶液D的成分进行检验,请选择一种方案进行回答。
方案一 | 方案二 | |
操作 | 取少量溶液D,向其中滴加紫色石蕊溶液,观察到溶液变为红色。 | 取少量溶液D,向其中滴加氯化钠溶液,无明显现象;再滴加碳酸钠溶液,观察到先有气泡产生,后产生白色沉淀。 |
结论 | D中所含阳离子一定有上________。 | D中所含阳离子一定有________。 |