题目内容
【题目】下列应用、相应原理(用化学方程式表示)及基本反应类型都正确的是( )
A. 用铁桶盛装稀盐酸:Fe + 2HCl = FeCl2 + H2↑ 置换反应
B. 常温下,铝具有很好的抗腐蚀性:4Al + 3O2![]() 2Al2O3 化合反应
2Al2O3 化合反应
C. 打开汽水瓶时碳酸分解: H2CO3= H2O + CO2 分解反应
D. 验证铜和铝的活动性:2Al+3CuSO4= Al2(SO4)3 +3Cu 置换反应
【答案】D
【解析】
A、铁和稀盐酸反应生成氯化亚铁和氢气;
B、常温下,铝和氧气反应生成的致密氧化物对内部的铝有保护作用;
C、打开汽水瓶,压强减小,二氧化碳的溶解度减小;
D、2Al+3CuSO4= Al2(SO4)3 +3Cu,能够验证铝比铜的活动性强,属于置换反应。
A、铁和稀盐酸反应生成氯化亚铁和氢气,不能用铁桶盛装稀盐酸,不符合题意;
B、常温下,铝和氧气反应生成的致密氧化物对内部的铝有保护作用,不需要加热,不符合题意;
C、打开汽水瓶,压强减小,二氧化碳的溶解度减小,不符合题意;
D、2Al+3CuSO4= Al2(SO4)3 +3Cu,能够验证铝比铜的活动性强,属于置换反应,符合题意。
故选D。

 名校课堂系列答案
名校课堂系列答案【题目】分类、类比是初中化学常用的学习方法。
(1)初中化学有许多实验,若按照实验方法分类,可将实验_____(填字母)分为一类;分类的依据是____________ 。
|
|
|
|
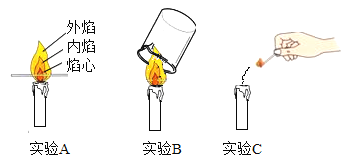
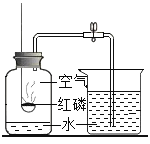
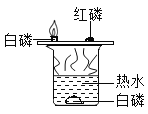
A 测定空气中氧气的含量 | B 探究可燃物燃烧 的条件 | C 探究反应前后物质的质量关系 | D 探究铁钉生锈的条件 |
(2)观察所给物质中氮元素化合价的排列规律,将合适的物质化学式填入空白处:N2 、N2O、____、N2O3、NO2。
(3)类比金属单质间的置换反应,某些非金属单质间也能发生置换反应,如 Cl2 比 Br2(溴)活泼,能与 HBr 发生反应:Cl2+2HBr=2HCl + Br2。已知 Cl2比 N2活泼,则 Cl2 与NH3 在一定条件下发生反应的化学方程式为____________________。