9. 有一无色透明溶液,欲确定是否含有下列离子:Na+、Mg2+、Al3+、Fe2+、Ba2+、
有一无色透明溶液,欲确定是否含有下列离子:Na+、Mg2+、Al3+、Fe2+、Ba2+、
 NO3-、SO42-、Cl-、I-、HCO3-,取该溶液实验如下,结论不正确的是:( )
NO3-、SO42-、Cl-、I-、HCO3-,取该溶液实验如下,结论不正确的是:( )
|
实验步骤 |
实验现象 |
|
①取少量该溶液,加几滴石蕊试剂 |
溶液变成红色 |
|
②取少量该溶液,加Cu片和浓H2SO4,加热 |
有无色气体产生,在空气中又变成红棕色 |
|
③取少量原溶液,加BaCl2溶液 |
有白色沉淀生成 |
|
④取③中上层清液,加AgNO3溶液 |
有白色沉淀生成,且不溶于稀HNO3 |
|
⑤取少量原溶液,加NaOH溶液 |
有白色沉淀生成,当NaOH过量时有部分沉淀溶解 |
A.溶液中肯定存在的离子是Al3+、NO3-、SO4 、Cl-
、Cl-
 B.溶液中肯定不存在的离子是Fe2+、Ba2+、I-、HCO3-
B.溶液中肯定不存在的离子是Fe2+、Ba2+、I-、HCO3-
 C.无法确定溶液中是否含有Na+ 、Cl-
C.无法确定溶液中是否含有Na+ 、Cl-
 D.要确定溶液中是否含Cl-,可取少量原溶液,加入足量Ba(NO3)2溶液后,取
D.要确定溶液中是否含Cl-,可取少量原溶液,加入足量Ba(NO3)2溶液后,取
 上层清液加入AgNO3溶液和稀HNO3
上层清液加入AgNO3溶液和稀HNO3
7. 设NA表示阿伏加德罗常数,下列说法正确的是( )
设NA表示阿伏加德罗常数,下列说法正确的是( )





















 A.9 g SiO2晶体中含有的硅氧键数目为0.3 NA
A.9 g SiO2晶体中含有的硅氧键数目为0.3 NA
 B.28 g乙烯和28 g丙烯中均含有6 NA对共用电子对
B.28 g乙烯和28 g丙烯中均含有6 NA对共用电子对
 C.在熔融状态下,l mol NaHSO4完全电离出的阳离子数目为2 NA
C.在熔融状态下,l mol NaHSO4完全电离出的阳离子数目为2 NA
 D.标准状况下,22.4 L氖气与22.4 L氟气所含原子数均为2 NA
D.标准状况下,22.4 L氖气与22.4 L氟气所含原子数均为2 NA

|
 A.工业上用电解法冶炼铝: 2Al2O3
(熔融) ==== 4Al+ 3O2↑
A.工业上用电解法冶炼铝: 2Al2O3
(熔融) ==== 4Al+ 3O2↑
 B.适当提高合成氨原料气中N2的含量,可提高H2的转化率
B.适当提高合成氨原料气中N2的含量,可提高H2的转化率
 C.采用离子交换膜法电解饱和食盐水制烧碱,可防止阴极室产生的Cl2进入阳极室
C.采用离子交换膜法电解饱和食盐水制烧碱,可防止阴极室产生的Cl2进入阳极室
 D.制硅酸盐水泥和普通玻璃都要用到石灰石作为原料
D.制硅酸盐水泥和普通玻璃都要用到石灰石作为原料
2.[江苏省兴化市2008-2009学年高三年级第一学期期中调研 ](10分)2008年9月24日,国家重点工程--川维20万吨合成氨项目顺利实现中间交接。合成氨是生产尿素、磷酸铵、硝酸铵等化学肥料的主要原料,工业生产过程是以天然气或煤炭等为原料通过水蒸气重整工艺制得氢气,然后在一定条件下与氮气进行合成制得合成氨。
⑴已知合成氨反应的热化学方程式如下:N2(g)+3H2(g) 2NH3(g)
2NH3(g)
△H=-92.4KJ/mol
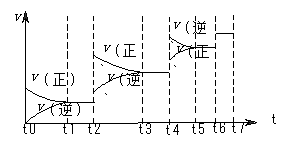
① 当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如上图所示。图中t2起平衡移动的条件可能是 。
其中表示平衡混合物中NH3的含量最高的一段时间是 。
②温度为T℃时,将2amolH2和amolN2放入0 . 5L密闭容器中,充分反应后测得N2的转化率为50﹪。则反应的平衡常数为 (用带a的代数式表示)
⑵科学家一直致力于研究常温、常压下“人工固氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。进一步研究NH3生成量与温度的关系,部分实验数据见下表(光照、压力1.0×105 Pa、反应时间3 h):
|
T/K |
303 |
313 |
323 |
353 |
|
NH3生成量/(10-6 mol) |
4.8 |
5.9 |
6.0 |
2.0 |
相应的热化学方程式如下:
N2(g)+3H2O(1)==2NH3(g)+  O2(g) △H1=+765.2 kJ·mol-1
O2(g) △H1=+765.2 kJ·mol-1
回答下列问题:
① 试在答题纸对应的图像中用虚线表示在上述反应中使用催化剂后能量的变化情况。
②与目前广泛使用的工业合成氨方法相比,该方法中固氮反应速率慢。请提出可提高其反应速率且增大NH3生成量的建议: 。


 流经皮肤血管的血液相对流量。据此判断,下列叙述
流经皮肤血管的血液相对流量。据此判断,下列叙述 如右图为植物光合作用强度随光照强度变化的坐标曲线图,分析下列叙述,不正确的是( )
如右图为植物光合作用强度随光照强度变化的坐标曲线图,分析下列叙述,不正确的是( )  下图表示人体通过体液免疫消灭破伤风杆菌外毒素的过程,下列相关叙述正确的是
下图表示人体通过体液免疫消灭破伤风杆菌外毒素的过程,下列相关叙述正确的是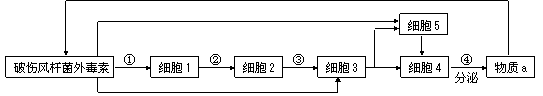
 下图是氮循环以及氮在生物体内的转化过程示意图,下列说法错误的是( )
下图是氮循环以及氮在生物体内的转化过程示意图,下列说法错误的是( )