4.(08山东省威海市08质量检测)以下物质的制备原理不正确的是
|
|
|
C.烧碱的制备:2NaCl+2H2O 2NaOH+H2↑+Cl2↑
D.漂粉精的制备:2Ca(OH)2+2Cl2=Ca(ClO)2+CaCl2+2H2O
1.(08山东省淄博高三模拟)(8分)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺,请按要求回答问题:
(1)“氨碱法”产生大量CaC12废弃物,请写出该工艺中产生CaC12的化学方程式:
;
(2)写出“联合制碱法”有关反应的化验学方程式:
; 。
(3)CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同?
;
(4)绿色化学的重要原则之一是提高反应的原子利用率。根据“联合制碱法”总反应,列出计算原子利用率的表达式:
原子利用率(%)= 。
答案(1)2NH4Cl+Ca(OH)2=====2NH3↑+CaCl2+2H2O;
|
2NaHCO3=====Na2CO3+ CO2↑+H2O;(1分)
(3)“氨碱法”的CO2来源于石灰石煅烧,“联合制碱法”的CO2来源于合成氨工业的废气。(2分)
(4)由于总反映可看作是:2NH3+2NaCl+CO2+H2O=Na2CO3+2NH4Cl,所以:原子利用率(%)
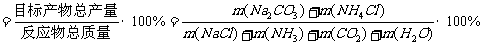 4.(08山东2、(省威海市08质量检测)下列关于工业生产的说法中,不正确的是 ( D )
4.(08山东2、(省威海市08质量检测)下列关于工业生产的说法中,不正确的是 ( D )
A.工业上,用焦炭在电炉中还原二氧化硅得到含少量杂质的粗硅
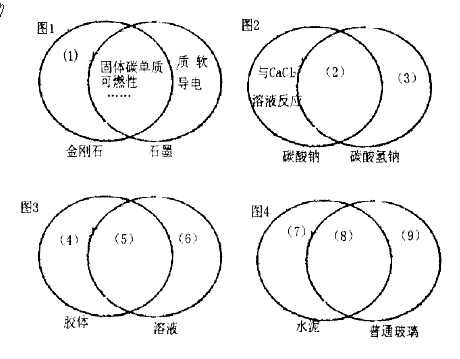
B.生产普通玻璃的主要原料有石灰石、石英和纯碱
C.工业上将粗铜进行精炼,应将粗铜连接在电源的正极
D.在高炉炼铁的反应中,焦炭为氧化剂
2.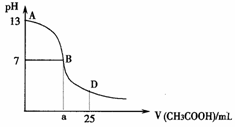 [江苏省泰州实验中学2008-2009学年度第一学期阶段Ⅱ考试 ](14分)I .右图为向25mL 0.1
mol·L-1 NaOH溶液中逐滴滴加0.2 mol·L-1 CH3COOH溶液过程中溶液pH的变化曲线。请回答:
[江苏省泰州实验中学2008-2009学年度第一学期阶段Ⅱ考试 ](14分)I .右图为向25mL 0.1
mol·L-1 NaOH溶液中逐滴滴加0.2 mol·L-1 CH3COOH溶液过程中溶液pH的变化曲线。请回答:
(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确? (选填“是”或“否”)。若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内? 区间(若正确,此问不答)
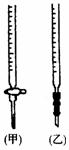
(2)关于该滴定实验,从下列选项中选出最恰当的一项 。(选填字母)
|
(3)AB区间,c(OH-)>c(H+),则c(OH-)与c(CH3COO-)大小关系
是
A.c(OH-)一定大于c(CH3COO-)
B.c(OH-)一定小于c(CH3COO-)
C.c(OH-)一定等于c(CH3COO-)
D.c(OH-)大于、小于或等于c(CH3COO-)
(4)在D点时,溶液中c(CH3COO-)+c(CH3COOH) 2c(Na+)。(填“>”、“<”或“=”)
II.t℃时,某稀硫酸溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知
a+b=13 :
(5)该温度下水的离子积常数K w的数值为 。(1分)
(6)该温度下(t℃),将100mL 0.1 mol·L-1的稀H2SO4溶液与100mL 0.4 mol·L-1的
NaOH溶液混合后(溶液体积变化忽略不计),溶液的pH= 。(2分)
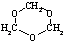 是甲醛的一种特殊商品形式,在酸的作用下,三聚甲醛可以分解为甲醛。由甲醛制取三聚甲醛的反应类型是
是甲醛的一种特殊商品形式,在酸的作用下,三聚甲醛可以分解为甲醛。由甲醛制取三聚甲醛的反应类型是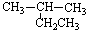 2-乙基丙烷
2-乙基丙烷
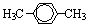 间二甲苯
间二甲苯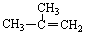 2-甲基-2-丙烯
2-甲基-2-丙烯


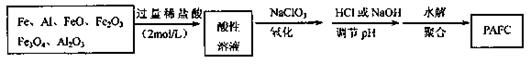 6.(08山东省威海市模拟)(14分)Ⅰ.一种新型高效净水剂PAFC(聚合氯化铁铝[AlFe(OH)uCl6-n]m),广泛用于日常生活用水和工业污水的处理。某化工厂欲以工业来生产废料(金属铁、铝及其氧化物)为原料制取PAFC,设计生产流程如下:
6.(08山东省威海市模拟)(14分)Ⅰ.一种新型高效净水剂PAFC(聚合氯化铁铝[AlFe(OH)uCl6-n]m),广泛用于日常生活用水和工业污水的处理。某化工厂欲以工业来生产废料(金属铁、铝及其氧化物)为原料制取PAFC,设计生产流程如下: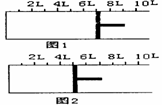 气体充入一容积可变的密闭容器中,可滑动的活塞的位置如图1所示。在恒温恒压下发生如下反应:
气体充入一容积可变的密闭容器中,可滑动的活塞的位置如图1所示。在恒温恒压下发生如下反应: 2SO2(g)+O2(g) 2SO3(g),其中△H<0。
2SO2(g)+O2(g) 2SO3(g),其中△H<0。 Ⅲ.某含0.02molNaCl与0.02molCuSO4的混合溶液200mL,常温下在恒定电压和电流的情况下进行电解,当40s时,阴极开始产生气体,100s时电解结束,此时两极产生的气体体积理论上相同,请在下图中画出阴阳两极产生气体的体积(已换成标准状况下的体积)与时间的关系图。
Ⅲ.某含0.02molNaCl与0.02molCuSO4的混合溶液200mL,常温下在恒定电压和电流的情况下进行电解,当40s时,阴极开始产生气体,100s时电解结束,此时两极产生的气体体积理论上相同,请在下图中画出阴阳两极产生气体的体积(已换成标准状况下的体积)与时间的关系图。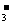 =6Fe3++Cl-+3H2O;
=6Fe3++Cl-+3H2O;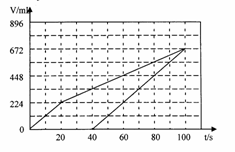 II.85.7%;1260L·mol-1
II.85.7%;1260L·mol-1