1.(严州中学2008第二次模拟)硫酸亚铁铵的化学式为(NH4)2Fe(SO4)2·6H2O,商品名为摩尔盐。硫酸亚铁可与硫酸铵生成硫酸亚铁铵,一般硫酸亚铁盐在空气中易被氧化,而形成摩尔盐后就比较稳定了。
三种盐的溶解度(单位为g/100g水)如下表:
|
温度/℃ |
10 |
20 |
30 |
40 |
50 |
70 |
|
(NH4)2SO4 |
73.0 |
75.4 |
78.0 |
81.0 |
84.5 |
91.9 |
|
FeSO4·7H2O |
40.0 |
48.0 |
60.0 |
73.3 |
- |
- |
|
(NH4)2Fe(SO4)2·6H2O |
18.1 |
21.2 |
24.5 |
27.9 |
31.3 |
38.5 |
实验室欲制备硫酸亚铁铵晶体,设计了如下方案。
(1)完成实验步骤中的填空:
①称取4g铁屑,放入小烧杯,加入15mL10%Na2CO3溶液,小火加热10min以除去_________,倒掉溶液,用蒸馏水把铁冲洗干净,干燥,备用。
②将处理好的铁屑放入小烧杯,加入15 mL 3 mol/L H2SO4溶液,水浴加热至不再有气体生成为止,趁热过滤去剩余铁屑,并用少量热水洗涤烧杯及滤纸,并将滤液和洗涤液一起转移到蒸发皿中,则蒸发皿中溶液的溶质为__________(填名称,不考虑水解), 其物质的量约为________mol。
③加入________g硫酸铵到蒸发皿中,缓缓加热、浓缩至表面出现结晶膜为止、冷却,得硫酸亚铁铵晶体。
(2)回答下列问题:
①硫酸亚铁溶液在空气中易被氧化变质,操作时应注意:步骤②中 ; 步骤③中 。
②加热、浓缩溶液时,不浓缩至干的理由是 。
③硫酸亚铁和硫酸铵的混合溶液加热浓缩就能得到硫酸亚铁铵晶体,试根据有关信息分析其原因 。
④称取两份质量均为1.96g的该硫酸亚铁铵,制成溶液。用未知浓度的KMnO4酸性溶液进行滴定。
A.滴定时,将KMnO4酸性溶液装在_______(填“酸式”或“碱式”)滴定管。
B.已知MnO4-被还原为Mn2+,试写出该滴定过程中的离子方程式:
_______________________________,
C.判断该反应到达滴定终点的现象为 。
D.假设到达滴定终点时,用去V mL KMnO4酸性溶液,则该KMnO4酸性溶液的浓度为_______mol/L。
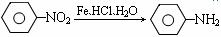 (苯胺、弱碱性、易氧化)
(苯胺、弱碱性、易氧化)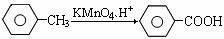
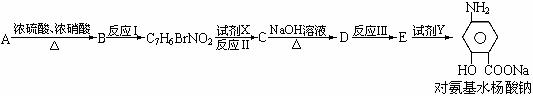
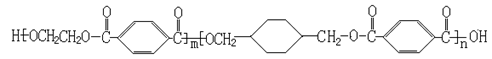


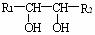 + HIO4 → R1CHO + R2CHO
+ HIO4 → R1CHO + R2CHO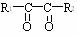 + HIO4 → R1COOH + R2COOH
+ HIO4 → R1COOH + R2COOH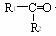
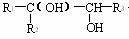 + HIO4 →
+ R3CHO
+ HIO4 →
+ R3CHO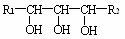 + 2HIO4 → R1CHO
+ HCOOH + R2CHO
+ 2HIO4 → R1CHO
+ HCOOH + R2CHO
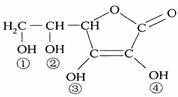 维生素C(VitaminC)又名抗坏血酸,具有酸性和强还原性,也是一种常见的食品添加剂,其结构如右图。下列有关说法中正确的是( )
维生素C(VitaminC)又名抗坏血酸,具有酸性和强还原性,也是一种常见的食品添加剂,其结构如右图。下列有关说法中正确的是( )