摘要:(一)Fe→Fe2+:铁与氧化性比较弱的非金属(如S.I2).非氧化性酸(如盐酸.稀H2SO4).不活泼金属的盐溶液(如CuSO4溶液)反应.都可实现这种转化.例如:Fe+CuSO4=Cu+FeSO4.
网址:http://m.1010jiajiao.com/timu_id_4226395[举报]
某化学兴趣小组利用实验室提供的下列试剂:铁粉、0.1mol?L-1FeCl3溶液、0.1mol?L-1FeCl2溶液、KSCN溶液、新制氯水,探究Fe2+、Fe3+ 的氧化性、还原性,并对实验结果加于应用.
(1)兴趣小组通过对Fe2+、Fe3+的价态分析,对Fe2+、Fe3+的氧化性、还原性提出了如下3种假设:
假设一:Fe2+ 具有
假设二:Fe2+ 具有
假设三:Fe3+ 具有
(2)设计实验方案,进行试验并描述实验现象,完成下列表格.
(3)该兴趣小组为说明“Fe2+具有氧化性”,提出了一个反应事实:FeCl2+Zn═ZnCl2+Fe该反应的离子方程式为:
(4)根据Fe3+的性质,该兴趣小组利用FeCl3溶液腐蚀铜箔制造印刷线路板,反应的离子方程式是:
查看习题详情和答案>>
(1)兴趣小组通过对Fe2+、Fe3+的价态分析,对Fe2+、Fe3+的氧化性、还原性提出了如下3种假设:
假设一:Fe2+ 具有
还原
还原
性;假设二:Fe2+ 具有
氧化
氧化
性;假设三:Fe3+ 具有
氧化
氧化
性;(2)设计实验方案,进行试验并描述实验现象,完成下列表格.
| 探究内容 | 实验方案 | 实验现象 | 写出下列离子方程式 |
| 探究Fe2+具有还原性 | 取少量0.1mol?L-1FeCl溶液,加入少量KSCN溶液后,再往溶液中加入少量 新制氯水 新制氯水 |
溶液先不变红,后变为血红色 | ①Fe2+发生的反应: 2Fe2++Cl2=2Fe3++2Cl- 2Fe2++Cl2=2Fe3++2Cl- |
| 探究Fe3+具有氧化性 | 取少量0.1mol?L-1FeCl溶液,加入足量 铁粉 铁粉 后,再往溶液中加入少量KSCN溶液 |
溶液不变为血红色 | Fe3+发生的反应: 2Fe3++Fe=3Fe2+ 2Fe3++Fe=3Fe2+ |
Zn+Fe2+=Fe+Zn2+
Zn+Fe2+=Fe+Zn2+
.(4)根据Fe3+的性质,该兴趣小组利用FeCl3溶液腐蚀铜箔制造印刷线路板,反应的离子方程式是:
2Fe3++Cu=2Fe2++Cu2+
2Fe3++Cu=2Fe2++Cu2+
.(2011?开封一模)“材料”的发现和使用往往会极大地推动生产、生活的发展,一些材料的出现甚至具有里程碑式划时代的意义.请你回答以下问题:
(1)无机非金属材料.高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”.这种材料可以按下列方法制备:
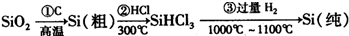
①写出步骤①的化学方程式
②步骤②经过冷凝得到的SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHCl3的主要化学操作的名称是
③请写出二氧化硅与氢氟酸反应的化学方程式
(2)磁性材料.这种材料一般含有铁元素,铁是用途最为广泛的金属,也较为活泼,所以从它的使用开始就不断实施着对它的防护.最常见的铁制品腐蚀就是电化学腐蚀,请出最为普遍的电化学腐蚀的负极反应式
(3)激光材料.我国是激光技术先进的国家,红宝石(Al2O3)是最早用于产生激光的材料,它是一种两性氧化物,请用离子方程式加以说明:
(4)纳米材料.胶体是一种物质以“纳米”颗粒的形式分散到另一种物质里形成的分散系,胶体粒子的直经大约是
(5)高分子材料.可以分成无机高分子材料和有机高分子材料.一种新型高效净水剂
[AlFe(OH)nCl6-n]m就属于无机高分子材料,广泛应用于生活用水和工业污水处理,其中铁元素的化合价为
一种合成纤维腈纶,又称“人造羊毛”,由丙烯腈(CH2=CH-CN)为原料聚合生成,请写出生成该有机高分子材料的化学方程式
 .
.
查看习题详情和答案>>
(1)无机非金属材料.高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”.这种材料可以按下列方法制备:
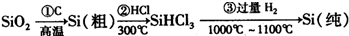
①写出步骤①的化学方程式
SiO2+2C
Si+2CO↑
| ||
SiO2+2C
Si+2CO↑
.
| ||
②步骤②经过冷凝得到的SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHCl3的主要化学操作的名称是
蒸馏(或分馏)
蒸馏(或分馏)
.③请写出二氧化硅与氢氟酸反应的化学方程式
SiO2+4HF=SiF4↑+2H2O
SiO2+4HF=SiF4↑+2H2O
.(2)磁性材料.这种材料一般含有铁元素,铁是用途最为广泛的金属,也较为活泼,所以从它的使用开始就不断实施着对它的防护.最常见的铁制品腐蚀就是电化学腐蚀,请出最为普遍的电化学腐蚀的负极反应式
Fe→Fe2++2e-
Fe→Fe2++2e-
.(3)激光材料.我国是激光技术先进的国家,红宝石(Al2O3)是最早用于产生激光的材料,它是一种两性氧化物,请用离子方程式加以说明:
Al2O3+6H+═2Al3++3H2O
Al2O3+6H+═2Al3++3H2O
,Al2O3+2OH-+3H2O=2[Al(OH)4]-
Al2O3+2OH-+3H2O=2[Al(OH)4]-
.(4)纳米材料.胶体是一种物质以“纳米”颗粒的形式分散到另一种物质里形成的分散系,胶体粒子的直经大约是
1nm~100nm
1nm~100nm
,三氯化铁溶液可以加速伤口止血,请简述原因氯化铁是电解质,使血液胶体聚沉
氯化铁是电解质,使血液胶体聚沉
.(5)高分子材料.可以分成无机高分子材料和有机高分子材料.一种新型高效净水剂
[AlFe(OH)nCl6-n]m就属于无机高分子材料,广泛应用于生活用水和工业污水处理,其中铁元素的化合价为
+3
+3
.一种合成纤维腈纶,又称“人造羊毛”,由丙烯腈(CH2=CH-CN)为原料聚合生成,请写出生成该有机高分子材料的化学方程式


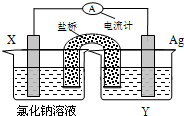 依据氧化还原反应:Cu2+(aq)+Fe(s)=Fe2+(aq)+Cu(s)设计的原电池如图所示.
依据氧化还原反应:Cu2+(aq)+Fe(s)=Fe2+(aq)+Cu(s)设计的原电池如图所示.请回答下列问题:
(1)电极X的材料是
Fe
Fe
;电解质溶液Y是CuSO4
CuSO4
;(2)X电极上发生的电极反应式为
Fe=Fe2++2e-
Fe=Fe2++2e-
.(3)针对上述原电池装置,下列说法中,不正确的是
CD
CD
.A.原电池工作时的总反应Cu2+(aq)+Fe(s)=Fe2+(aq)+Cu(s),一定为放热反应
B.原电池工作时,X电极流出电子,发生氧化反应
C.原电池工作时,银电极上发生氧化反应
D.原电池工作时,盐桥中的阳离子不断移向左池的氯化钠溶液中
(4)若Y为氯化钠溶液,则经过一段时间,发现X极上出现锈斑,则此过程中正极的电极反应式为
O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
.(1)写出下列离子方程式相对应的化学方程式
①Ca2++CO32-=CaCO3↓化学方程式:
②Cu2++Fe=Fe2++Cu化学方程式:
(2)用一种试剂除去Na2SO4溶液中含有的CuSO4.写出所用试剂及离子方程式.
除杂试剂:
(3)鉴别饱和碳酸钠溶液和澄清石灰水
可选用鉴别的试剂有(多选,填编号)
A.盐酸 B.NaCl溶液 C.硝酸 D.BaCl2溶液
依次写出鉴别中有明显现象的反应的离子方程式:
查看习题详情和答案>>
①Ca2++CO32-=CaCO3↓化学方程式:
CaCl2+Na2CO3=CaCO3↓+2NaCl
CaCl2+Na2CO3=CaCO3↓+2NaCl
②Cu2++Fe=Fe2++Cu化学方程式:
CuSO4+Fe=FeSO4+Cu
CuSO4+Fe=FeSO4+Cu
(2)用一种试剂除去Na2SO4溶液中含有的CuSO4.写出所用试剂及离子方程式.
除杂试剂:
NaOH
NaOH
(用化学式表示),离子方程式:Cu2++2OH-=Cu(OH)2↓
Cu2++2OH-=Cu(OH)2↓
.(3)鉴别饱和碳酸钠溶液和澄清石灰水
可选用鉴别的试剂有(多选,填编号)
ACD
ACD
.A.盐酸 B.NaCl溶液 C.硝酸 D.BaCl2溶液
依次写出鉴别中有明显现象的反应的离子方程式:
CO32-+2H+=CO2↑+H2O
CO32-+2H+=CO2↑+H2O
;Ba2++CO32-=BaCO3↓
Ba2++CO32-=BaCO3↓
.Ⅰ.同学甲选用下图所示仪器制备少量无水FeCl3,仪器连接顺序正确的是:
a→e→d→

Ⅱ.同学乙善于利用类比的方法学习,他根据已知资料:硝酸能把铁氧化成Fe(NO3)3,但当铁过量时,产物是Fe(NO3)2.提出一个相似的观点:氯气与铁粉反应,当C12足量时生成FeCl3,当铁粉过量时产物是FeCl2.为验证该观点是否正确,他将一根细的纯铁丝分别在足量和少量的Cl2中点燃,取其表面生成物并分别编号为A、B,然后通过实验确定其成分.探究过程如下:
(1)提出假设:A是FeCl3;B是FeCl2.
(2)设计实验方案:分别取A、B的溶液均进行以下实验.请填写下表中的相应空格.
(3)根据上述实验结论,写出Cl2与铁粉加热时发生反应的化学方程式:
(4)实际应用:FeCl3溶液常作印刷电路铜板腐蚀剂,腐蚀后的废液中含有FeCl3、FeCl2、CuCl2,同学们设计了从废液中回收Cu的方案:向废液中加入过量的铁粉,充分反应后,过滤.在所得滤渣中加入足量的盐酸,充分反后,再过滤即得到铜.该方案涉及的四种阳离子的氧化性由强到弱的顺序为:
查看习题详情和答案>>
a→e→d→
c
c
→b
b
→h
h
→j
j
→g
g
.
Ⅱ.同学乙善于利用类比的方法学习,他根据已知资料:硝酸能把铁氧化成Fe(NO3)3,但当铁过量时,产物是Fe(NO3)2.提出一个相似的观点:氯气与铁粉反应,当C12足量时生成FeCl3,当铁粉过量时产物是FeCl2.为验证该观点是否正确,他将一根细的纯铁丝分别在足量和少量的Cl2中点燃,取其表面生成物并分别编号为A、B,然后通过实验确定其成分.探究过程如下:
(1)提出假设:A是FeCl3;B是FeCl2.
(2)设计实验方案:分别取A、B的溶液均进行以下实验.请填写下表中的相应空格.
| 实验方法 | 实验现象 | 结论 |
| 分别向A、B溶液中加KSCN溶液 | 溶液变红色 溶液变红色 |
固体物质中含有FeCl3 |
| 分别向KMnO4溶液中加入适量A、B溶液 | KMnO4溶液颜色无明显变化 | 固体物质中不含 FeCl2 FeCl2 |
2Fe+3Cl2
2FeCl3
| ||
2Fe+3Cl2
2FeCl3
;
| ||
(4)实际应用:FeCl3溶液常作印刷电路铜板腐蚀剂,腐蚀后的废液中含有FeCl3、FeCl2、CuCl2,同学们设计了从废液中回收Cu的方案:向废液中加入过量的铁粉,充分反应后,过滤.在所得滤渣中加入足量的盐酸,充分反后,再过滤即得到铜.该方案涉及的四种阳离子的氧化性由强到弱的顺序为:
Fe3+>Cu2+>H+>Fe2+
Fe3+>Cu2+>H+>Fe2+
;请写出该方案涉及的反应的离子方程式:2Fe3++Fe=3Fe2+、Cu2++Fe=Fe2++Cu、2Fe3++Cu=2Fe2++Cu2+、Fe+2H+=Fe2++H2↑
2Fe3++Fe=3Fe2+、Cu2++Fe=Fe2++Cu、2Fe3++Cu=2Fe2++Cu2+、Fe+2H+=Fe2++H2↑
.