题目内容
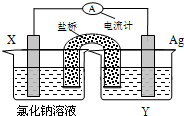 依据氧化还原反应:Cu2+(aq)+Fe(s)=Fe2+(aq)+Cu(s)设计的原电池如图所示.
依据氧化还原反应:Cu2+(aq)+Fe(s)=Fe2+(aq)+Cu(s)设计的原电池如图所示.请回答下列问题:
(1)电极X的材料是
Fe
Fe
;电解质溶液Y是CuSO4
CuSO4
;(2)X电极上发生的电极反应式为
Fe=Fe2++2e-
Fe=Fe2++2e-
.(3)针对上述原电池装置,下列说法中,不正确的是
CD
CD
.A.原电池工作时的总反应Cu2+(aq)+Fe(s)=Fe2+(aq)+Cu(s),一定为放热反应
B.原电池工作时,X电极流出电子,发生氧化反应
C.原电池工作时,银电极上发生氧化反应
D.原电池工作时,盐桥中的阳离子不断移向左池的氯化钠溶液中
(4)若Y为氯化钠溶液,则经过一段时间,发现X极上出现锈斑,则此过程中正极的电极反应式为
O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
.分析:(1)在原电池中,活泼失电子的金属为负极,得电子的阳离子是电解质中的阳离子;
(2)在原电池中,活泼失电子的金属为负极,发生失电子的氧化反应;
(3)A、原电池中所发生的反应是自发的、放热的氧化还原反应;
B、原电池工作时负极流出电子,发生氧化反应;
C、原电池工作时,正电极上发生还原反应;
D、原电池工作时,盐桥中的阳离子、电解质中的阳离子均要移向正极;
(4)金属腐蚀中常见的电化学腐蚀是吸氧腐蚀,根据吸氧腐蚀的原理来书写电极反应.
(2)在原电池中,活泼失电子的金属为负极,发生失电子的氧化反应;
(3)A、原电池中所发生的反应是自发的、放热的氧化还原反应;
B、原电池工作时负极流出电子,发生氧化反应;
C、原电池工作时,正电极上发生还原反应;
D、原电池工作时,盐桥中的阳离子、电解质中的阳离子均要移向正极;
(4)金属腐蚀中常见的电化学腐蚀是吸氧腐蚀,根据吸氧腐蚀的原理来书写电极反应.
解答:解:(1)氧化还原反应:Cu2+(aq)+Fe(s)=Fe2+(aq)+Cu(s)中,活泼的失电子的金属Fe为负极,得电子的阳离子Cu2+是电解质中的阳离子,所以电解质可以选择硫酸铜溶液,故答案为:Fe;CuSO4;
(2)在原电池反应Cu2+(aq)+Fe(s)=Fe2+(aq)+Cu(s)中,失电子的金属Fe为负极,发生失电子的氧化反应,即Fe=Fe2++2e-,故答案为:Fe=Fe2++2e-;
(3)A、只有自发的、放热的氧化还原反应才能设计成原电池,所以原电池工作时的总反应Cu2+(aq)+Fe(s)=Fe2+(aq)+Cu(s),一定为放热反应,故A正确;
B、原电池工作时,试点的金属铁为负极,流出电子,发生氧化反应,故B正确;
C、原电池工作时,银电极是正极,该极上发生还原反应,故C错误;
D、原电池工作时,盐桥中的阳离子、电解质中的阳离子均要移向正极,即移向银电极,故D错误.
故选CD;
(4)若Y为氯化钠溶液,则经过一段时间,发现Fe极上出现锈斑,则金属铁发生了电化学腐蚀中的吸氧腐蚀,正极上是阳极发生得电子的还原反应,即O2+2H2O+4e-=4OH-,故答案为:O2+2H2O+4e-=4OH-.
(2)在原电池反应Cu2+(aq)+Fe(s)=Fe2+(aq)+Cu(s)中,失电子的金属Fe为负极,发生失电子的氧化反应,即Fe=Fe2++2e-,故答案为:Fe=Fe2++2e-;
(3)A、只有自发的、放热的氧化还原反应才能设计成原电池,所以原电池工作时的总反应Cu2+(aq)+Fe(s)=Fe2+(aq)+Cu(s),一定为放热反应,故A正确;
B、原电池工作时,试点的金属铁为负极,流出电子,发生氧化反应,故B正确;
C、原电池工作时,银电极是正极,该极上发生还原反应,故C错误;
D、原电池工作时,盐桥中的阳离子、电解质中的阳离子均要移向正极,即移向银电极,故D错误.
故选CD;
(4)若Y为氯化钠溶液,则经过一段时间,发现Fe极上出现锈斑,则金属铁发生了电化学腐蚀中的吸氧腐蚀,正极上是阳极发生得电子的还原反应,即O2+2H2O+4e-=4OH-,故答案为:O2+2H2O+4e-=4OH-.
点评:本题考查学生原电池的设计、构成条件以及工作原理知识,注意平时只是的积累是解题关键,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
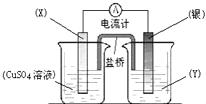 依据氧化还原反应:2Ag+(aq)+Cu(s)?Cu2+(aq)+2Ag(s)设计的原电池如图所示.下列说法不正确的是( )
依据氧化还原反应:2Ag+(aq)+Cu(s)?Cu2+(aq)+2Ag(s)设计的原电池如图所示.下列说法不正确的是( )| A、电极X的材料是铜 | B、电解质溶液Y是硝酸银溶液 | C、银电极为电池的正极,发生的电极反应为:Ag++e-?Ag | D、盐桥中的阳离子向硫酸铜溶液中运动 |
 化学科学的重要责任在于认识自然界里存在的各种各样的、奇妙的化学反应,探索纷繁的化学反应的本质和规律.通过化学反应原理模块的学习,我们可以比较深刻地理解化学科学的精髓,提高化学学科素养.请根据所学化学反应原理,解决以下问题.
化学科学的重要责任在于认识自然界里存在的各种各样的、奇妙的化学反应,探索纷繁的化学反应的本质和规律.通过化学反应原理模块的学习,我们可以比较深刻地理解化学科学的精髓,提高化学学科素养.请根据所学化学反应原理,解决以下问题. 根据所学化学反应原理,解决以下问题:
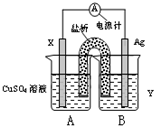
根据所学化学反应原理,解决以下问题: (2011?河西区一模)依据氧化还原反应:2Ag+(aq)+Zn(s)=2Ag(s)+Zn2+(aq)设计的原电池如图所示.下列叙述正确的是( )
(2011?河西区一模)依据氧化还原反应:2Ag+(aq)+Zn(s)=2Ag(s)+Zn2+(aq)设计的原电池如图所示.下列叙述正确的是( )