网址:http://m.1010jiajiao.com/timu_id_406150[举报]
已知在酸性溶液中,碘酸钾和亚硫酸钠会发生如下一些反应:
①![]() +3
+3![]() ====3
====3![]() +3H++I-(慢)
+3H++I-(慢)
②![]() +5I-+6H+====3I2+3H2O(慢)
+5I-+6H+====3I2+3H2O(慢)
③I2+![]() + H2O====2I-+
+ H2O====2I-+![]() +3H+(快)
+3H+(快)
分别配制下面三种溶液。
溶液A:0.9 g碘酸钾溶于少量温水中,再稀释到500 mL。
溶液B:0.45 g亚硫酸钠配成溶液,稀释到500 mL。
溶液C:取5 g可溶性淀粉,放在小烧杯中,加入25 mL冷水,搅拌成悬浊液。另取200 mL水加热至沸,趁沸腾时倒入淀粉悬浊液并迅速搅拌,使淀粉糊化、溶解。到溶液冷却后边搅拌边慢慢加入12.5 mL浓硫酸,最后也稀释到500 mL。
溶液 D:200 mL水+50 mL A液+50 mL C液
溶液 E:225 mL水+25 mL A液+50 mL C液
试完成下列问题:
(1)根据实验原理,化学反应速率由哪步反应决定_________(填“①”“②”或“③”)。
(2)当哪种离子耗尽时才能见到溶液变蓝色_____(填:“I-”“![]() ”“H+”或“
”“H+”或“![]() ”)。
”)。
(3)在盛放D液和E液的两只烧杯里同时加入50 mL B液。D、E两烧杯哪个溶液先变蓝色__________(填“D”或“E”)。
(4)为研究温度对反应速率的影响,准备三份E液(各300 mL,配法同上),用三只量筒分别量取50 mL B液,同时把三份B液分别加入下述不同温度的三份E液中。
a.第一份放在石棉网上加热到50 ℃左右,b.第二份维持在室温,c.第三份浸在冰水里冷却到近冰点。先变蓝色的是__________(填“a”“b”或“c”)。
查看习题详情和答案>>已知在酸性溶液中,碘酸钾和亚硫酸钠会发生如下一些反应
①![]() +3
+3![]() ====3
====3![]() +3H++I-(慢)
+3H++I-(慢)
②![]() +5I-+6H+====3I2+3H2O(慢)
+5I-+6H+====3I2+3H2O(慢)
③I2+![]() +H2O====2I-+
+H2O====2I-+![]() +3H+(快)
+3H+(快)
分别配制下面三种溶液。
溶液A:0.9 g碘酸钾溶于少量温水中,再稀释到500 mL。
溶液B:0.45 g亚硫酸钠配成溶液,稀释到500 mL。
溶液C:取5 g可溶性淀粉,放在小烧杯中,加入25 mL冷水,搅拌成悬浊液。另取200 mL水加热至沸,趁沸腾时倒入淀粉悬浊液并迅速搅拌,使淀粉糊化、溶解。到溶液冷却后边搅拌边慢慢加入12.5 mL浓硫酸,最后也稀释到500 mL。
溶液 D:200 mL水+50 mL A溶液+50 mL C溶液
溶液 E:225 mL水+25 mL A溶液+50 mL C溶液
试完成下列问题:
(1)根据实验原理,化学反应速率由哪步反应决定:___________(填“①”“②”或“③”)。
(2)当哪种离子耗尽时才能见到溶液变蓝色:___________ (填“I-”“![]() ”“H+”或“
”“H+”或“![]() ”)。
”)。
(3)在盛放D溶液和E溶液的两只烧杯里同时加入50 mL B溶液。D、E两烧杯中哪种溶液先变蓝色:___________ (填“D”或“E”)。
(4)为研究温度对反应速度的影响,准备三份E溶液(各300 mL,配法同上),用三只量筒分别量取50 mL B溶液,同时把三份B溶液分别加入下述不同温度的三份E溶液中:
a.第一份放在石棉网上加热到50 ℃左右,b.第二份维持在室温,c.第三份浸在冰水里冷却到近冰点。先变蓝色的是:___________(填“a”“b”或“c”)。
查看习题详情和答案>>已知在酸性溶液中,碘酸钾和亚硫酸钠会发生如下一些反应:
①![]() +3
+3![]() ====3
====3![]() +3H++I-(慢)
+3H++I-(慢)
②![]() +5I-+6H+====3I2+3H2O(慢)
+5I-+6H+====3I2+3H2O(慢)
③I2+![]() +H2O====2I-+
+H2O====2I-+![]() +3H+(快)
+3H+(快)
分别配制下面三种溶液。
溶液A:0.9 g碘酸钾溶于少量温水中,再稀释到500 mL。
溶液B:0.45 g亚硫酸钠配成溶液,稀释到500 mL。
溶液C:取5 g可溶性淀粉,放在小烧杯中,加入25 mL冷水,搅拌成悬浊液。另取200 mL水加热至沸,趁沸腾时倒入淀粉悬浊液并迅速搅拌,使淀粉糊化、溶解。到溶液冷却后边搅拌边慢慢加入12.5 mL浓硫酸,最后也稀释到500 mL。
溶液D:200 mL水+50 mL A液+500 mL C液
溶液E:225 mL水+25 mL A液+50 mL C液
试完成下列问题:
(1)根据实验原理,化学反应速率由哪步反应决定____________。(填“①”“②”或“③”)
(2)当哪种离子耗尽时才能见到溶液变蓝色____________。(填“I-”“![]() ”“H+”或“
”“H+”或“![]() ”)
”)
(3)在盛放D液和E液的两只烧杯里同时加入50 mL B液。D、E两烧杯哪个溶液先变蓝色____________(填“D”或“E”)
(4)为研究温度对反应速率的影响,准备三份E液(各300 mL,配法同上),用三只量筒分别量取50 mL B液,同时把三份B液分别加入下述不同温度的三份E液中。
a.第一份放在石棉网上加热到50 ℃左右,b.第二份维持在室温,c.第三份浸在冰水里冷却到近冰点。先变蓝色的是____________。(填“a”“b”或“c”)
查看习题详情和答案>>(1)硫代硫酸钠(Na2S2O3)是常用的还原剂.在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素C完全氧化,剩余的I2用Na2S2O3溶液滴定,可测定溶液中维生素C的含量.发生的反应为:
C6H8O6+I2═C6H6O6+2H++2I- 2S2O32-+I2═S4O62-+2I-在一定体积的某维生素C溶液中加入a mol?L-1I2溶液V1mL,充分反应后,用Na2S2O3溶液滴定剩余的I2,消耗b mol?L-1Na2S2O3溶液V2mL.
①指示剂用
②滴定终点判断方法
③该溶液中维生素C的物质的量是
(2)在酸性溶液中,碘酸钾(KIO3)被亚硫酸钠还原成I2,完成下列方程式:
生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率.某同学设计实验如下表所示:
| 0.01mol?L-1 KIO3酸性溶液(含淀粉)的体积/mL |
0.01mol?L-1 Na2SO3溶液的体积/mL |
H2O的体积 /mL |
实验温度 /℃ |
溶液出现蓝色时所需时间/s | |
| 实验1 | 5 | V1 | 35 | 25 | t1 |
| 实验2 | 5 | 5 | 40 | 25 | t2 |
| 实验3 | 5 | 5 | V2 | 0 | t3 |
(3)某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验.

请回答下列问题:
①装置A中盛放亚硫酸钠的仪器名称是
②实验过程中,装置B、C中分别说明SO2具有的性质是
③装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作、现象及结论
二氧化硫是硫的重要化合物,在生产、生活中有广泛应用。探究二氧化硫的制取和性质都有着非常重要的意义。
(1)工业上用黄铁矿(FeS2,其中S元素为-1价)在高温下和氧气反应制备SO2:

该反应中被氧化的元素是__________(填元素符号)。当该反应转移5.50mol电子时,生成的二氧化硫在标准状况下的体积为________L。
(2)①实验室可用70%的浓硫酸和亚硫酸钠反应制取二氧化硫,如果能控制反应速度,下图中可选用的发生装置是_______(填写字母)。
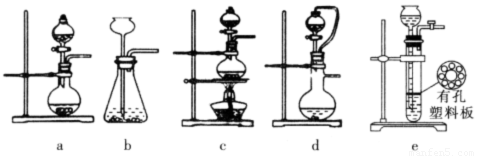
②若用硫酸和亚硫酸钠反应制取3.36L(标准状况)二氧化硫,如果已有4.0%亚硫酸钠(质量分数)被氧化成硫酸钠,则至少需称取该亚硫酸钠_______g(保留一位小数)。
(3)某化学兴趣小组设计用如图装置验证二氧化硫的化学性质。
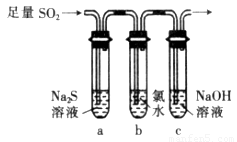
①能说明二氧化硫具有氧化性的实验现象为___________________________。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成
上述方案中合理的是________(填“Ⅰ”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为______________。
查看习题详情和答案>>