摘要:2%-4.3%
网址:http://m.1010jiajiao.com/timu_id_404870[举报]
一、1.解析:Fe Fe2+
Fe2+ Fe3+
Fe3+ Fe(OH)3
Fe(OH)3 Fe2O3。
Fe2O3。
答案:A?
2.B 3.C?
4.解析:根据2Fe3++Fe===3Fe2+知,消耗1 mol Fe生成3 mol Fe2+,还消耗2 mol Fe3+。
答案:C?
5.C 6.A 7.B 8.A 9.C 10.AD?
二、11.Fe2O3 CO和H2 Fe3O4、FeO?
12.(1)白色沉淀 灰绿色
灰绿色 红褐色沉淀?
红褐色沉淀?
(2)3Fe+2NO +8H+===3Fe2++2NO↑+4H2O?
+8H+===3Fe2++2NO↑+4H2O?
(3)由反应2HNO3+NO===3NO2+H2O知,在浓HNO3中不可能生成NO?
13.(1)Fe Cl2 H2?
(2)2Fe+3Cl2 2FeCl3
2FeCl3
(3)2HCl+Fe===FeCl2+H2↑?
(4)2FeCl2+Cl2===2FeCl3?
14.(1)Fe FeCl3 FeCl2 Fe(OH)3 Fe2O3 (2)略?
15.65 g 20.5%?
16.(1)ac?
(2)设Fe2O3原有n0 mol,还原百分率为A%,则有?


A%= ≈33.3%
≈33.3%
(3)3-
(4)Fe2O3、Fe3O4 8<a<9?
Fe3O4、FeO 6<a<8?
Fe2O3、Fe3O4、FeO 6<a<9
 ①~⑧是元素周期表中的部分元素.
①~⑧是元素周期表中的部分元素.| 族 周期 |
ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)元素③④⑧的气态氢化物中最稳定的是
HF
HF
(填化学式).(2)元素⑤和⑦的最高价氧化物对应水化物反应的离子方程式是
OH-+Al(0H)3═AlO2-+H2O
OH-+Al(0H)3═AlO2-+H2O
.(3)元素⑥和⑧形成的化合物的电子式是


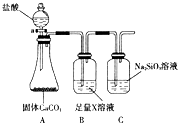
(4)某同学为了比较元素②和硅元素非金属性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验).请回答:
a.X是
NaHCO3
NaHCO3
(填化学式),B装置的作用是吸收CO2中混有的HCl气体
吸收CO2中混有的HCl气体
.b.能说明元素②和硅元素非金属性强弱的实验现象是
C中产生白色胶状沉淀
C中产生白色胶状沉淀
,相关的化学方程式是CO2+H2O+Na2SiO3=Na2CO3+H2SiO3↓
CO2+H2O+Na2SiO3=Na2CO3+H2SiO3↓
.同主族元素从上到下电子层数逐渐增加,原子半径逐渐增大
电子层数逐渐增加,原子半径逐渐增大
,得电子能力逐渐减弱,非金属性逐渐减弱.(5)请设计实验比较元素⑥与⑦金属性的相对强弱
取一小段镁条和一小片铝片,磨去表面氧化膜,分别放入2支试管中,各加入等体积等浓度的盐酸,观察发生的现象
取一小段镁条和一小片铝片,磨去表面氧化膜,分别放入2支试管中,各加入等体积等浓度的盐酸,观察发生的现象
.3,4,5-三甲氧基苯甲醛(见图)是白色或微黄色针状晶体,熔点为74~75℃.常用作磺胺增效剂、抗菌增效剂TMP的重要中间体.3,4,5-三甲氧基苯甲醛的合成路线如下:

(1)D→E转化过程中的有机反应类型属于
(2)D的同分异构体有多种.请写出含有苯环且苯环上只有一个取代基的同分异构体的结构简式
 、
、
 .
.
(3)在3,4,5-三甲氧基苯甲醛的核磁共振氢谱图上可以找到
(4)对甲氧基苯甲酸甲酯( )用于医药中间体,也用于有机合成.请结合所学有机知识并利用提示信息设计合理方案并完成以对氯甲苯和甲醇为原料合成对甲氧基苯甲酸甲酯的合成(用合成路线流程图表示,并注明反应条件).
)用于医药中间体,也用于有机合成.请结合所学有机知识并利用提示信息设计合理方案并完成以对氯甲苯和甲醇为原料合成对甲氧基苯甲酸甲酯的合成(用合成路线流程图表示,并注明反应条件).
提示:① ,
, 高温下易脱去羧基.
高温下易脱去羧基.
②
③合成过程中无机试剂任选;
④如有需要,可以利用本题中出现过的信息.
⑤合成反应流程图表示方法示例:C2H5OH
CH2=CH2

查看习题详情和答案>>

(1)D→E转化过程中的有机反应类型属于
取代
取代
反应.(2)D的同分异构体有多种.请写出含有苯环且苯环上只有一个取代基的同分异构体的结构简式




(3)在3,4,5-三甲氧基苯甲醛的核磁共振氢谱图上可以找到
4
4
种不同类型的氢原子.(4)对甲氧基苯甲酸甲酯(
 )用于医药中间体,也用于有机合成.请结合所学有机知识并利用提示信息设计合理方案并完成以对氯甲苯和甲醇为原料合成对甲氧基苯甲酸甲酯的合成(用合成路线流程图表示,并注明反应条件).
)用于医药中间体,也用于有机合成.请结合所学有机知识并利用提示信息设计合理方案并完成以对氯甲苯和甲醇为原料合成对甲氧基苯甲酸甲酯的合成(用合成路线流程图表示,并注明反应条件).提示:①
 ,
, 高温下易脱去羧基.
高温下易脱去羧基.②

③合成过程中无机试剂任选;
④如有需要,可以利用本题中出现过的信息.
⑤合成反应流程图表示方法示例:C2H5OH
| 浓H2SO4 |
| 170℃ |
| Br2 |

①~⑩是元素周期表中的十种元素:
回答下列问题:
(1)某同学对下列性质进行了对比,其中正确的是
A.原子半径:⑩>⑨>⑦
B.离子半径:⑨>④>⑦
C.非金属性:③>②>⑥
D.单质的熔点:④>⑨>⑩>⑧
E.单质的氧化性:③>⑦>⑧
(2)用合适的化学用语回答:
金属性最强的元素离子结构示意图为
 ,常温下呈液态的氢化物的结构式为:
,常温下呈液态的氢化物的结构式为:
(3)在上述元素中,②、⑧元素形成的气态氢化物可以相互反应,该反应的化学方程式为
查看习题详情和答案>>
| 主族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | ① | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
(1)某同学对下列性质进行了对比,其中正确的是
CD
CD
.A.原子半径:⑩>⑨>⑦
B.离子半径:⑨>④>⑦
C.非金属性:③>②>⑥
D.单质的熔点:④>⑨>⑩>⑧
E.单质的氧化性:③>⑦>⑧
(2)用合适的化学用语回答:
金属性最强的元素离子结构示意图为


H-O-H
H-O-H
.(3)在上述元素中,②、⑧元素形成的气态氢化物可以相互反应,该反应的化学方程式为
NH3+HCl═NH4Cl
NH3+HCl═NH4Cl
;⑨、⑤元素形成的最高价氧化物的水化物可以相互反应,该反应的离子方程式为Al(OH)3+OH-═AlO2-+2H2O
Al(OH)3+OH-═AlO2-+2H2O
.

 合成高分子化合物
合成高分子化合物 合成反应流程图表示方法示例如下:
合成反应流程图表示方法示例如下:
