摘要:(1)若以A点表示25℃时的电离平衡时离子的浓度.当温度升高到100℃.水的电离平衡状态到B点.则此时水的离子积从 增加到 .造成水的离子积增人的原因是 . (2)25℃时.将pH = 10的Ba (OH)2溶液与pH = 3的盐酸溶液混合.若所得混合溶液为中性.则Ba(OH)2溶液与盐酸溶液的体积比为 . (3)100℃时.将pH = 8的NaOH溶液与pH = 5的硫酸溶液混合.若所得混合溶液的pH = 7.则NaOH溶液与硫酸溶液的体积比为 .(4)100℃时.若10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性.则混合之前.该强酸的pH1与强碱的pH2溶液之间应满足的关系是 .
网址:http://m.1010jiajiao.com/timu_id_217402[举报]
 水的电离平衡曲线如图所示.
水的电离平衡曲线如图所示.(1)若以A点表示25℃时水的电离平衡的离子浓度,当温度升高到100℃时,水的电离平衡状态移动到B点,则此时水的离子积从
10-14
10-14
变化到10-12
10-12
.(2)将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合,并保持100℃的恒温,致使混合溶液的pH=7,则Ba(OH)2和盐酸的体积比为
2:9
2:9
.(3)已知AnBm的离子积为[c(Am+)]n[c(Bn-)]m,式中c(Am+)n和c(Bn-)m表示离子的物质的量浓度.在某温度下,Ca(OH)2的溶解度为0.74g,其饱和溶液密度设为1g/mL,其离子积约为
4×10-3
4×10-3
. 水的电离平衡曲线如图所示.?
水的电离平衡曲线如图所示.?(1)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从
10-14
10-14
增加到10-12
10-12
.(2)将常温下的pH=8的Ba(OH)2溶液升至100℃,则Ba(OH)2溶液的pH:
B
B
.A、>10 B、=6 C、6~8 D、>8 E、不能确定
(3)已知AnBm的离子积=[c(Am+)]n?[c(Bn-)]m?,式中c(Am+)n和c(Bn-)m表示离子的物质的量浓度幂.在某温度下,Ca(OH)2的浓度为0.02mol?L-1,其离子积为
3.2×10-5mol3/L3
3.2×10-5mol3/L3
. 水的电离平衡曲线如图所示.
水的电离平衡曲线如图所示.(1)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从
10-14
10-14
增加到10-12
10-12
.(填写具体数值)(2)在25℃时将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合,并保持25℃的恒温,欲使混合溶液pH=7,则Ba(OH)2与盐酸的体积比为
10:1
10:1
. 水的电离平衡曲线如图所示.?
水的电离平衡曲线如图所示.?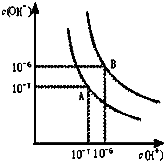 水的电离平衡曲线如图所示.
水的电离平衡曲线如图所示.