题目内容
 水的电离平衡曲线如图所示.
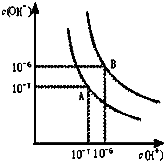
水的电离平衡曲线如图所示.(1)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从
(2)100℃时,将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合,并保持恒温,欲使混合溶液pH=7,则Ba(OH)2与盐酸的体积比为
(3)若0.1mol/L NaHA溶液的pH=2,则0.1mol/L H2A溶液中氢离子的物质的量浓度应
分析:(1)根据水的离子积表达式KW=c(H+)?c(OH-)进行计算;
(2)设氢氧化钡的体积为x,盐酸的体积为y,根据题中数据列式计算出体积之比;
(3)0.1mol?L-1H2A溶液,H2A═H++HA-,电离出0.1mol/LH+,0.1mol?L-1NaHA溶液的pH=2,则由HA-?H++A2-可知,电离出0.01mol/LH+,但第一步电离生成的H+抑制了HA-的电离.
(2)设氢氧化钡的体积为x,盐酸的体积为y,根据题中数据列式计算出体积之比;
(3)0.1mol?L-1H2A溶液,H2A═H++HA-,电离出0.1mol/LH+,0.1mol?L-1NaHA溶液的pH=2,则由HA-?H++A2-可知,电离出0.01mol/LH+,但第一步电离生成的H+抑制了HA-的电离.
解答:解:(1)25℃时纯水中C(H+)=c(OH-)=10-7 mol/L,Kw=c(H+).c(OH-)=10-14 ,当温度升高到100℃,纯水中c(H+)=c(OH-)=10-6 mol/L,Kw=c(H+).c(OH-)=10-12 ;
故答案为:10-14,10-12;
(2)将pH=8的Ba(OH)2溶液中c(OH-)=10-4 mol/L,pH=5的稀盐酸中c(H+)=10-5 mol/L,设氢氧化钡的体积为x,盐酸的体积为y,混合溶液的pH=7,溶液呈碱性,c(OH-)=
=10-5 mol/L,c(OH-)=
=10-5 mol/L,
解得 x:y=2:9,
故答案为:2:9;
(3)0.1mol?L-1H2A溶液,H2A═H++HA-,电离出0.1mol/LH+,0.1mol?L-1NaHA溶液的pH=2,则由HA-?H++A2-可知,电离出0.01mol/LH+,但第一步电离生成的H+抑制了HA-的电离,所以溶液中氢离子的物质的量浓度小于0.1mol/L+0.01mol/L,
故答案为:<;H2A第一步电离生成的H+抑制了HA-的电离.
故答案为:10-14,10-12;
(2)将pH=8的Ba(OH)2溶液中c(OH-)=10-4 mol/L,pH=5的稀盐酸中c(H+)=10-5 mol/L,设氢氧化钡的体积为x,盐酸的体积为y,混合溶液的pH=7,溶液呈碱性,c(OH-)=
| 10-12 |
| 10-7 |
| 10-4x-10-5y |
| x+y |
解得 x:y=2:9,
故答案为:2:9;
(3)0.1mol?L-1H2A溶液,H2A═H++HA-,电离出0.1mol/LH+,0.1mol?L-1NaHA溶液的pH=2,则由HA-?H++A2-可知,电离出0.01mol/LH+,但第一步电离生成的H+抑制了HA-的电离,所以溶液中氢离子的物质的量浓度小于0.1mol/L+0.01mol/L,
故答案为:<;H2A第一步电离生成的H+抑制了HA-的电离.
点评:本题考查了弱电解质的电离、溶液pH简单计算,题目难度不大,注意掌握水的离子积表达式,明确“混合溶液呈中性,即强酸和强碱反应时氢离子和氢氧根离子的物质的量相等”即可分析解答.

练习册系列答案
相关题目
 水的电离平衡曲线如图所示.
水的电离平衡曲线如图所示. (2006?成都模拟)水的电离平衡曲线如图所示:
(2006?成都模拟)水的电离平衡曲线如图所示: (2012?济南一模)(1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100°C时水的电离达平衡时的离子浓度.100℃时1mol?L-1 的NaOH溶液中,由水电离出的c(H+)=
(2012?济南一模)(1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100°C时水的电离达平衡时的离子浓度.100℃时1mol?L-1 的NaOH溶液中,由水电离出的c(H+)= (2011?烟台模拟)水的电离平衡曲线如图所示:
(2011?烟台模拟)水的电离平衡曲线如图所示: