摘要:12.有Fe2+.NO3-.Fe3+.NH.H+和H2O六种粒子.它们都是同一氧化还原反应中的反应物或生成物.下列叙述不正确的是 ( ) A.该反应中氧化剂与还原剂物质的量之比为1︰8 B.若有lmol NO 发生还原反应.转移电子数为5mol C.该反应说明Fe (NO3)2溶液不宜加酸酸化 D.若把该反应设计成原电池.负极反应为Fe2+-e- =Fe 3+
网址:http://m.1010jiajiao.com/timu_id_1745897[举报]
有Fe2+、NO 、Fe3+、NH
、Fe3+、NH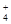 、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是( )
、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是( )
A. 氧化剂与还原剂的物质的量之比为1:8
B. 该过程说明Fe(NO3)2 溶液不宜加酸酸化
C. 若有1 mol NO 发生氧化反应,则转移8 mol电子
发生氧化反应,则转移8 mol电子
D. 若把该反应设计为原电池,则负极反应为Fe2+ — e- = Fe3+
查看习题详情和答案>>
有Fe2+、NO![]() 、Fe3+、NH
、Fe3+、NH![]() 、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是( )
、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是( )
A. 氧化剂与还原剂的物质的量之比为1:8
B. 该过程说明Fe(NO3)2溶液不宜加酸酸化
C. 若有1 mol NO![]() 发生氧化反应,则转移8 mol电子
发生氧化反应,则转移8 mol电子
D. 若把该反应设计为原电池,则负极反应为Fe2+ — e-= Fe3+
查看习题详情和答案>>
有Fe2+、NO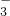 、Fe3+、NH
、Fe3+、NH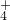 、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是
、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是
- A.氧化剂与还原剂的物质的量之比为1:8
- B.该过程说明Fe(NO3)2 溶液不宜加酸酸化
- C.若有1mol NO
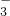 发生氧化反应,则转移8mol电子
发生氧化反应,则转移8mol电子 - D.若把该反应设计为原电池,则负极反应为Fe2+-e-═Fe3+
有Fe2+、NO![]() 、Fe3+、NH
、Fe3+、NH![]() 、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是( )
、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是( )
A. 氧化剂与还原剂的物质的量之比为1:8
B. 该过程说明Fe(NO3)2 溶液不宜加酸酸化
C. 若有1 mol NO![]() 发生氧化反应,则转移8 mol电子
发生氧化反应,则转移8 mol电子
D. 若把该反应设计为原电池,则负极反应为Fe2+ — e- = Fe3+
查看习题详情和答案>>在一些地质灾害之后,为防止在灾后疫病流行,会使用大量的各种消毒剂、漂白剂等.
(1)二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与SO2反应制得.请写出反应的离子方程式:
(2)过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3?3H2O2,它具有Na2CO3和H2O2的双重性质.过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠只发生了氧化反应的是
A.MnO2 B.KMnO4溶液 C.稀盐酸 D.Na2SO3溶液
(3)漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平).当1mol HClO2发生分解反应时,转移的电子数是:
(4)有Fe2+、NO3-、Fe3+、NH4+、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,则该反应中氧化剂与还原剂的物质的量之比为
查看习题详情和答案>>
(1)二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与SO2反应制得.请写出反应的离子方程式:
2ClO3-+SO2=2ClO2+SO42-
2ClO3-+SO2=2ClO2+SO42-
.(2)过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3?3H2O2,它具有Na2CO3和H2O2的双重性质.过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠只发生了氧化反应的是
B
B
.A.MnO2 B.KMnO4溶液 C.稀盐酸 D.Na2SO3溶液
(3)漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平).当1mol HClO2发生分解反应时,转移的电子数是:
0.8NA(4.816×1023)
0.8NA(4.816×1023)
.(4)有Fe2+、NO3-、Fe3+、NH4+、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,则该反应中氧化剂与还原剂的物质的量之比为
1:8
1:8
.