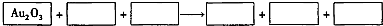摘要:⑴Au2O3.Na2S2O3.H2O.Na2S4O6.Au2O.NaOH ⑵Au(+3) Na2S2O3 ⑶ ⑷1:4 本资料由 提供!
网址:http://m.1010jiajiao.com/timu3_id_49776[举报]
在下列物质中:NaCl、NaOH、Na2S、H2O2、Na2S2、(NH4)2S、CO2、CCl4、C2H2、SiO2、SiC、晶体硅、金刚石.
(1)其中只含有离子键的离子晶体是
(2)其中既含有离子键又含有极性共价键的离子晶体是
(3)其中既含有离子键,又含有极性共价键和配位键的离子晶体是
(4)其中既含有离子键又含有非极性共价键的离子晶体是
(5)其中含有极性共价键的非极性分子是
(6)其中含有极性共价键和非极性共价键的非极性分子是
(7)其中含有极性共价键和非极性共价键的极性分子是
(8)其中含有极性共价键的原子晶体是
查看习题详情和答案>>
(1)其中只含有离子键的离子晶体是
NaCl、Na2S
NaCl、Na2S
;(2)其中既含有离子键又含有极性共价键的离子晶体是
NaOH、(NH4)2S
NaOH、(NH4)2S
;(3)其中既含有离子键,又含有极性共价键和配位键的离子晶体是
(NH4)2S
(NH4)2S
;(4)其中既含有离子键又含有非极性共价键的离子晶体是
Na2S2
Na2S2
;(5)其中含有极性共价键的非极性分子是
CO2、CCl4、C2H2
CO2、CCl4、C2H2
;(6)其中含有极性共价键和非极性共价键的非极性分子是
C2H2
C2H2
;(7)其中含有极性共价键和非极性共价键的极性分子是
H2O2
H2O2
;(8)其中含有极性共价键的原子晶体是
SiC
SiC
.(2008?上海)某反应体系中的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O.
(1)请将Au2O3之外的反应物与生成物分别填入以下空格并配平.
+
(2)反应中1mol还原剂
(3)纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白后布匹的“脱氯剂”,Na2S2O3和Cl2反应的产物是H2SO4、NaCl和HCl,则还原剂和氧化剂物质的量之比为
查看习题详情和答案>>
(1)请将Au2O3之外的反应物与生成物分别填入以下空格并配平.
+
4Na2S2O3
4Na2S2O3
+2H2O
2H2O
=Au2O
Au2O
+2Na2S4O6
2Na2S4O6
+4NaOH
4NaOH
(2)反应中1mol还原剂
失去
失去
(填“得到”或“失去”)1
1
mol电子.(3)纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白后布匹的“脱氯剂”,Na2S2O3和Cl2反应的产物是H2SO4、NaCl和HCl,则还原剂和氧化剂物质的量之比为
1:4
1:4
.下图是一种正在投入生产的大型蓄电系统.左右两侧为电解质储罐,中央为电池,电解质通过泵不断在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过;放电前,被膜隔开的电解质为Na2S2和NaBr3,放电后,分别变为Na2S4和NaBr.

(1)左、右储罐中的电解质分别为:左
(2)写出电池充电时,阳极和阴极的电极反应式.
阳极:
阴极:
(3)写出电池充、放电的反应方程式:
(4)指出在充电过程中钠离子通过膜的流向:
查看习题详情和答案>>

(1)左、右储罐中的电解质分别为:左
NaBr3/NaBr
NaBr3/NaBr
,右Na2S2/Na2S4
Na2S2/Na2S4
.(2)写出电池充电时,阳极和阴极的电极反应式.
阳极:
3NaBr-2e-=NaBr3+2Na+(或3Br--2e-=Br3-)
3NaBr-2e-=NaBr3+2Na+(或3Br--2e-=Br3-)
,阴极:
Na2S4+2Na++2e-=2Na2S2(或S42-+2e-=2S22-)
Na2S4+2Na++2e-=2Na2S2(或S42-+2e-=2S22-)
.(3)写出电池充、放电的反应方程式:
2Na2S2+NaBr3
Na2S4+3NaBr
| 放电 |
| 充电 |
2Na2S2+NaBr3
Na2S4+3NaBr
.| 放电 |
| 充电 |
(4)指出在充电过程中钠离子通过膜的流向:
Na+的流向为从左到右
Na+的流向为从左到右
.短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉D和气体E,D既能溶于强酸,也能溶于强碱.E在足量空气中燃烧产生刺激性气体G,G在大气中能导致酸雨的形成.E被足量氢氧化钠溶液吸收得到无色溶液F.溶液F在空气中长期放置发生反应,生成物之一为H.H与过氧化钠的结构和化学性质相似,其溶液显黄色.
请回答下列问题:
(1)组成单质A的元素在周期表中的位置是
(2)组成单质B的元素的原子结构示意图为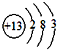
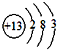 .
.
(3)G与氯酸钠在酸性条件下反应可生成消霉杀菌剂二氧化氯.该反应的氧化剂为
(4)溶液F在空气中长期放置生成H的化学反应万程式为:
(5)H的溶液与稀硫酸反应产生的现象为
查看习题详情和答案>>
请回答下列问题:
(1)组成单质A的元素在周期表中的位置是
第三周期 第ⅥA族
第三周期 第ⅥA族
.(2)组成单质B的元素的原子结构示意图为
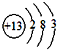
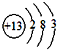
(3)G与氯酸钠在酸性条件下反应可生成消霉杀菌剂二氧化氯.该反应的氧化剂为
氯酸钠(NaClO3)
氯酸钠(NaClO3)
.(4)溶液F在空气中长期放置生成H的化学反应万程式为:
4Na2S+O2+2H2O═4NaOH+2Na2S2(或2Na2S+O2+2H2O═4NaOH+2S,Na2S+S═Na2S2)
4Na2S+O2+2H2O═4NaOH+2Na2S2(或2Na2S+O2+2H2O═4NaOH+2S,Na2S+S═Na2S2)
.(5)H的溶液与稀硫酸反应产生的现象为
溶液由黄色变为无色,产生浅黄色沉淀和臭鸡蛋气味的气体
溶液由黄色变为无色,产生浅黄色沉淀和臭鸡蛋气味的气体
.